
【题目】根据题意填空
(1)苯的2氯取代有种,则其4氯取代有种.
(2)实验室中苯与液溴反应的方程式为 ,
(3)制得的产物常显褐色原因是 , 除去颜色的简单步骤是 , 其中相关化学方程式是
【答案】
(1)3;3
(2)![]()
(3)产物中溶有未反应的溴;向产物中加入稀氢氧化钠溶液洗涤,除去溴,然后再通过分液漏斗进行分液操作,除去溴化钠;Br2+2NaOH=NaBr+NaBrO+H2O
【解析】解:(1)苯的2氯取代有邻、间、对3种,则4氯取代也有3种,所以答案是:3;3;(2)在催化条件下,苯与液溴发生取代反应生成溴苯,方程式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(3)因溴易溶于苯,所得溴苯常显褐色,可用氢氧化钠溶液除去溴,反应的方程式为Br2+2NaOH=NaBr+NaBrO+H2O,除去颜色的简单步骤是向产物中加入稀氢氧化钠溶液洗涤,除去溴,然后再通过分液漏斗进行分液操作,除去溴化钠,
;(3)因溴易溶于苯,所得溴苯常显褐色,可用氢氧化钠溶液除去溴,反应的方程式为Br2+2NaOH=NaBr+NaBrO+H2O,除去颜色的简单步骤是向产物中加入稀氢氧化钠溶液洗涤,除去溴,然后再通过分液漏斗进行分液操作,除去溴化钠,
所以答案是:产物中溶有未反应的溴;向产物中加入稀氢氧化钠溶液洗涤,除去溴,然后再通过分液漏斗进行分液操作,除去溴化钠;Br2+2NaOH=NaBr+NaBrO+H2O.


科目:高中化学 来源: 题型:
【题目】利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.上述电池工作时,有关说法正确的是( ) 
A.铝罐将逐渐被腐蚀
B.碳粒和炭棒上发生的反应为:O2+4e﹣=2O2﹣
C.炭棒应与玩具电机的负极相连
D.该电池工作一段时间后炭棒和炭粒的质量会减轻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 氧化还原反应中氧化剂失电子总数等于还原剂得电子总数
B. 电解质不一定导电,导电的物质不一定是电解质
C. 任何化学反一定都遵循质量守恒,是离子反应的还要遵循电荷守恒
D. 离子方程式不仅可以表示一个具体的反应,而且可以表示所有同一类型的离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
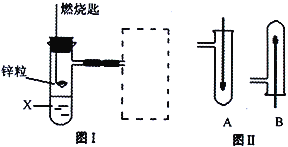
【题目】(1)图Ⅰ是实验室用H2还原CuO实验的简易装置,其中的铜质燃烧匙可以在试管中上下移动,虚线框中需从图Ⅱ中选取装置。图Ⅱ中的细铜丝一端被弯成螺旋状,实验时,先在酒精灯火焰上加热,变黑后再迅速伸入制得的H2中。
①在图Ⅰ中,X溶液应选用______。
A.稀硫酸 B.浓硫酸 C.NaCl溶液
②在图Ⅰ虚线框中,应选用图Ⅱ中的_______(填A或B)装置。
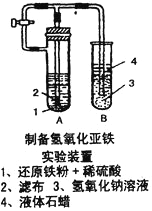
(2)某学生设计了一个制取氢氧化亚铁的实验方案,实验装置见上右图,请分析实验过程:
①在B试管中加入NaOH溶液后加热煮沸l-2分钟并立即加入2mL液体石蜡,上述操作中加热煮沸的目的是:_____________________________。
②在具支试管A中加入稀H2SO4溶液和略微过量的铁粉,分析为什么铁粉要过量_____________。
③连接好导管,同时打开活栓,当铁粉与稀硫酸反应平稳时,关闭活栓,这时看到A试管中_________(填现象),B试管中_________(填现象)。
④如果B中产生的氢氧化亚铁遇到空气,出现的现象是_______________,发生变化的化学方程式为_____________。
(3)现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。
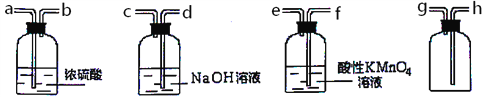
①要达到实验目的,按气流从左到右,各接口连接顺序正确的是_______。
A.dcabh B.feabh C.feabg
②本实验除去SO2的原理是利用SO2的________性质(填序号)。
A.氧化性 B.漂白性 C.还原性 D.酸性
③SO2与酸性高锰酸钾反应的离子方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某些离子或物质的检验所用试剂或方法不正确的是
A. 某溶液中加入盐酸产生气体,则其中一定含有CO32-
B. 用焰色反应检验钠元素的存在
C. 用氢氧化钠溶液和湿润的红色石蕊试纸检验NH4+
D. 用盐酸和氯化钡溶液检验 SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X(g)+Y(g)2Z(g);正反应放热.从反应开始经过t1后达到平衡状态,t2 时由于条件改变,平衡受到破坏,在t3时又达到平衡,据如图回答:从t2→t3的曲线变化是由哪种条件引起的( ) 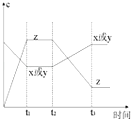
A.增大X或Y的浓度
B.增大压强
C.增大Z的浓度
D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为:PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( ) 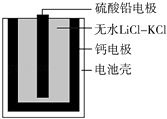
A.正极反应式:Ca+2Cl﹣﹣2e﹣═CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1 mol电子,理论上生成20.7 g Pb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com