
【题目】(题文)海洋是一座巨大的化学资源宝库,从中可以提取许多常见的化学物质,结合所学知识回答下列问题,
(1)“吹出法”提溴空气吹出法是工业规模提溴的常用方法,其流程如下:
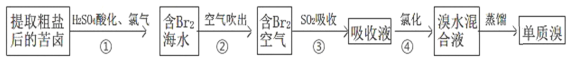
其中步骤②~④的目的是________________________________________________。步骤③反应的离子方程式为_______________________________。除SO2外,步骤③还可以选用Na2CO3溶液吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移电子的物质的量为____________mol。
(2)实验室模拟从海带中提取碘,可能经历如下操作(或过程),请选择必要的操作(或过程),并按实验的先后顺序排列___________________________(填写编号)
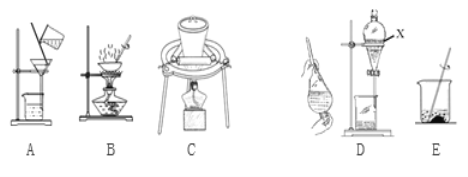
(3)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按下图流程制备轻质氧化镁,若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,回答下列问题:

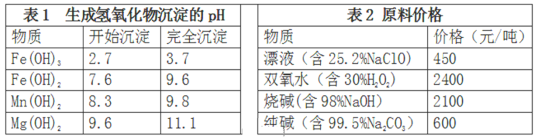
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去。
步骤①反应的离子方程式为:_____________________________________;
步骤②的反应方程式为:_________________________________________。
【答案】富集溴元素(或提高溴水浓度)SO2+Br2+2H2O=4H++SO42-+2Br-5/3CEADClO-+2H++2Fe2+=2Fe3++Cl-+H2OMgCO3+H2O![]() Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
【解析】
(1)氧化后的海水虽然含有溴单质,但浓度低,如県直接蒸馏原料,生产成本高。“空气吹出、SO2吸收、氧化”的过程实际上是一个Br2的浓缩过程;Na2CO3溶液吸收溴反应配平可得:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6 NaHCO3,其中溴与转移的电子的关系为:3Br2-5e-,故答案为:富集元素(或提高溴水浓度)、SO2+Br2+2H2O=4H++SO42-+2Br-;吸收1molBr2时,转移电子的物质的量为![]() mol;
mol;
(2)由从海带中提取碘的实验分析可得结论,故答案为CEAD;
(3)步骤①是为了将Fe2+氧化成Fe3+,并在控制合通适的pH条件时生成Fe(OH)3沉淀而除之,虽然漂液和H2O2都可采用,但对比表2提供的原料价格可以看出,漂液比H2O2的价格低得多,所以选漂液最合理,故X为漂液;加入Y的目的是使镁离子沉淀,Y为纯碱,故答案为:ClO-+2H++2Fe2+=2Fe3++Cl-+H2O、MgCO3+H2O![]() Mg(OH)2+CO2↑。
Mg(OH)2+CO2↑。


科目:高中化学 来源: 题型:
【题目】德国化学家F.Haber利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是( )
分别表示N2、H2、NH3,下列说法正确的是( )
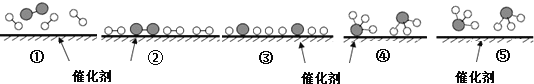
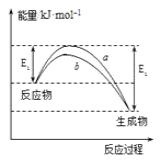
A. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
B. 催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C. 在该过程中,N2、H2断键形成N原子和H原子
D. 使用催化剂,合成氨反应放出的热量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 32.5g锌粒与足量盐酸反应产生11.2 L H2
B. 标准状况下,11.2 L CCl4所含分子数为0.5NA
C. 1mol NaHSO4中含有的阴阳离子的总数目为 3NA
D. 常温常压下,40g O2和O3的混合气体中,含有氧原子的数目为2.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
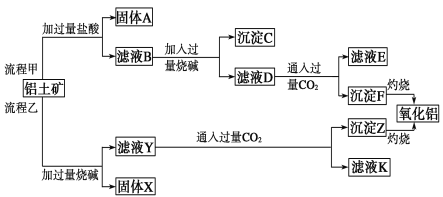
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_______________________。
(2)流程乙加入烧碱后生成AlO2-的离子方程式为____________________。
(3)滤液E、K中溶质的主要成分是__________(填化学式)。
(4)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
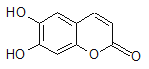
A、2 mol Br2 2 mol NaOH
B、2 mol Br2 3 mol NaOH
C、3 mol Br2 4 mol NaOH
D、4 mol Br2 4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为______________。
(2)A与溴的四氯化碳溶液反应的化学方程式为_________________________________,反应类型是________。
(3)已知:![]()
![]()
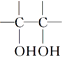 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应产物的结构简式:_____________________。
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应产物的结构简式:_____________________。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式_________________________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水作还原剂的是
A. 2H2O+2F2=4HF+O2 B. 2Na2O2+2H2O=4NaOH+O2↑
C. 2Na+2H2O=2NaOH+H2↑ D. 2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 金属钠投入到足量的稀盐酸中: Na+2H+==Na++H2↑
B. CuO溶解在稀盐酸中:O2-+2H+==H2O
C. 氢氧化钡溶液与稀硫酸反应:Ba2++SO![]() +H++OH-== BaSO4↓+H2O
+H++OH-== BaSO4↓+H2O
D. 碳酸氢钙溶液与稀盐酸反应:HCO![]() +H+==H2O+CO2↑
+H+==H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 油脂在碱性条件下水解可生成高级脂肪酸盐和甘油
B. 淀粉、纤维素和蔗糖都属于糖类,一定条件下水解都只生成葡萄糖
C. 蛋白质在紫外线、CuSO4溶液、福尔马林作用下均会发生变性
D. 二氧化碳和环氧丙烷(![]() )在催化剂作用下可生成一种可降解的塑料
)在催化剂作用下可生成一种可降解的塑料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com