
【题目】某密闭容器中放入一定量的NO2,发生反应2NO2(g)![]() N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,有可能使平衡混合气体平均相对分子质量减小的是
N2O4(g) △H<0,在达平衡后,若分别单独改变下列条件,重新达到平衡后,有可能使平衡混合气体平均相对分子质量减小的是
A.通入NO2B.通入N2O4C.通入N2D.降低温度
【答案】C
【解析】
混合气体平均相对分子质量=![]() ;
;
A.通入NO2后如果达到的是等效平衡,则气体平均相对分子质量不变,但由于容器体积不变所以压强增大平衡会正向移动,气体的物质的量减小,平均相对分子质量会增大,故A错误;
B.通入N2O4后如果达到的是等效平衡,则气体平均相对分子质量不变,但由于容器体积不变所以压强增大平衡会正向移动,气体的物质的量减小,平均相对分子质量会增大,故B错误;
C.通入N2,氮气虽不参与反应,但是氮气的相对分子质量要比NO2的相对分子质量小,所以体系平均相对分子质量会减小,故C正确;
D.该反应焓变小于零,正反应为放热反应,降低温度平衡右移,气体的物质的量减小,平均相对分子质量会增大,故D错误;
故答案为C。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.100molL-1的NH4SCN溶液滴定25.00mL0.100molL-1AgNO3溶液,以NH4Fe(SO4)212H2O为指示剂,测得溶液中pSCN=lgc(SCN-)、pAg=lgc(Ag+)随加入NH4SCN溶液的体积变化如图所示。已知:Ag++SCN-AgSCN↓,Ksp(Ag2SO4)=1.4×10-5。下列说法错误的是( )

A.滴定至终点时溶液颜色变为红色,且振荡后不褪色
B.该温度下AgSCN的溶度积常数Ksp=1.0×10-12
C.为防止指示剂失效,溶液应维持酸性
D.当加入15.00mLNH4SCN溶液时,溶液中c(SO42-)=0.14molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组采用电渗析法从含NH4H2PO4 和(NH4)2HPO4的废水中回收NH3·H2O和 H3PO4,装置如图所示。下列说法错误的是( )
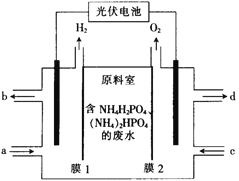
A.膜1为阳离子交换膜,膜2为阴离子交换膜
B.a处进入稀氨水,d处流出浓H3PO4溶液
C.阴极区总反应式为2H2O+2NH4++2e-=2NH3·H2O+H2↑
D.每放出11.2L(标准状况)H2时,能回收98gH3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①___;
b.若B、C都不是气体,气体的平均相对分子质量②____;
c.若B是气体,C不是气体,气体的平均相对分子质量③___;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④___态,C是⑤___态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______。装置A中试剂是_______。
③ 能说明碳的非金属性比硅强的实验现象是_________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ____ | ____ |
写出其中SO2显示还原性生成沉淀的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,把0.5molN2O4通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系己达平衡,此时容器内压强为开始时的1.6 倍。下列说法正确的是( )
A.前2s以N2O4的浓度变化表示的平均反应速率为0.01mol·L-1·s-1
B.在平衡时体系内N2O4的物质的量为0.25mol
C.在2s时体系内的压强为开始时的1.1倍
D.平衡时,N2O4的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A为电源,B为浸透饱和食盐水和酚酞的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1 ,断开K2 ,通电后,d端显红色,则电源a端为______极,若c、d为惰性电极,c端的电极反应是____________________________________
检验c端产物的方法_______________________________________________
高锰酸钾液滴现象__________________________________________________
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3 ,且均为0.1 mol,断开K1,闭合K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+ 氧化能力由大到小的顺序是_______;

(3)D装置中反应的方程式 ___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诺贝尔化学奖获得者GeorgeA.Olah提出了“甲醇经济”的概念,他建议使用甲醇来代替目前广泛使用的化石燃料用作能源储存材料和燃料。
工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206.0kJ·mol-1
CO(g)+3H2(g) ΔH=+206.0kJ·mol-1
(ii)合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.67kJ·mol-1
CH3OH(g) ΔH=-90.67kJ·mol-1
(1)制备合成气:工业生产中为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生的反应(iii):CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH=+41.17kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为_____。
CO(g)+H2O(g) ΔH=+41.17kJ·mol-1,为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为_____。
(2)为节约化石能源、减少碳排放,用CO2代替CO作为制备甲醇的碳源正成为当前研究的焦点。
①请写出二氧化碳加氢合成甲醇的热化学方程式_____。
②研究表明在二氧化碳合成甲醇的原料气中加入一氧化碳可以降低CO2与H2反应的活化能。在200-360℃,9MPa时合成气初始组成H2、CO、CO2物质的量之比7:2:1的条件下研究甲醇的合成反应。如图所示,CO2的平衡转化率随温度升高先减小后增大,分析可能的原因是____。

(3)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:CH3OH(g)+CO(g)![]() HCOOCH3(g) ΔH=+29.1kJ·mol-1
HCOOCH3(g) ΔH=+29.1kJ·mol-1
科研人员对该反应进行了研究,部分研究结果如下:

根据图,分析工业上制取甲酸甲酯时,选择的合适条件为_____。
(4)某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料,该电池工作原理见图。该反应负极电极反应式为_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g);ΔH<0。有下列判断,其中正确的是( )
pC(g)+qD(g);ΔH<0。有下列判断,其中正确的是( )
A.若温度不变,将容器的体积增大为原来的两倍,此时A物质的浓度变为原来的0.48倍,则m+n>p+q
B.若平衡时A、B的转化率相等,说明反应开始时A、B的物的量之比为n:m
C.若温度不变而压强增大为原来的两倍,则达到新的平衡时平衡混合物的体积小于原体积的![]()
D.若平衡体系共有amol气体,再向其中加入bmolB,当达到新平衡时共有(a+b)mol气体,则m+n=p+q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com