
����Ŀ��[��ѧ��ѡ���л���ѧ����]
������F�Ǻϳɿ�����ʧ��ҩ��������ص��м������Ա�Ϊԭ�Ϻϳ�F��·������:

��֪����CH3CH=CH2![]() CH3CHBrCH3 ��CH3CH=CH2
CH3CHBrCH3 ��CH3CH=CH2![]() CH3CH2CH2Br
CH3CH2CH2Br
�Իش���������
��1������Aת���ķ�Ӧ������ ��
��2��������C��Dת���ķ�Ӧ����ͨ���� ��������D ������ڡ����������ڡ���˳���칹����֪������C�ĺ˴Ź���������ʾ�����ַ壬�ҷ�������Ϊ2�U2�U1�U3����C�Ľṹ��ʽΪ ��
��3��д��E��Fת���Ļ�ѧ����ʽ ��
��4������B��ͬ���칹���ж��֣���������������ͬ���칹�干�� �֡�
�����ڷ����廯����
�ڷ��ӽṹ��û�м������а���
���ܷ���������Ӧ��ˮ�ⷴӦ��������NaOH��Ӧ�����ʵ���֮��Ϊ1�U2
��5������ͪ�� ���������л���ѧ�ϳɵ��м��壬���������ϳ�F�IJ��ֲ��裬���һ���Ա�Ϊ��ʼԭ���Ʊ�����ͪ�ĺϳ�·�� ��
���������л���ѧ�ϳɵ��м��壬���������ϳ�F�IJ��ֲ��裬���һ���Ա�Ϊ��ʼԭ���Ʊ�����ͪ�ĺϳ�·�� ��
���𰸡���1��ȡ����Ӧ
��2��NaOH����Һ������ ������ ![]()
��3��![]() ��CH3NH2
��CH3NH2![]() ��HBr
��HBr
��4��3
��5��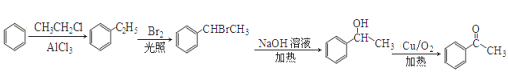
��������
�����������1������һ�����鷴Ӧ���ڱ����������һ���˵��Ϊȡ����Ӧ��
��2��C��D��±��������ȥ��Ӧ������ΪNaOH����Һ�ͼ��ȣ�������D������ϩ����������˳���칹��C�ĺ˴Ź���������ʾ�����ַ壬��˵����������ԭ�ӣ���ṹΪ![]() ��
��
��3��E��F�Ƿ�����ȡ����Ӧ������ʽΪ
![]() ��CH3NH2
��CH3NH2![]() ��HBr��
��HBr��
��4��������B��ͬ���칹��������Ҫ����ܷ���������Ӧ��ˮ�ⷴӦ��˵�����м������������������Ʒ�Ӧ�����ʵ�����Ϊ1:2������ˮ���������ǻ���˵���ṹ������������ ���ֱ�Ϊ-CH2NH2��-OOCH�����������ڱ����Ͽ������ڼ������λ�ù�ϵ��������3�ֽṹ��
��5�������Ʒ���������Ҫ�����ʻ�����Ҫ�ȳ����ǻ�������������Ӧ���ɣ����ǻ��ij�������±����ˮ�����ɵģ���±��������������±���ڹ��������·���ȡ����Ӧ�õ��ģ��������ڱ����������һ��������ұ������ڹ���������ȡ���м�̼ԭ���ϵ���ԭ�����ɴ������������ɣ��������£�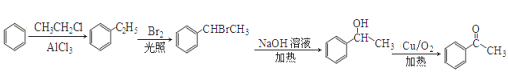 ��
��


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ�������Ϊ2 L���ܱ������У���̬����A��B��E��F�����ʵ���n��ʱ��t�ı仯�����ͼ����ʾ����һ�������·�Ӧ�ﵽƽ��״̬����Ӧ����������Ӧ������ʱ��ı仯�����ͼ����ʾ����t2��t4ʱ�̷ֱ�ֻ�ı�һ������(�¶ȡ�ѹǿ��ij��Ӧ�����)������˵���������( )

A. ���¶��£��÷�Ӧ�Ļ�ѧ����ʽΪ2A(g)+E(g)![]() 2B(g)+F(g)
2B(g)+F(g)
B. ��ƽ��״̬�ٺ͢ڶ�Ӧ���¶���ͬ����ٺ͢ڶ�Ӧ��ƽ�ⳣ��Kһ����ͬ
C. t2ʱ�̸ı������������ѹǿ
D. t4ʱ�̸ı�������ǽ����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�顣
I���� NaOH��Һ�� NH4Cl ��Һ������� NH3��H2O���Ӷ���֤NaOH�ļ��Դ���NH3��H2O���̶�������֤Na�Ľ����Դ���N������Ϊ������Ƿ����?��˵�����ɣ�_________��
II��������ͼ��ʾװ��ͼ�ش��������⡣
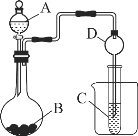
��1��ʵ����������ҩƷNa2S��KMnO4��Ũ���ᣬijͬѧ��֤�ȵķǽ����Դ�������д���Թ��з������ӷ�Ӧ����ʽ______
��2����ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮���ϵ���������ͼװ����һ�������N��C��Si���ַǽ���Ԫ�صķǽ�����ǿ���Ƚϵ�ʵ���о���д��ѡ�����ʵ����ƣ�A__��B__��C___��������Ӧ�����ӷ���ʽ_____��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����д��������������������ͼ�е�װ�ý���ʵ�顣

��Ҫʵ�鲽�����£�
�ٰ�ͼ��װ�����������װ�õ�������
�ڽ�ag����������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ
�۳���ʢ�м�ʯ�ҵ�U�ܵ��������õ�bg
�ܴӷ�Һ©������6mol/L�����ᣬֱ�����ٲ�������ʱΪֹ
�ݴӵ���A����������һ�����Ŀ���
���ٴγ���ʢ�м�ʯ�ҵ�U�ܵ��������õ�cg
���ظ�����ݺ͢IJ�����ֱ��U�ܵ������������䣬Ϊdg
�������������:
(1)װ���и����B��������____________��
(2)�������Ũ©���е����ỻ��Ũ����ͬ�����ᣬ���ԵĽ��______(��ƫ�ߡ�ƫ�ͻ�)��
(3)����ݵ�Ŀ����______________��
(4)����ߵ�Ŀ����___________________��
(5)�������д�������������ļ���ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����48g̼����ȫȼ�����������У�CO��CO2��ռ![]() �������C��s��+
�������C��s��+![]() O2��g���TCO��g����H=��110.5kJmol��1��CO��g��+
O2��g���TCO��g����H=��110.5kJmol��1��CO��g��+![]() O2��g���TCO2��g����H=��283kJmol��1������Щ̼��ȫȼ����ȣ���ʧ��������
O2��g���TCO2��g����H=��283kJmol��1������Щ̼��ȫȼ����ȣ���ʧ��������
A. 172.5 kJB. 1 149 kJC. 283 kJD. 566 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������������ȷ���ǣ� ��
A. ��֪������12�ĽṹʽΪ![]() ���÷�����ƽ���η���
���÷�����ƽ���η���
B. 1molƻ����[HOOCCH(OH)CH2COOH]����3molNaHCO3������Ӧ
C. �üױ��ֱ���ȡTNT������ױ����漰�ķ�Ӧ��Ϊȡ����Ӧ
D. ![]() ��һ�ȴ��ﹲ��5��(�����������칹)
��һ�ȴ��ﹲ��5��(�����������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л�������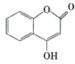 �������Ʊ�����Ѫҩ��ͨ������·�ߺϳɣ�
�������Ʊ�����Ѫҩ��ͨ������·�ߺϳɣ�

��1��B��C�ķ�Ӧ������__________��
��2��д��F����Na0H��Һ����ʱ��Ӧ�Ļ�ѧ����ʽ__________��
��3�����й���G��˵����ȷ����__________������ĸ����
a.�����嵥�ʷ�Ӧ b.��������Ʒ�Ӧ
c.1molG����ܺ�3mol������Ӧ d.����ʽ��C9H6O3
��4��E��ͬ���칹��ܶ࣬��E��������������Ĺ�__________�֡�
a.�������������Ȼ�����Һ��ɫ�� b.������������ȡ������ c.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������գ�
��1����Fe(NO3)3��Һ�м���Na2SO3��Һ,��Һ�����ػ�ɫ��Ϊdz��ɫ����һ���ֱ�Ϊ�ػ�ɫ����Һ�ȱ�Ϊdz��ɫ��ԭ����_________________�������ֱ�����ֱ�Ϊ�ػ�ɫ�����ӷ���ʽ��_____________________��
��2�������꿪���ļ״�ȼ�ϵ�ز��ò����缫����������е����ӽ���Ĥֻ�������Ӻ�ˮ����ͨ�����乤��ԭ����ʾ��ͼ���£�

Pt(a)�缫�ǵ�ص�________�����缫��ӦʽΪ________________________��Pt(b)�缫����________��Ӧ(���������ԭ��)���缫��ӦʽΪ_________________________
��3����֪Ǧ���صĹ���ԭ��ΪPb��PbO2��2H2SO4![]() 2PbSO4��2H2O��������ͼװ�ý��е��(���Һ����)����õ�Ǧ������ת��0.4 mol����ʱ���缫����������11.2 g����ش��������⡣
2PbSO4��2H2O��������ͼװ�ý��е��(���Һ����)����õ�Ǧ������ת��0.4 mol����ʱ���缫����������11.2 g����ش��������⡣

��A��Ǧ���ص�________����Ǧ����������ӦʽΪ_____________________��
��Ag�缫�ĵ缫��Ӧʽ��__________________________��
��Cu�缫�ĵ缫��Ӧʽ��________________________________��
CuSO4��Һ��Ũ��________(���С���������䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ���Σ���A��B��C��D��E���ֶ�����Ԫ��Ԫ����ɡ�������ˮ��ɵ�����������ӣ����к�����A��B�γɵ�10���������ӡ�AԪ��ԭ�Ӻ�����������E����1��D��E����ͬ���塣�ü�������ʵ�飺
��ȡ�����ľ�����������ˮ�����Һ��
��ȡ��������Һ���Թ��У������м���ϡ���ᣬ�ټ���BaCl2��Һ�����ְ�ɫ������
��ȡ��������Һ���Թ�����ε���NaOH��Һ�����ɳ��������������NaOH��Һ�������ϵ����ͼ��ʾ��

��ȡ��������Һ���Թ��У���������NaOH��Һ�����ȡ�
�ش��������⣺
��1��C��Ԫ�ط�����_______��D�����ڱ��е�λ����________��
��2�����ⶨ�����Ħ������Ϊ453 gmol-1�����������Ӻ����������ʵ���֮��Ϊ1:1�������Ļ�ѧʽΪ________��
��3��ʵ����и���ͼ���V(oa):V(ab):V(bc)= _______��
��4��ʵ��������ӷ���ʽ��___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com