
����Ŀ����ŵ�����һ���������ʪ�Թؽ���ҩ���ͨ�����·����ϳɣ�

��ش��������⣺
��1����ŵ����еĺ���������Ϊ________________�������ƣ���
��2����Ӧ���м�����Լ�X�ķ���ʽΪC8H8O2��X�Ľṹ��ʽΪ______________��
��3���������岽��Ӧ�У�����ȡ����Ӧ����_______________������ţ���
��4��B��һ��ͬ���칹����������������
���ܷ���������Ӧ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��
��������6�ֲ�ͬ��ѧ�������⣬�ҷ����к�������������
д����ͬ���칹��Ľṹ��ʽ��_______________��
��5����������֪ʶ����������Ϣ��д���� Ϊԭ���Ʊ�
Ϊԭ���Ʊ� �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
![]()
�ϳ�·������ͼ��һ���Ѹ������벹��������
 _________________________________________��
_________________________________________��
���𰸡� �Ѽ����Ȼ�  �٢ۢ�
�٢ۢ� 

���������ɺϳ�����ͼ��֪��A����ȡ����Ӧ����B��Ȼ�����η�����ԭ��Ӧ��ȡ����Ӧ��ȡ����Ӧ��ˮ�ⷴӦ���ɷ�ŵ��ҡ���
��1���ɽṹ��ʽ��֪��ŵ����еĹ�����Ϊ�Ѽ��� �Ȼ�����2��A����ȡ����Ӧ����B������AB����ʽ�IJ��첢���X�ķ���ʽ֪����B���Ѽ����ϼ���ʹ�ѻ�ת��Ϊ���ǻ�������X�ϣ�����X�Ľṹ��ʽΪ ����3����Ϊȡ����Ӧ����Ϊ�ӳɷ�Ӧ����Ϊȡ����Ӧ����Ϊȡ����Ӧ����Ϊˮ�ⷴӦ��ʵ�����ȼӳɺ�ȡ��������ȡ����Ӧ���Т٢ۢ�����4�� �ܷ���������Ӧ��˵������ȩ������ˮ�����֮һ�����Ȼ���������ɫ��Ӧ��˵�����з��ǻ�����������6�ֲ�ͬ��ѧ�������⣬�ҷ����к�������������˵���÷����к���������������ԭ��������6������������Ľṹ��ʽΪ
����3����Ϊȡ����Ӧ����Ϊ�ӳɷ�Ӧ����Ϊȡ����Ӧ����Ϊȡ����Ӧ����Ϊˮ�ⷴӦ��ʵ�����ȼӳɺ�ȡ��������ȡ����Ӧ���Т٢ۢ�����4�� �ܷ���������Ӧ��˵������ȩ������ˮ�����֮һ�����Ȼ���������ɫ��Ӧ��˵�����з��ǻ�����������6�ֲ�ͬ��ѧ�������⣬�ҷ����к�������������˵���÷����к���������������ԭ��������6������������Ľṹ��ʽΪ ����5������ȩ��NaBH4������ԭ��Ӧ���ɱ��Ҵ������Ҵ�������ȥ��Ӧ���ɱ���ϩ������ϩ�����ӳɷ�Ӧ����
����5������ȩ��NaBH4������ԭ��Ӧ���ɱ��Ҵ������Ҵ�������ȥ��Ӧ���ɱ���ϩ������ϩ�����ӳɷ�Ӧ����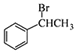 ��
�� ��NaCN����ˮ�ⷴӦ����
��NaCN����ˮ�ⷴӦ���� �����ϳ�·��ͼΪ
�����ϳ�·��ͼΪ ��
��


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��������߷��ӻ��������
A. ���� B. ���� C. ��֬ D. ��ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʯīϩ�-������һ�ָ���������ѭ���������ͳɱ��������Ѻõ����Ͷ��ε�أ��õ�ؽṹ��ͼ��ʾ����ط�ӦΪ2Li +nS![]() Li2Sn���йظõ�ص�˵����ȷ����
Li2Sn���йظõ�ص�˵����ȷ����

A. �ŵ�ʱ��Li+��Ǩ��
B. ���ʱ��A�缫���ӵ�Դ�ĸ���
C. ���ʱ��ÿ����n mol Sת��2n mol����
D. �ŵ�ʱ�������Ͽɷ�����Ӧ2Li+ +2Li2S6+2e-=3Li2S4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����Fe��Fe2O3��������2mol��L��1��HNO3��Һ25 mL�У���Ӧ��ɺ�����ʣ�࣬����224 mL NO����(��״��)������Ӧ�����Һ�м���1 mol��L��1��NaOH��Һ��Ҫʹ��Ԫ��ȫ����������������NaOH��Һ�����������( )
A��45 mL B��50 mL C��40 mL D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ���ů��ʹ�ö���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Եø��ӽ��ȡ������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯��������ʡ�
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼������(����)�����ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��
___ C+ ___ KMnO4+ ____ H2SO4��____CO2��+ ____MnSO4+ ____K2SO4+ ____H2O
��2����̿��������ȡˮú�������12 g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131.6 kJ�������÷�Ӧ���Ȼ�ѧ����ʽΪ______________________________________________________��
��3����ҵ���ں����ܱ������������з�Ӧ�ϳɼ״���
CO(g)��2H2(g)![]() CH3OH(g) ��H��akJ/mol ��
CH3OH(g) ��H��akJ/mol ��
�±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
���жϷ�Ӧ�ﵽƽ��״̬��������_____________��
A������CH3OH������������CO���������
B����������ƽ����Է�����������
C�����������ܶȲ���
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��ij�¶��£���2 mol CO��һ������H2����2 L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c![]() mol��L������H2��ʾ�ķ�Ӧ����v(H2)=___________��
mol��L������H2��ʾ�ķ�Ӧ����v(H2)=___________��
��4��CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2��
�����Ϊ������ȼ�����Ƶ���650 ���¹�����ȼ�ϵ�أ���������Ӧʽ:
O2+ 2CO2+4e����2CO32������������Ӧʽ:______________________________________��
��5����BaSO4�����м��뱥��̼������Һ����ֽ��裬��ȥ�ϲ���Һ����˴�����Σ���ʹBaSO4ȫ��ת��ΪBaCO3��������Ӧ��BaSO4(s)+CO32��(aq) ![]() BaCO3(s)+SO42��(aq)����֪ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=4.0��10��2��BaSO4��Ksp=1.0��10��10���� BaCO3���ܶȻ�Ksp=___________��
BaCO3(s)+SO42��(aq)����֪ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=4.0��10��2��BaSO4��Ksp=1.0��10��10���� BaCO3���ܶȻ�Ksp=___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֱ�����ص�صĽṹ��ͼ��ʾ������˵������ȷ����

A. ̼�缫���ö�ײ��ô�ý��ɼӿ췴Ӧ����
B. ��ع���ʱ����ѧ��ת��Ϊ����
C. Y���ĵ缫��ӦʽΪH2NCONH2+H2O-6e-=N2��+CO2+6H+
D. ��ع���ʱ��H+��Y����Ǩ�ƣ�Y����Χ��Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͭ�ۻ������Ʒ11.6 g����μ���2.0 mol��L��1��������Һ����ַ�Ӧ��ʣ��������������������Һ����仯���±���
������Һ/mL | 20.0 | 40.0 | 60.0 | 80.0 |
ʣ�����/g | 9.36 | 7.12 | 4.88 | 3.20 |
��ش���
(1)��Ʒ������ͭ�����ʵ���֮��n(Fe)��n(Cu)��________��
(2)�ڷ�Ӧ�����ϵ�����ټ���4.0 mol��L��1��H2O2��Һ25.0 mL������������������Һ����ַ�Ӧ����Һ�д��ڵĸ��������ӵ����ʵ����ֱ��Ƕ�����__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С��ͬѧ�ڡ�������չ�Ķ�������˽���������ڳ�������ˮ���ҷ�Ӧ������һ�ֿ�ȼ�����塣��ʦ���С������֪ʶ�������ͼ��ʾװ�ý���ʵ�顣
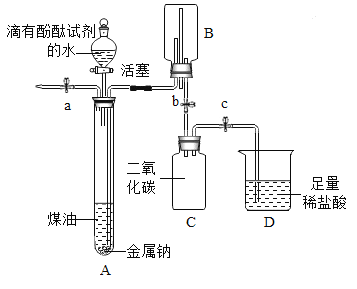
��С���ϡ�������һ������ú���л���ʯ����棬ú�͵��ܶ�Ϊ0.8g/mL��
��1�����⣺��ȡ������������Ƶķ����У�ú�ͻ�ʯ����������__________��
��2��ʵ�����
���� | ������ | |
�� | ��ֹˮ��a����Һ©����������Һ��������Թܺر�ֹˮ��a����Һ©�������� | Һ��ֲ㣬���۳�����ɫС����Һ��ֲ�Ľ����Ϸ������������������ݣ��²���Һ��ɺ�ɫ������ѹ��B�С��ɴ˿�֪�����Ƶ���������_______��д��һ�㼴�ɣ��� |
�� | ��ֹˮ��b����B�в�����Һ����C�У�Ѹ�ٹر�ֹˮ��b�� | ��Ӧ�Ļ�ѧ����ʽΪ_____________. |
�� | ��ֹˮ��c�� | _______����Һ��ɫ��ʧ�� ��Ӧ�Ļ�ѧ����ʽΪ_________�� |
�� | ��ȼ�ŵ�ľ���쵽���ܼ��촦����ֹˮ��a�� �ڻ����Ϸ���һ��������ձ��� | ����ȼ�գ���������ɫ���� �ձ��ڱ�����ɫҺ�����ɣ�A������Ϊ������ |
��3����˼����
��������ˮ��Ӧ�Ļ�ѧ����ʽΪ_____________��
��Ӧ������C����Һ��������_________��ָʾ�����⣬д�����п��ܣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����գ����������˶������Ѱ�����Ҫ�ɷְ����ҳ���SO2��NOx���л�̼�⻯��������ӡ��������������������ķ���֮һ��
(1)�����dz���������������֮һ��������ԭ������NO(g)��Ӧ���ɿ����д��ڵ����������ʡ�
��д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��_____________��
����֪��4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ��H1=-907.28kJ mol-1��
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)��H2= -1269.02kJ mol-1��105��ʱ��������������Ӧ�ġ�H=_______���÷�Ӧ________(��ܡ� ������ȷ�������Է����У�
������������Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ________��ÿ����1mol��ԭ�����Ӧ��ת�Ƶ�����Ϊ_________mol��
(2)����Ҳ��������������������������ķ�Ӧ֮һΪ2NO2(g)+O3(g)![]() N2O5(g)+O2(g)����ͬ�¶��£����������������з���������Ӧ�������Ϣ���±���ͼ��ʾ���ش���������:
N2O5(g)+O2(g)����ͬ�¶��£����������������з���������Ӧ�������Ϣ���±���ͼ��ʾ���ش���������:
���� | �� | �� |
�ݻ�/L | 1 | 1 |
�¶�/K | T1 | T2 |
��ʼ������ | lmolO3 2mol NO2 | lmolO3 2mol NO2 |

0~10min�ڼ������з�Ӧ��ƽ�����ʣ�v(O3) =_______mol��L-1��min-1 ��
��T1________T2 (�>����<����=������T1ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ____________��
�����д�ʩ�������������NO2ת���ʵ���________(����ţ���
A.�������г���He������������ѹǿ
B.�����������¶�
C.���������ٳ���һ������NO2
D.���������ٳ���lmol O3��2mo NO2
��T1ʱ������ʼʱ���������г���2mo1 NO2��lmolO3��2mollN2O5��2molO2����������Ӧ�ﵽƽ��ǰ��v(��)________v(��) (�>����<����=��)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com