
【题目】含碳化合物种类繁多。回答下列问题:
(1)一定温度下,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为_________%。
CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为_________%。
(2)在催化剂Ru催化下,CO2与H2反应可生成CH4,反应方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正______(填“增大”“减小”或“不变”,下同),v逆_______,平衡常数K________,转化率α________;若在相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正______(填“增大”“减小”或“不变”,下同),v逆_______,平衡常数K________,转化率α________;若在相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
c(CO2)/mol/L | c(H2)/mol/L | c(CH4)/mol/L | c(H2O)/mol/L | |
平衡I | a | b | c | d |
平衡II | m | n | x | y |
则a、b、c、d与m、n、x、y之间的关系式为_____________。
(3)已知相关物质的电离平衡常数如下表:

①0.1 mol·L-1的Na2CO3溶液的pH_______(填“大于”“小于”或“等于”)0.1 mol·L-1的Na2C2O4溶液的pH。
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中粒子浓度大小的顺序正确的是_________(填字母)。
a.c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-) b.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
c.c(H+)>c(HC2O4-)>c(CO32-)>c(C2O42-) d.c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
【答案】40 增大 增大 减小 减小 ![]() 大于 a
大于 a
【解析】
(1)假设反应开始时CO(g)和H2O(g)为1 mol,反应达到平衡时产生H2的物质的量为x,根据该温度下平衡常数K=16计算x的值,再计算H2的平衡含量;
(2)温度升高,化学反应速率加快;利用温度升高,H2的含量增大判断反应的热效应,再分析温度对平衡常数及物质平衡转化率的影响;平衡常数的定义式书写平衡常数,利用同一温度下的平衡常数相同计算;
(3)根据盐的水解规律分析、比较。
(1) 假设反应开始时CO(g)和H2O(g)为1 mol,反应达到平衡时产生H2的物质的量为x,根据反应CO(g)+H2O(g)![]() CO2(g)+H2(g)中物质转化关系可知平衡时n(CO)=n(H2O)=(1-x) mol,n(CO2)=n(H2)=x mol,该反应是反应前后气体体积相等的反应,所以根据平衡常数的含义可得K=
CO2(g)+H2(g)中物质转化关系可知平衡时n(CO)=n(H2O)=(1-x) mol,n(CO2)=n(H2)=x mol,该反应是反应前后气体体积相等的反应,所以根据平衡常数的含义可得K=![]() =16,解得x=0.8 mol,所以平衡时H2的体积分数为:
=16,解得x=0.8 mol,所以平衡时H2的体积分数为:![]() ×100%=40%;
×100%=40%;
(2)对于反应CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加,说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,所以该反应的正反应为放热反应。若温度从300℃升至400℃,温度升高化学反应速率加快,所以重新达到平衡时v正增大,v逆增大,平衡逆向移动,使平衡常数K减小,反应物的转化率α减小。若在相同温度时,上述反应在不同起始浓度下分别达到平衡,根据各物质的平衡浓度可知平衡I的化学平衡常数K1=
CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加,说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,所以该反应的正反应为放热反应。若温度从300℃升至400℃,温度升高化学反应速率加快,所以重新达到平衡时v正增大,v逆增大,平衡逆向移动,使平衡常数K减小,反应物的转化率α减小。若在相同温度时,上述反应在不同起始浓度下分别达到平衡,根据各物质的平衡浓度可知平衡I的化学平衡常数K1=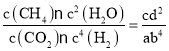 ,平衡II的化学平衡常数K2=
,平衡II的化学平衡常数K2=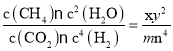 ,由于是该反应同一温度下的平衡常数,所以K1= K2,所以
,由于是该反应同一温度下的平衡常数,所以K1= K2,所以![]() ;
;
(3)①根据表格数据可知弱酸的电离平衡常数K2:H2C2O4>H2CO3,Na2CO3、Na2C2O4都是强碱弱酸盐,水解使溶液显碱性,由盐的水解规律:谁弱谁水解,谁强显谁性,越弱越水解,可知水解程度Na2CO3>Na2C2O4,所以两种溶液的pH:Na2CO3>Na2C2O4;
②碳酸H2CO3:Ka1=4.3×10-7,Ka2=5.6×10-11,草酸H2C2O4:Ka1=5.9×10-2,Ka2=6.4×10-5,酸性:H2C2O4>H2CO3,根据酸电离平衡常数越大,该酸电离产生的离子浓度越大,溶液中H+是两种酸电离产生,则H+浓度最大,由于酸电离分步进行,电离平衡常数减小,则该酸电离产生的离子浓度也逐渐减小,酸溶液中主要以酸分子存在,分子浓度大于电离产生的离子浓度,酸性强,则电离程度大,所以c(H2CO3)>c(H2C2O4),根据电离平衡常数的大小可以得到离子浓度大小顺序是:c(H+)>c(HC2O4-)>c(HCO3-)>c(C2O42-)>c(CO32-),故合理选项是a。


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】模拟“人工树叶”的电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是
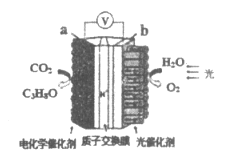
A.该装置将化学能转化为光能和电能
B.b电极上发生得e-的氧化反应
C.该装置工作时,H+从b极区向a极区迁移
D.a电极上反应:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法正确的是
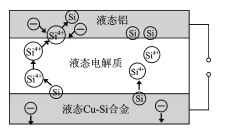
A.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
B.液态Cu-Si合金作阳极,固体硅作阴极
C.电流强度的大小不会影响硅提纯速率
D.三层液熔盐的作用是增大电解反应接触面积,提高硅沉积效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A. 光合作用 B. 自然降雨
C. 化石燃料的燃烧 D. 碳酸盐的沉积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中加入反应物N2、H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如表所示:
2NH3(g)。反应过程中的部分数据如表所示:

下列说法正确的是
A.0~2min内,H2的反应速率为0.1 mol/(L·min)
B.2min时,NH3的物质的量浓度为0.2 mol/L
C.4min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼是一种过渡金属元素,其单质通常用作合金及不锈钢的添加剂,这种金属可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。下图是化工生产中制备金属钼的主要流程:

(1)用简单氧化物形式表示![]() 的组成:____________________________。
的组成:____________________________。
(2)写出反应①的化学方程式:______________________。
(3)反应①的尾气可以再利用,写出两种利用该尾气制得的化学药品:______________________。
(4)工业上制备还原性气体的反应原理有: ,
, 。将含甲烷体积分数为80%的a L(标准状况下)天然气与足量二氧化碳和水蒸气混合物在高温下反应,甲烷的转化率为90%,用产生的还原性气体(
。将含甲烷体积分数为80%的a L(标准状况下)天然气与足量二氧化碳和水蒸气混合物在高温下反应,甲烷的转化率为90%,用产生的还原性气体(![]() 和
和![]() )依据反应⑤冶炼钼,理论上生成钼的质量为___________(已知
)依据反应⑤冶炼钼,理论上生成钼的质量为___________(已知![]() 的相对原子质量为96)
的相对原子质量为96)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰不仅是活性好的催化剂,也被广泛用作干电池的正极材料。某化学小组设计用高硫锰矿(主要成分为锰的化合物和硫化亚铁)为原料制取二氧化锰的工艺流程如图:
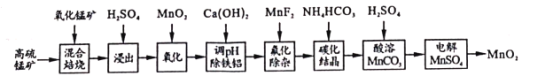
已知:①“混合焙烧”后的烧渣含MnSO4、Fe2O3及少量FeO、MgO、Al2O3
②在该条件下,金属离子开始沉淀和完全沉淀的pH如表:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀 | 1.8 | 6.8 | 4.0 | 7.5 |
完全沉淀 | 3.2 | 8.0 | 5.0 | 8.4 |
(1)写出浸出时与铝元素有关的离子反应方程式____。
(2)上述“氧化”步骤是否可省略____(填“是”或“否”),你的依据是 _____。
(3)“调pH除铁铝’’时,生成沉淀的pH范围为____;“氟化除杂”中除去的离子为____。
(4)请用平衡移动原理解释除杂处理后的Mn2+用NH4HCO3转化成MnCO3沉淀的过程___(用文字和离子方程式表达)。
(5)用惰性电极电解MnSO4制备MnO2时,其阳极反应式为____;整个流程中能够循环利用的物质除MnO2外还有___(写名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
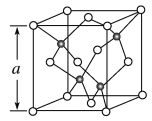
【题目】(1)Cu的一种氯化物晶胞结构如图所示(黑球表示铜原子,白球表示氯原子),该氯化物的化学式是__。若该晶体的密度为ρg·cm-3,以NA表示阿伏加德罗常数的值,则该晶胞的边长a=__nm。
(2)一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
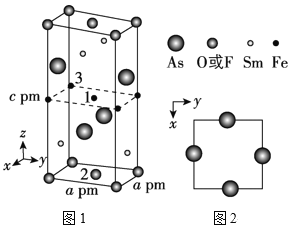
图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为__,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=__g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ,
,![]() ,
,![]() ),则原子2和3的坐标分别为__、__。
),则原子2和3的坐标分别为__、__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com