
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 足量MnO2与40 mL 10 mol·L-1的浓盐酸充分反应,生成的氯气分子数为0.1NA
B. 常温下,224 mL H2O中所含氢氧键的数目约为0.02NA
C. 0.1mol FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 NA
D. 常温下,1 L pH=11的Na2CO3溶液中由水电离出的H+数目为0.001NA
【答案】D
【解析】
A.二氧化锰只能与浓盐酸反应,和稀盐酸不反应,题给浓盐酸不能反应完全,则生成的氯气分子数小于0.1NA,故A错误;B.常温下,22.4 mL水的物质的量约为m/M=(22.4 mL![]() 1g/cm3)/18g
1g/cm3)/18g![]() mol-1=1.24mol,1个H2O分子中含有2个H—O键,则22.4 mL水中含H—O键的物质的量约为1.24mol×2≈2.49 mol,故B错误;C. FeCl3水解形成的Fe(OH)3胶体粒子是多个Fe(OH)3的聚集体,所以0.1mol FeCl3水解形成的Fe(OH)3胶体粒子数小于0.1 NA,故C错误;常温下,1 L pH=11的Na2CO3溶液中c(OH-)=0.001 mol·L-1,则由水电离出的H+数目为0.001NA,故D正确。答案:D。
mol-1=1.24mol,1个H2O分子中含有2个H—O键,则22.4 mL水中含H—O键的物质的量约为1.24mol×2≈2.49 mol,故B错误;C. FeCl3水解形成的Fe(OH)3胶体粒子是多个Fe(OH)3的聚集体,所以0.1mol FeCl3水解形成的Fe(OH)3胶体粒子数小于0.1 NA,故C错误;常温下,1 L pH=11的Na2CO3溶液中c(OH-)=0.001 mol·L-1,则由水电离出的H+数目为0.001NA,故D正确。答案:D。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中正确的是
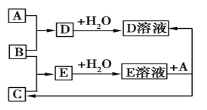
A. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B. A、B、C中有一种金属且为B
C. 如果E溶液是一种强酸,则E溶液为硫酸
D. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别一定不是碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示。其中温度为T1时平衡混合气体中氨气的体积分数为25.0%。
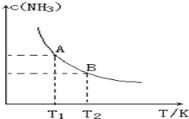
(1)当温度由T1变化到T2时,平衡常数关系K1___________K2(填“>”,“<”或“=”),焓变△H___________0(填“>”或“<”)。
(2)该反应在T1温度下5.0min达到平衡,这段时间内N2的化学反应速率为_________,N2的转化率___________。
(3)T1温度下该反应的化学平衡常数K1=______________。
(4)T1温度时,若测得高炉中c(N2)=0.5mol/L,c(H2)=0.5mol/L,c(NH3)=0.5mol/L,在这种情况下,该反应是否处于平衡状态___________(填是或否),此时反应速率是v正___________v逆(填>,<,=)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应判断有关物质还原性由强到弱的顺序是
①H2SO3+I2+H2O═H2SO4+2HI②2FeCl3+2HI═2FeCl2+2HCl+I2
A.H2SO3> HI>FeCl2B.HI >FeCl2>H2SO3
C.FeCl2>HI >H2SO3D.FeCl2>H2SO3>HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述中正确的是( )

A. 根据图甲可知合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g) △H1=(b-a)kJ·mol-1
B. 图乙表示2mol H2(g)所具有的能量比2mol气态水所具有的能量多483.6kJ
C. 1mol NaOH分别和1mol CH3COOH、1mol HNO3反应,后者比前者△H小
D. 汽油燃烧时将全部的化学能转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是

A. 该氨水的浓度为0.100 0 mol·L-1
B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-)
C. 点②溶液中c(NH4+)=c(Cl-)
D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.5 molL -1 盐酸与50 mL0.55 mol L -1 NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是______________________。

(2)烧杯间填满碎纸条的作用是______________________________________。
(3)若大烧杯上不盖硬纸板,求得中和热数值_______(填“偏大”“偏小”或“无影响”)。
(4)实验中改用60 mL 0.50 molL -1 盐酸跟50 mL 0.55 molL -1 NaOH溶液进行反应,与上述实验相比,所放出的热量 _______(填“相等”或“不相等”),所求中和热 _____(填“相等”或“不相等”),简述理由_______________________________。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会_________;用0.50 molL -1 NaOH溶液50 mL进行上述实验,测得的中和热的数值会__________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中:xA(g)+yB(g) ![]() zC(g) △H<0,达到平衡后A气浓度为0.5mol/L;恒温下将密闭容器的容积扩大到原来的两倍并再达平衡,测A浓度为0.3 mol/L。下列叙述正确的是( )
zC(g) △H<0,达到平衡后A气浓度为0.5mol/L;恒温下将密闭容器的容积扩大到原来的两倍并再达平衡,测A浓度为0.3 mol/L。下列叙述正确的是( )
A. 平衡向右移动 B. x+y>z C. B的转化率提高 D. C的体积分数增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com