
����Ŀ���������������ǵĽ���ϢϢ��أ�Ŀǰ�ҹ�ͨ�����6����Ⱦ�������Ũ���������������ָ����AQI����SO2��NO2��CO������3���е���Ⱦ�
��1��һ���¶��£���̶����Ϊ2L���ܱ������г���SO2��NO2��1mol��������ӦSO2��g��+NO2��g��SO3��g��+NO��g�������������Ӧ5minĩ����ƽ�⣬��ʱ������NO��NO2�������Ϊ3��1�������ʱ����SO2�ķ�Ӧ���ʦԣ�SO2��= �� �˷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K= ��
��2���״�������Ϊ��Ҫ���л�ȼ�ϣ�ͨ������CO��H2�ϳɼ״����䷴Ӧ�Ļ�ѧ����ʽΪCO��g��+2H2��g��CH3OH��g��������һ�ݻ��ɱ���ܱ������У�����10mol CO��20mol H2���ںϳɼ״���CO��ƽ��ת���ʣ��������¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ��ʾ��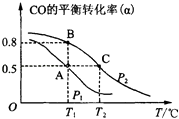
�������ϳɼ״��ķ�ӦΪ��Ӧ������ȡ������ȡ�����
��A��B��C�����ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ �� A��B�����Ӧ��ѹǿ��С��ϵ��PAPB������ڡ�����С�ڡ����ڡ�����
�������ﵽƽ��״̬Aʱ���ɵļ״����ڹ��ɼ״�һ����ȼ�ϵ�أ��������ҺΪKOHŨ��Һ����õ�ع���ʱ�����ĵ缫��ӦʽΪ �� ������ͨ�����·�ĵ������Ϊ mol��
���𰸡�
��1��0.075mol/��L?min����9
��2��KA=KB��KC��KA=KB��KC��С�ڣ�O2+2H2O+4e��=4OH����30
���������⣨1����μӷ�Ӧ��SO2Ϊnmol
SO2��g�� | + | NO2��g�� | = | SO3��g�� | + | NO��g�� | |
��Ӧǰ��mol�� | 1 | 1 | 0 | 0 | |||
��Ӧ�ˣ�mol�� | n | n | n | n | |||
5minĩ��mol�� | 1��n | 1��n | n | n |
![]() =
= ![]() ����ã�n=
����ã�n= ![]() =0.75
=0.75
�ԣ�SO2��= ![]() =0.075mol/��Lmin��
=0.075mol/��Lmin��
���������2L��������Ե�Ũ�ȴ������K
K= ![]() =9
=9
���Դ��ǣ�0.075mol/��Lmin����9��
��2.���ٴ�ͼ�Ͽɼ�����P2ʱ�����¶ȵ�����CO��ת����Խ��Խ�ͣ��ɼ�������ʱƽ���������ƶ�������������ԭ��������Ӧ���ȣ�
���Դ��ǣ����ȣ�
�ڻ�ѧƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬�÷�Ӧ���ȣ��¶�Խ��ƽ�������ƶ���Kֵ��С������ѹǿ��ƽ�������ƶ���CO��ת��������֪PA С��PB ��
���Դ��ǣ�KA=KB��KC��С�ڣ�
��ȼ�ϵ�ص���������������Ӧ���ڼ�����������ˮ����������������
O2+2H2O+4e��=4OH��
A��CO��ƽ��ת����50%���μӷ�Ӧ��COΪ��10mol��50%=5mol
��CO��g��+2H2��g��=CH3OH��g������������CH3OHҲΪ5mol��CH3OHȼ�����ɶ�����̼��ˮ��ֻ��C�ļ�̬�ө�2��Ϊ+4��H��O��̬û�䣬����1molCH3OHȼ��ת��6mol���ӣ���5molCH3OH��Ӧת�Ƶ���Ϊ��5��6=30��
���Դ��ǣ�O2+2H2O+4e��=4 OH����30��
�����㾫����������Ĺؼ��������⻯ѧƽ��״̬���ʼ����������֪ʶ�����ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�����Լ��Ի�ѧƽ��ļ�������⣬�˽ⷴӦ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.���ǡ����ۡ���֬����ˮ������Ϊ�ǵ����
B.�����������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH
C.������Cu(OH)2����Һ���Լ������ᡢ�Ҵ���������
D.�������ΪCH4��C2H6O���л��ﲻ����ͬ���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����W��X��Y��Z���ֽ���������װ�ý���ʵ�飮����˵������ȷ���ǣ� ��
װ�� |
|
|
|
���� | ����W�����ܽ� | Y���������� | W�������巢�� |
A.װ�ü���W��ԭ��ظ���
B.װ������Y�缫�ϵķ�ӦʽΪCu2++2e��=Cu
C.װ�ñ�����Һ��pH��С
D.���ֽ����Ļ��ǿ��˳��ΪZ��W��X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�У�ԭ����(N2��H2��CO��NH3�Ļ����)�ڽ���ϳ���ǰ���ô��������ͭ(l)��Һ������ԭ���е�CO���䷴Ӧ��
[Cu(NH3)2Ac]��CO��NH3![]() [Cu(NH3)3]Ac��CO��Q
[Cu(NH3)3]Ac��CO��Q
��1�������ȥԭ������CO��ԭ����?
��2�����������ͭ(l)����CO��������������
��3������CO��Ĵ���ͭ��Һ�����ʵ������ֿ��������ָ�������CO��������ѭ��ʹ�ã�����ͭ��Һ������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶��£����ʵ���Ũ����ͬ��������Һ��pH������
A��NaCl B��CH3COONa C��Na2CO3 D��NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������г��������֮һ�������뻷���ĺ�г��չ��������ɫ��ѧ����������ָ�Ӽ�����������ƿ��еĻ�ѧ��Ӧ�������ܼ��ٶԻ����ĸ����ã����л�ѧ��Ӧ�����ϡ���ɫ��ѧ���������( )
A.�������᳧β���е�SO2��SO2��2NH3��H2O===(NH4)2SO3
B.�������Ṥҵβ���ĵ����������Ⱦ��NO��NO2��2NaOH===2NaNO2��H2O
C.��CuSO4��Cu��2H2SO4(Ũ) ![]() CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
D.��CuSO4��2Cu��O2��2H2SO4 ![]() 2CuSO4��2H2O
2CuSO4��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ת���ķ�Ӧ����ʽ�У���ȷ���ǣ� ��
A.H2SO3��H2SO4��2H2SO3+O2=2H2SO4
B.Fe��Fe3+��2Fe+6H+=2Fe3++3H2��
C.Br����Br2��2Br��+I2=Br2+2I��
D.Cu��CuSO4��Cu+2H2SO4��ϡ��=CuSO4+SO2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ӧ���У�����Ӽ��������йص���( )
A. �Ȼ��ƾ�������ˮB. ����ؾ�����ڻ�����ȴ
C. ����������ɱ������D. ������·��ˮ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com