
【题目】硫氰化钾(KSCN)是中学实验室的常见药品,某校化学兴趣小组在实验室制备少量样品,并进行探究实验。他们查有关资料:CS2+2NH3![]() NH4SCN+H2S,该反应比较缓慢。
NH4SCN+H2S,该反应比较缓慢。
Ⅰ.制备KSCN样品。
(1)先制备NH4SCN溶液,装置如图:
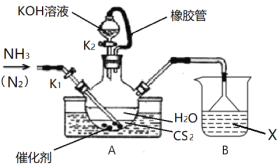
①实验开始时打开K1,关闭K2,加热水浴装置,缓缓地向三颈烧瓶中持续通入NH3,并持续通入N2,通入N2的作用是:____________。
②一段时间后,当CS2反应完毕,停止实验,此时可以观察到三颈烧瓶内的现象是:______。
③烧杯内的溶液X是______________。
(2)再制备KSCN溶液:关闭K1,打开K2,利用耐碱分液漏斗缓慢加入适量KOH溶液,继续加热,此时三颈烧瓶中发生反应的化学方程式是____________________。
(3)样品检测:待冷却后,用胶头滴管吸取少量样品滴入试管中的FeCl3溶液中,并没有观察到明显变红的现象,请分析可能的原因:_____________。
Ⅱ.KSCN的探究实验,同学们用实验室配制的KSCN溶液做下列实验(不是刚才兴趣小组合成的)。
(4)同学甲想检测Fe3O4中是否有三价铁,他把在充满氧气的集气瓶中燃烧后的铁丝残渣放入试管,加适量盐酸使其溶解,再往混合液中滴入少量KSCN溶液检验是否有Fe3+,结果没变红,请分析原因:_________________。
(5)同学乙想利用反应Fe3++3SCN-Fe(SCN)3来研究浓度对化学平衡的影响。他往盛有5 mL 0.05 mol/L FeCl3溶液的试管中加入5 mL_____ mol/L KSCN溶液,再把反应后的溶液均分置于两只试管中,分别加4滴浓FeCl3溶液和4滴浓KSCN溶液,观察现象并得出有关结论。
(6)同学丙往FeCl2和KSCN的混合溶液中滴加氯水,溶液变成红色,不过他注意到,当氯水过量时,红色会褪去,为此,他设计如图装置进行探究。
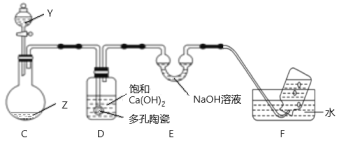
Y为NaClO溶液,Z为FeCl3和KSCN的混合溶液。打开分液漏斗,持续缓慢滴入NaClO溶液至过量,他观察到:C中红色变浅,有大量气泡产生,C中还有现象为:___________________;D中的现象为:_______________,F中有气泡。由此推测,KSCN具有______________性。
【答案】搅拌作用;或者稀释氨气,使接触更加充分,转化率高 溶液不再分层 NaOH或者CuSO4、CuCl2或者KMnO4等 NH4SCN + KOH![]() KSCN + H2O + NH3↑ 原样品中KOH过量,会和FeCl3溶液生成Fe(OH)3沉淀 铁除了生成Fe3O4,还有Fe过量,会把Fe3+还原为Fe2+ 0.15 有红褐色沉淀生成 澄清石灰水变浑浊 还原性
KSCN + H2O + NH3↑ 原样品中KOH过量,会和FeCl3溶液生成Fe(OH)3沉淀 铁除了生成Fe3O4,还有Fe过量,会把Fe3+还原为Fe2+ 0.15 有红褐色沉淀生成 澄清石灰水变浑浊 还原性
【解析】
(I)在三颈烧瓶中NH3与CS2混合加热发生反应:CS2+2NH3![]() NH4SCN+H2S,为使反应物充分接触发生反应,同时避免发生副反应,可不断通入N2,根据CS2是液态有机溶剂,不溶于水,反应产物易溶于水的性质,当液体不再分层时,可判断反应完全,然后通过分液漏斗向三颈烧瓶中滴加KOH溶液,发生反应制取KSCN,反应产生的H2S是有毒气体,可根据H2S是酸性气体、具有强的还原性,金属硫化物的难溶性分析判断试剂X可能的物质;根据Fe3+遇KSCN溶液变为血红色检验,检验时要注意杂质离子的干扰;
NH4SCN+H2S,为使反应物充分接触发生反应,同时避免发生副反应,可不断通入N2,根据CS2是液态有机溶剂,不溶于水,反应产物易溶于水的性质,当液体不再分层时,可判断反应完全,然后通过分液漏斗向三颈烧瓶中滴加KOH溶液,发生反应制取KSCN,反应产生的H2S是有毒气体,可根据H2S是酸性气体、具有强的还原性,金属硫化物的难溶性分析判断试剂X可能的物质;根据Fe3+遇KSCN溶液变为血红色检验,检验时要注意杂质离子的干扰;
(II)(4)铁丝残渣中含有Fe3O4,可能含有Fe,根据它们与酸可能反应产生的物质成分判断溶液中离子的存在;
(5)要证明平衡移动,需使溶液中的Fe3+、SCN-完全反应,然后改变某种离子浓度,根据溶液颜色变化分析判断;
(6)NaClO是强碱弱酸盐,水解使溶液显碱性,Fe3+与OH-反应会产生Fe(OH)3沉淀,同时NaClO具有强氧化性,会将SCN-氧化产生SO42-、CO2、N2等物质,据此分析解答。
(1)①向盛有CS2、H2O混合物的三颈烧瓶中缓缓持续通入NH3,并水浴加热发生反应:CS2+2NH3![]() NH4SCN+H2S,为了使反应物充分接触,提高转化率,要持续通入N2;
NH4SCN+H2S,为了使反应物充分接触,提高转化率,要持续通入N2;
②CS2是有机溶剂,与水互不相溶,当反应一段时间后,若CS2反应完毕,由于反应产生的物质都易溶解在水中,此时可以观察到三颈烧瓶内的现象是溶液不再分层,此时停止实验;
③发生反应产生的H2S是有毒气体,会造成环境污染,可根据H2S水溶液显酸性,用NaOH等碱性溶液吸收;也可以利用H2S与CuSO4或CuCl2会产生CuS沉淀吸收除去;还可以利用其强的还原性,用具有强氧化性的物质如酸性KMnO4溶液等将其氧化除去,故烧杯内的溶液X是NaOH或CuSO4、CuCl2或者KMnO4等物质;
(2)将KOH溶液与NH4SCN溶液混合加热,发生反应:NH4SCN + KOH![]() KSCN + H2O + NH3↑,得到KSCN溶液;
KSCN + H2O + NH3↑,得到KSCN溶液;
(3)待冷却后,用胶头滴管吸取少量样品滴入试管中的FeCl3溶液中,并没有观察到明显变红的现象,可能是原样品中加入的KOH过量,与FeCl3溶液发生复分解反应生成Fe(OH)3红褐色沉淀,导致未发生3KSCN+ FeCl3![]() Fe(SCN)3+3KCl,因此不能观察到溶液变为红色;
Fe(SCN)3+3KCl,因此不能观察到溶液变为红色;
(4)Fe与O2在点燃时发生反应产生Fe3O4,把在充满氧气的集气瓶中燃烧后的铁丝残渣放入试管,加适量盐酸使其溶解,Fe3O4与HCl反应产生FeCl2、FeCl3和H2O,若铁丝残渣中含有未反应的Fe,则FeCl3与Fe反应转化为FeCl2,当溶液中不再含有Fe3+时,再往混合液中滴入少量KSCN溶液就不会变红色;
(5)使5mL 0.05 mol/L FeCl3完全发生反应:3KSCN+FeCl3=Fe(SCN)3+3KCl,根据物质反应关系可知n(KSCN)=3n(FeCl3),由于加入KSCN溶液的体积与FeCl3溶液的体积相同,也是5 mL,因此KSCN溶液的浓度就是FeCl3的三倍,故c(KSCN)=3×0.05 mol/L=0.15 mol/L;
(6)往FeCl2和KSCN的混合溶液中滴加氯水,首先发生反应:2Fe2++Cl2=2Fe3++2Cl-,Fe2+被氧化产生Fe3+,Fe3+遇SCN-使溶液变成红色,当氯水过量时,SCN-会被过量氯水氧化成(SCN)2逸出,导致溶液的红色褪去;若将溶液Y改为NaClO,由于NaClO是强碱弱酸盐,水解使溶液显碱性,烧瓶中的Fe3+与水解产生OH-反应会产生Fe(OH)3


科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g)![]() 3Z(g) △H=-a kJ·mol-1(a>0)。下列说法不正确的是
3Z(g) △H=-a kJ·mol-1(a>0)。下列说法不正确的是
A. 达到化学平衡状态时,反应放出的总热量可能达到akJ
B. 升高反应温度,逆反应速率增大,正反应速率减小
C. 达到化学平衡状态时,X、Y、Z的浓度不再发生变化
D. 0.1 mol X和0.2 molY充分反应生成Z的物质的量一定小于0.3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质类别和核心元素的价态是学习元素及其化合物性质的重要认识视角。如图是某元素的“价类二维图”,其中单质b是黄色固体,f、h均为正盐,且焰色都是黄色。下列说法不正确的是

A.d能使品红溶液褪色
B.a和c反应可以生成b
C.e的浓溶液可用铝槽车运输
D.h的水溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+![]() O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=
O2(g)=SO2(g)+H2O(g) ΔH1 ②2H2S(g)+SO2(g)=![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
③H2S(g)+![]() O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
O2(g)=S(g)+H2O(g) ΔH3 ④2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为
A.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)B.ΔH4=
(ΔH1+ΔH2-3ΔH3)B.ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=![]() (ΔH1+ΔH2-3ΔH3)D.ΔH4=
(ΔH1+ΔH2-3ΔH3)D.ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些共价键的键能数据如表(单位:kJmol-1):
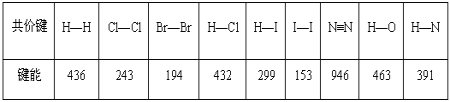
(1)把1mol Cl2分解为气态原子时,需要___(填“吸收”或“放出”)243kJ能量。
(2)由表中所列化学键形成的单质分子中,最稳定的是___;形成的化合物分子中最不稳定的是___。
(3)发射火箭时用气态肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知32gN2H4(g)完全发生上述反应放出568kJ的热量,热化学方程式是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验过程中,若一种气体极易溶于一种液体,则容易发生倒吸现象,给实验造成危险。现有4位同学分别设计了一个实验,希望通过观察到的明显现象来说明二氧化碳极易溶于氢氧化钠溶液,设计的装置如下:

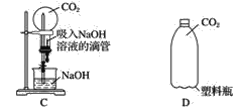
其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
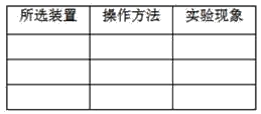
_______________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com