
| A、可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B、热的纯碱溶液去油污效果好 |
| C、加热AlCl3溶液可得到AlCl3固体 |
| D、Mg粉投入到饱和NH4Cl溶液中无明显现象 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、该溶液物质的量浓度为1mol?L-1 |
| B、该溶液中含有40g NaOH |
| C、配制100mL该溶液需用4.0g NaOH |
| D、量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 实验操作 | |
| A. | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| B. | 检验淀粉水解产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C. | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液,取出上层液体 |
| D. | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝酸银溶液,观察是否出现白色沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量指的是物质所含构成粒子数的多少,它的单位是“摩尔” |
| B、1mol H2O含有6.02×1023个水分子 |
| C、1mol H2O的质量是18g |
| D、1mol H2O蒸汽的体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ H+ HCO3- Cl- |
| B、K+ Ca2+ HCO3- OH- |
| C、Na+ K+ CO32- Cl- |
| D、Na+ K+ HCO3-CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氦气所含原子数为NA | ||
| B、2.3g金属钠变为钠离子时失去的电子数为0.1NA | ||
| C、常温常压下,44g CO2的质子数为15NA | ||
D、标准状况下,a L的氧气和氮气的混合物含有的分子数约为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
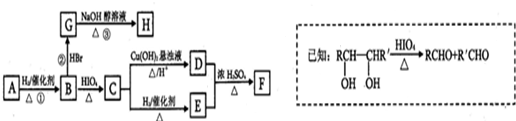
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com