
| A、标准状况下,22.4L氦气所含原子数为NA | ||
| B、2.3g金属钠变为钠离子时失去的电子数为0.1NA | ||
| C、常温常压下,44g CO2的质子数为15NA | ||
D、标准状况下,a L的氧气和氮气的混合物含有的分子数约为
|
| a |
| 22.4 |
| a |
| 22.4 |


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
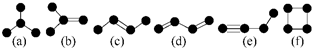 如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )
如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )| A、一个有机物a分子中含有8个氢原子 |
| B、有机物b、c、f互为同分异构体 |
| C、有机物d、e的1H核磁共振谱中,特征峰的数目相同 |
| D、有机物b、c、e中4个碳原子可处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于10 | B、小于10 |
| C、等于10 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B、热的纯碱溶液去油污效果好 |
| C、加热AlCl3溶液可得到AlCl3固体 |
| D、Mg粉投入到饱和NH4Cl溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业制取金属钾:Na(l)+KCl(l)?NaCl(l)+K(g),选取适宜的温度,使K成蒸汽从反应混合物中分离出来 |
| B、开启啤酒瓶时,有大量泡沫状气泡涌出瓶口 |
| C、工业合成氨气,采用铁触媒,并在500℃进行反应 |
| D、对于2HI(g)?H2(g)+I2(g);△H>0,升高温度可使颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com