
| A、吸水性 | B、脱水性 |
| C、强氧化性 | D、强酸性 |
科目:高中化学 来源: 题型:
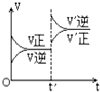 对达到平衡状态的可逆反应:X(?)+Y(?)?W(?)+Z(?)(已配平),在t'时增大压强,则正逆反应速率变化如右图所示(V代表速率,t代表时间.下列有关X、Y、Z、W的状态叙述正确的是( )
对达到平衡状态的可逆反应:X(?)+Y(?)?W(?)+Z(?)(已配平),在t'时增大压强,则正逆反应速率变化如右图所示(V代表速率,t代表时间.下列有关X、Y、Z、W的状态叙述正确的是( )| A、X、Y、W为气体,Z不是气体 |
| B、X、Y为气体,W、Z中有一种是气体 |
| C、W、Z为气体,X、Y中有一种是气体 |
| D、W、Z中有一种为气体,X、Y都不是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| N2 | H2 | NH3 | |
| ′起始浓度mol/L | 1.0 | 3.0 | 0 |
| 2秒末mol/L | 0.6 | 1.8 | 0.8 |
| A、0.2 | B、0.4 |
| C、0.6 | D、0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中必须含有金属阳离子 |
| B、物质中化学键被破坏,则一定发生化学变化 |
| C、NaCl的结构式为Na-Cl |
| D、H2O的沸点高于H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氦气所含原子数为NA | ||
| B、2.3g金属钠变为钠离子时失去的电子数为0.1NA | ||
| C、常温常压下,44g CO2的质子数为15NA | ||
D、标准状况下,a L的氧气和氮气的混合物含有的分子数约为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2的摩尔质量为78g |
| B、标准状况下,22.4LH2O的物质的量为1mol |
| C、同温、同压下,CO2的密度是H2密度的22倍 |
| D、1molHCl通入1L水中,所得盐酸的物质的量浓度为1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+O2?2SO3
在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+O2?2SO3查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com