
����Ŀ��������(C6H5COOHʽ����122���۵�122��4�棬�ܶ�Ϊ1.2659g��cm-3)��һ��һԪ�л����ᣬ����ˮ�������Ҵ���ʵ�������ɼױ�(ʽ����92���ܶ�Ϊ0.8669 g��cm-3)�Ʊ��������ʵ�����£�
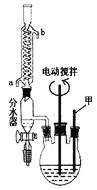
��һ������18.4g�ױ��������ữ��KMnO4��Һ������ͼ������ƿ�У����ȱ��ַ�Ӧ����Һ�¶���90����������Ӧ������
�ڶ���������Ӧ����Һ���ˣ���Һ��Ũ�����ữ�����˵ôֲ�Ʒ��
���������ֲ�Ʒ��ˮϴ��2��3�Σ���������ù���23.4g��
��ش��������⣺
(1)����������Ϊ_________________��
(2)��һ��������Ӧ�Ļ�ѧ����ʽΪ____________________________��
(3)�ڶ����г��˵��ŵ���____________________________________��
(4)������֤��ϴ�Ӹɾ��ķ�����_________________________________��
�������ѷ�����________ (�����)
a.��������Ȼ���b����ˮԡ�ϸ���c��ֱ�Ӽ��ȸ���
(5)����������֪������IJ���Ϊ_____________��
(6)ijѧ��Ϊ�ⶨ������ĵ���ƽ�ⳣ�����ʵ�����£������£���a mol�������b mol KOH��ϼ�ˮ�γ�2L��Һ�������Һ��pH=7�����ú�a��b�Ĵ���ʽ��ʾ���������Ka=____________������Һ�е�����Ũ�ȴ�С��ϵΪ____________________��
���𰸡� �¶ȼ� 5C6H5CH3+6KMnO4+9H2SO4��5C6H5COOH+3K2SO4+6MnSO4+14H2O �����ٶȿ죬�õ��Ĺ���ˮ���� ȡ���һ�ε�ϴ��Һ�еμ���������Һ������ͽ���ɣ���˵������ϴ�Ӹɾ��� b 96����9-9% b��10-7/(a-b) c(K+)=c(C6H5COO-)>c(H+)=c(OH-)
��������(1)�������������֪����������Ϊ�¶ȼơ�(2)��һ�������ķ�Ӧ�Ǽױ��������ﱽ���ᣬ��Ӧ�Ļ�ѧ����ʽΪ5C6H5CH3+6KMnO4+9H2SO4��5C6H5COOH+3K2SO4+6MnSO4+14H2O��(3)�ڶ����г��˵��ŵ��ǹ����ٶȿ죬�õ��Ĺ���ˮ���١�(4)���ڵڶ�������Ũ�������ԣ���˿���ͨ���������������жϵ�����֤��ϴ���Ƿ�ɾ���������ȡ���һ�ε�ϴ��Һ�еμ���������Һ������ͽ���ɣ���˵������ϴ�Ӹɾ��ˣ���������۵㳬��100�棬Ϊ�˼ӿ������̣�������ģ��������ѷ����Ƿ�ˮԡ�ϸ����ѡb��(5) 18.4g�ױ������ʵ�����0.2mol�����������ɱ�������0.2mol��������0.2mol��122g/mol��24.4g����˱�����IJ���Ϊ23.4g/24.4g��100%��96%��(6)���������غ��֪��Һ��c(C6H5COO-)��c(C6H5COOH)��0.5a�����������bmol����c(C6H5COO-)��0.5bmol�����Ա������Ka=![]() ��b��10-7/(a-b)��
��b��10-7/(a-b)��
���ݵ���غ��֪����Һ�е�����Ũ�ȴ�С��ϵΪc(K+)=c(C6H5COO-)>c(H+)=c(OH-)��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NaHC2O4��Һ��pH < 7�������£���pH=8.4��Na2C2O4��Һ�еμ�0.1mol/L��HCl��Һ����ҺpH��pOH[pOH=-lgc(OH-)�ݵı仯��ϵ��ͼ��ʾ�����и�����ʾ��Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����

A. a�㣺c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B. b�㣺c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C. c�㣺c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D. d�㣺c(OH-)+ c(Cl-)��c(H+)+2c(H2C2O4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaCl��NaBr��NaI��NaS��Һ����ѡ�õ��Լ���
A. ��ˮ B. AgNO3��Һ C. �� D. FeCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ����
A. �������ۼ�����Ϊ0.4NA�İ���(P4)�ͼ�������ʵ������
B. 10gŨ��Ϊ46�����Ҵ�ˮ��Һ�к��е���ԭ������Ϊ1.2NA
C. 2 g H2�ֱ���������C12��N2��ַ�Ӧ��ת�Ƶĵ�������Ϊ2NA
D. 1molFe(OH)3�뺬3molHI����Һ��ȫ��Ӧ����Һ������I-����ĿΪ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������λ�������������������Ϳ�ѧʵ����Ӧ�ù㷺��
��1��һ��������Fe2O3����鷴Ӧ��ȡ��������ͬʱ����CO��H2��
��֪��Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ��H=-27.6kJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g) ��H=+206.4kJ/mol
CO(g)+H2O(g)=CO2(g)+H2(g) ��H=-41.0kJ/mol
�ٷ�ӦFe2O3(s)+3 CH4(g)![]() 2Fe(s)+3CO(g) +6H2(g)�ġ�H______0���>������<����=����
2Fe(s)+3CO(g) +6H2(g)�ġ�H______0���>������<����=����
�����÷�Ӧ��5L���ܱ������н��У�1min��ﵽƽ�⣬�����ϵ�й�����������0.96g����ö�ʱ����CO��ƽ����Ӧ����Ϊ__________��
�����÷�Ӧ�ں��º�ѹ�����н��У��ܱ����÷�Ӧ�ﵽƽ��״̬����______(ѡ�����)
a��c(CH4)=c(CO)
b�����������������
c��v(CO)��v(H2)�ı�ֵ����
d����������ƽ����Է�����������
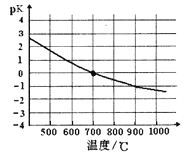
�ܸ÷�Ӧ�Ļ�ѧƽ�ⳣ���ĸ�����pK�淴Ӧ�¶�T�ı仯��������ͼ������ƽ���ƶ�ԭ���������ߵı仯���ɣ�______________________����700��ʱ���cƽ��(H2)=1.0mol��L-1����CH4��ת����Ϊ_________��
(2)���������Ҫ�ɷ��ǣ�FeCO3��ʵ�����п���ͨ��FeSO4��NaHCO3��Һ����Ƶ�FeCO3���йط�Ӧ�����ӷ���ʽΪ��____________________����֪Ksp[FeCO3]=3.2��10-11��H2CO3��Ka1=4.30��10-7��Ka2=5.61��10-11����ͨ���������ݼ�Ҫ����˵���÷�Ӧ�ܽ��е�ԭ��_____________________��
(3)Na2FeO4��һ�ָ�Ч��ˮ������ҵ����FeΪ������NaOHΪ�������Һ���е���Ʊ��� д�������缫��Ӧʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ľ������������������о���������Ҫ����;����ͼ�Ǵ����������Ʊ����Ĺ������̣�

��֪����1�����������Ҫ�ɷ���Al2O3�������������SiO2��Fe2O3�����ʣ�
��2����Һ�еĹ�������ƫ�����Ʒ�Ӧ�������ɹ������γ�������ѧ��Ӧ����ʽΪ2Na2SiO3+2NaAlO2+2H2O=Na2A12Si2O8��+4NaOH����ش��������⣺
��1����������Al2O3������������Һ��Ӧ�����ӷ���ʽΪ_________________________________��
��2���ڹ��������С��ữ��ʱ��������������B��________��������_______________________��д���ữ���̷�����Ӧ�Ļ�ѧ����ʽ��________________________________��
��3����ҵ����Al2O3��C��Cl2�ڸ��������·�Ӧ��ȡAlCl3��������ÿ����6.0 g̼���ʣ�ת��1 mol���ӣ���Ӧ�Ļ�ѧ����ʽΪ__________________________________��
��4��ijͬѧ�Ʋ������������������ȷ�Ӧ�õ����������л�����Fe2O3����������·�������֤��ȡһ���������Ͷ������ϡ�����У���Ӧһ��ʱ�����Ӧ��Ļ��Һ�еμ����ʼ���Һ���۲���Һ��ɫ�ı仯������֤�����������Ƿ���Fe2O3��
�����ʼ���_________(�ѧʽ)�����жϸ�ͬѧ��Ƶ�ʵ�鷽���ĺ�����_________(�������������������ԭ����_______________________________________����������������д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�����к͵ζ�ʵ�������˵����ȷ����
A. ϴ������ƿ���ɺ��ٵ������Һ
B. �ô�����Һ��ϴ��ƿ���Լ�С���
C. ���ζ��յ�ʱ�����ӿ̶���¼���ݣ��ᵼ�²ⶨ���ƫ��
D. ������װ������Һǰ������ˮϴ�������ø���Һ��ϴ�Լ�С���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶Ի�ѧ�仯����ʶ����ȷ����
A. ������ѧ���ı仯 B. ������µ�����
C. ��Ȼ��������״̬�ı仯 D. ��Ȼ�����������ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯����ȡ����Ӧ����(����)
A. ������ˮ��ϣ�ˮ����ɫ B. �ױ����������ױ�
C. �Ҵ���Ũ������������ȡ��ϩ D. ����������һ���������������Ȼ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com