
【题目】鉴别NaCl、NaBr、NaI、NaS溶液可以选用的试剂是
A. 溴水 B. AgNO3溶液 C. 苯 D. FeCl3溶液
科目:高中化学 来源: 题型:
【题目】八角茴香属于草本植物,是我国民间常用做烹调的香料。医学研究成果显示,从八角茴香中可以提取到莽草酸,莽草酸有抗炎、镇痛作用,是合成某些抗癌药物的中间体。莽草酸的分子结构模型如图所示(分子中只有C、H、O三种原子)。下列有关莽草酸结构、性质叙述正确的是( )

A. 与氢气加成反应消耗氢气的物质的量为4mol.
B. 不能使溴水褪色,但能与氢气发生加成反应
C. 分子中同时含有羧基、羟基、碳碳双键三种官能团
D. 能与氯化铁溶液反应,溶液呈紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】左乙拉西坦(物质G)是一种治疗癫痫的药物,可通过以下方法合成:

(1)B中的含氧官能团名称为_______。
(2)E→F的反应类型为_________。
(3)X的分子式为C4H7ON,写出X的结构简式:____________。
(4)写出同时满足下列条件的G的一种同分异构体的结构简式:________。
① 能发生水解反应,水解产物仅有一种,且为α-氨基酸;
② 分子中含六元环结构,且有4种不同化学环境的氢。
(5)请以![]() 和
和![]() 为原料制备
为原料制备 ,写出相应的合成路线流程图________ [合成须使用试剂HAl(t-Bu)2,无机试剂任用,合成路线流程图示例见本题题干]。
,写出相应的合成路线流程图________ [合成须使用试剂HAl(t-Bu)2,无机试剂任用,合成路线流程图示例见本题题干]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:下表为25℃时某些弱酸的电离平衡常数。
CH3COOH | HClO | H2CO3 |
Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
下图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是 ( )

A. 相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+) > c(ClO-)> c(CH3COO-)> c(OH-)> c(H+)
B. 向NaClO溶液中通入少量二氧化碳的离子方程式为: ClO-+CO2+ H2O =HClO+CO32-
C. 图像中a、c两点处的溶液中![]() 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D. 图像中a点酸的总浓度大于b点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:

(1)反应的ΔH________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应的平衡常数K1为________。
(2)100 ℃时达平衡后,将反应容器的容积增大一倍,平衡向________(填“正反应”或“逆反应”)方向移动,达到新的平衡后N2O4的浓度范围是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用“ Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“ Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 ![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:

(1)放电时,正极的电极反应式为______________________________________________。
(2)若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为________ g。
(3)选用高氯酸钠-四甘醇二甲醚作电解液的优点是___________________________________(至少写两点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某氨基酸(CxHyNzOp)的分子组成。取m g 该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。按下图所示装置进行实验。

请回答下列问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是__________________
(2)以上装置中需要加热的仪器有_________________(用字母填空,下同)。操作时应先点燃_______处的酒精灯。
(3)A装置中发生反应的化学方程式是_____________________。
(4)装置D的作用是___________________________。
(5)读取N2的体积时,应注意
①______________________
②______________________
③______________________
(6)实验中测得N2的体积为V mL(标准状况)。为确定此氨基酸的化学式,还需要的有关数据是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g·cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇。实验室中由甲苯(式量:92,密度为0.8669 g·cm-3)制备苯甲酸的实验如下:
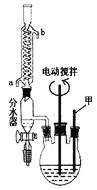
第一步:将18.4g甲苯和硫酸酸化的KMnO4溶液置于如图的三颈瓶中,加热保持反应物溶液温度在90℃左右至反应结束。
第二步:将反应后混合液过滤,滤液用浓盐酸酸化,抽滤得粗产品。
第三步:粗产品用水洗涤2到3次,干燥称量得固体23.4g。
请回答下列问题:
(1)仪器甲的名称为_________________。
(2)第一步发生反应的化学方程式为____________________________。
(3)第二步中抽滤的优点是____________________________________。
(4)第三步证明洗涤干净的方法是_________________________________;
干燥的最佳方法是________ (填代号)
a.空气中自然风干b.沸水浴上干燥c.直接加热干燥
(5)由以上数据知苯甲酸的产率为_____________。
(6)某学生为测定苯甲酸的电离平衡常数设计实验如下:常温下,将a mol苯甲酸和b mol KOH混合加水形成2L溶液,测得溶液的pH=7,请用含a、b的代数式表示出苯甲酸的Ka=____________,该溶液中的离子浓度大小关系为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与下图中四种物质发生的反应填空(a、b、c、d重合部分代表物质间可反应,且氯水足量)。

(1)能证明氯水具有漂白性的是_____(填“a”“b”“c”或“d”)。
(2)c过程中的现象是______________
b过程中发生反应的离子方程式为__。
(3)a过程中发生反应的化学方程式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com