
【题目】某化学兴趣小组的同学们对SO2与漂粉精、过氧化钠的反应进行实验探究:
【实验I】SO2与漂粉精反应。
操作 | 现象 |
取4g 漂粉精固体,加入100mL 水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
| 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的反应中氧化剂与还原剂的物质的量之比为__________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是____________。
(3)兴趣小组将A中产生的白雾引出导入硝酸酸化的AgN03溶液中,有沉淀产生,据此判断白雾成分为HCl小液滴,该结论合理吗?____________请说明理由____________________。
(4)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。该反应的离子方程式为______________。
(5)①将A瓶中混合物过滤、洗涤,得到沉淀X,X的成分是____________(填化学式);
② 用离子方程式解释现象3中黄绿色褪去的原因____________________。
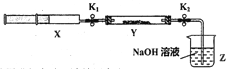
【实验II】SO2与过氧化钠反应。将一定量(过量)SO2充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好。在室温下按图示装置进行实验,请填写空白。
操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | (1)_______ | (2)反应的化学方程式:_________________ |
将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | (3)________ | (4)不用解释 |
【答案】【实验I】(1)1:1;(2)碱性、漂白性;
(3)不合理(1分);因为白雾中可能含有少量Cl2和SO2,也容易产生沉淀(1分);
(4)ClO-+Cl-+2H+=2H2O+Cl2↑;
(5)①CaSO4(1分);②SO2+Cl2+2H2O+Ca2+=CaSO4↓+2Cl-+4H+(或SO2+Cl2+2H2O=SO42-+2Cl-+4H+)
【实验II】(1)浅黄色固体变为白色;(2)SO2+Na2O2=Na2SO4;
(3)Z中NaOH溶液倒吸入Y管中
【解析】
试题分析:(1)Cl2和Ca(OH)2制取漂粉精反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,氯气既是氧化剂,也是还原剂,氯化钙是还原产物,次氯酸钙是氧化产物,因此氧化剂与还原剂的物质的量之比为1:1;
(2)pH 试纸先变蓝(约为12),后褪色,说明漂粉精溶液具有的性质是碱性、漂白性;
(3)由于白雾中可能含有少量Cl2和SO2,导入硝酸酸化的AgNO3溶液中,也容易产生沉淀,所以结论不合理;
(4)现象2中溶液变为黄绿色,说明有氯气产生,这是由于随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应,该反应的离子方程式为ClO-+Cl-+2H+=2H2O+Cl2↑;
(5)①SO2被氧化生成硫酸,进而生成硫酸钙沉淀,因此将A瓶中混合物过滤、洗涤,得到的沉淀为CaSO4;
②由于氯气能把SO2氧化为硫酸,进而产生硫酸钙沉淀,所以黄绿色褪去,反应的离子方程式为SO2+Cl2+2H2O+Ca2+=CaSO4↓+2Cl-+4H+。
【实验II】过氧化钠具有强氧化性,能把SO2氧化为硫酸钠,因此实验现象是浅黄色固体变为白色,反应的化学方程式为SO2+Na2O2=Na2SO4;将注射器活塞退回原处并固定,待装置恢复到室温,打开K2后由于SO2被吸收,压强减小,从而产生倒吸现象,所以实验现象为Z中NaOH溶液倒吸入Y管中。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某同学设计如下实验方案:

(1)操作①为____________;
(2)操作②~④加入的试剂可以为 。
(3)如何判断SO![]() 已除尽,简述实验操作 ;
已除尽,简述实验操作 ;
(4)实验过程中产生的多次沉淀_________(填“需要”或“不需要”)多次过滤,理由 。
(5)该同学设计的实验方案____________(填“合理”或“不合理”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于离子键、共价键的各种叙述中,下列说法中正确的是( )
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子中
C.任何物质里都含有化学键
D.在共价化合物分子内,一定不存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.同温同压下,相同数目的分子必具有相同的体积
B.等质量的O2和H2的物质的量之比为16∶1
C.不同的气体若体积不等,则它们所含的分子数一定不等
D.同温同体积下,两种气体的物质的量之比等于压强之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加成反应也是有机化学中的一类重要的反应类型,下列各组物质中不能全部发生加成反应的是
A.乙烷、乙烯 B.乙烯、乙炔
C.氯乙烯、溴乙烯 D.顺-2-丁烯、反-2-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、K+、Mg2+、Cu2+等阳离子及MnO![]() 、SiO
、SiO![]() 、AlO
、AlO![]() 、CO
、CO![]() 、HCO
、HCO![]() 、SO
、SO![]() 、Cl-等阴离子,已知:①该溶液呈无色;②经测定溶液的pH=12;③取少量溶液,加入足量100 mL 2 mol·L-1稀盐酸进行酸化,有白色沉淀生成,还得到一种无色无味的气体,该气体使澄清石灰水(足量)变浑浊。对酸化后的溶液过滤,得到滤液甲。
、Cl-等阴离子,已知:①该溶液呈无色;②经测定溶液的pH=12;③取少量溶液,加入足量100 mL 2 mol·L-1稀盐酸进行酸化,有白色沉淀生成,还得到一种无色无味的气体,该气体使澄清石灰水(足量)变浑浊。对酸化后的溶液过滤,得到滤液甲。
(1)由①②③可判断:原溶液中一定不存在的离子是_____________,一定存在的离子是_____________。
(2)将滤液甲分成两等份,一份中逐滴加入氨水、最终有白色胶状沉淀,说明原溶液中一定有_____________(填离子符号),刚开始加入氨水时,没有沉淀产生,原因是____________________(用离子方程式表示);另一份中加入足量的Ba(NO3)2溶液,有白色沉淀生成,说明原溶液中一定有_____________(填离子符号),过滤得到滤液乙。
(3)往滤液乙中加入足量的AgNO3溶液,过滤、洗涤、干燥得固体26.5 g,则原溶液中是否有Cl-?_____________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素及其化合物的说法不正确的是( )
A.Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应
B.Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同
C.在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解
D.金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法错误的是
A.可用铝槽密闭盛装浓硫酸
B.工业上利用蛋白质的水解反应生产肥皂和甘油
C.乙醇可用作汽车燃料
D.食醋可用于消除暖水瓶中的水垢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com