
【题目】下列气态氢化物中,最不稳定的是( )
A. HI B. HBr C. HCl D. HF
科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
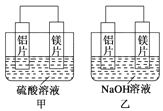
(1)写出甲中正极的电极反应式___________________。
(2)乙中总反应的离子方程式:________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出_____________活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有______________。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,应具体问题具体分析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
A.只有硫酸铜作氧化剂
B.SO![]() 既不是氧化产物又不是还原产物
既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3∶7
D.1 mol硫酸铜可以氧化5/7 mol的硫原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O2(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
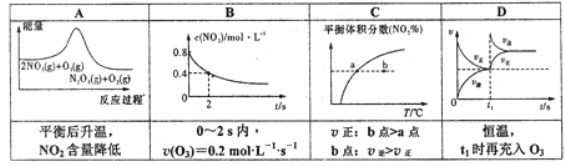
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学们对SO2与漂粉精、过氧化钠的反应进行实验探究:
【实验I】SO2与漂粉精反应。
操作 | 现象 |
取4g 漂粉精固体,加入100mL 水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
| 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的反应中氧化剂与还原剂的物质的量之比为__________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是____________。
(3)兴趣小组将A中产生的白雾引出导入硝酸酸化的AgN03溶液中,有沉淀产生,据此判断白雾成分为HCl小液滴,该结论合理吗?____________请说明理由____________________。
(4)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。该反应的离子方程式为______________。
(5)①将A瓶中混合物过滤、洗涤,得到沉淀X,X的成分是____________(填化学式);
② 用离子方程式解释现象3中黄绿色褪去的原因____________________。
【实验II】SO2与过氧化钠反应。将一定量(过量)SO2充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好。在室温下按图示装置进行实验,请填写空白。
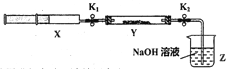
操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | (1)_______ | (2)反应的化学方程式:_________________ |
将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | (3)________ | (4)不用解释 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用98%的浓H2SO4(ρ="1.84" g/cm3)配制成浓度为1.0mol/L的稀硫酸250 mL。
(1)现有主要仪器:A量筒 B烧杯 C玻璃棒 D胶头滴管 还缺少的仪器_______________;
(2)请将下列操作序号按正确顺序填在横线上:
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加水至刻度
D.洗涤烧杯、玻璃棒2-3次
E.稀释浓H2SO4
F.冷却后将溶液转入容量瓶
其操作正确顺序为__________________;
(3)下列操作中,容量瓶所不具备的功能有________(填序号);
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.贮存溶液
E.用来加热和溶解固体溶质
(4)简要回答下列问题
①所需浓H2SO4的体积为___________mL;
②将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌,若搅拌过程中有液体溅出,会使最终结果_________ (填“偏高”、“偏低”或“无影响”,下同);若将量筒洗涤转移到容量瓶会使最终结果_________ ;定容时水加多后用滴管吸出会使结果_________;
(5)该浓硫酸与等质量的水混合所得溶液的物质的量浓度________9.2 mol/L (填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
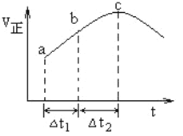
A. 反应在c点达到平衡状态
B. 反应物浓度:a点小于b点
C. 反应物的总能量低于生成物的总能量
D. △t1=△t2时,SO2的转化率:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同物质的量的浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3∶2∶1,则SO![]() 浓度之比为1∶1∶3
浓度之比为1∶1∶3
B. 将10 mL 1 mol/L H2SO4稀释成0.1 mol/L的H2SO4,可向该溶液中加入100 mL水
C. 将1 mol/L的NaCl溶液和0.5 mol/L的BaCl2溶液等体积混合后,不考虑溶液体积变化c(Cl-)=0.75 mol/L
D. 50 g浓度为c mol/L,密度为ρg·cm-3的氨水(ρ<1)中加入一定量的水(ρ=1g·cm-3)稀释成0.5c mol/L,则加入水的体积应小于50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为 3Zn + 2K2FeO4+ 8H2O![]() 3Zn(OH)2+ 2Fe(OH)3+ 4KOH下列叙述不正确的是( )
3Zn(OH)2+ 2Fe(OH)3+ 4KOH下列叙述不正确的是( )
A. 放电时负极反应为:Zn-2e- +2OH-= Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+ 5 OH-= FeO42-+ 4H2O
C. 放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com