
����Ŀ�����Ƕ�������ʶ�����м��������ʷ��������һ����dz����ɵͼ���������ʶ���̡�����Ŀǰ��ѧ�α��е����������1887�갢������˹(Arrhenius)��������������ۡ�
(1)1905�긻������(Franklin)�����о���ˮ��Һ���������ԣ��Ѱ�������˹��ˮΪ�ܼ��ĸ��������ƹ㵽�κ��ܼ������������ܼ����ۡ�����ܼ�������Ϊ���������������ܼ������ӵ�����Ϊ�ᣬ�������������ܼ������ӵ�����Ϊ���д��Һ������ķ���ʽ(���ɵ����������������)��_________��
(2)1923�굤��ѧ�Ҳ���˹�غ�Ӣ����ѧ���������������������ۡ����ܹ���������(������)���κ����ʶ�������ܹ���������(������)�����ʶ��Ǽ���������ۣ���������ˮ��Һ�ȿɿ������ֿɿ��������________(����ĸ)��
A��H2O��B��NH![]() ��C��OH����D��HCO
��C��OH����D��HCO![]() ��E��CH3COO�� F��Cl��
��E��CH3COO�� F��Cl��
(3)1923��·��˹(Lewis)����˹��������������ܸ������ӶԶ������γɻ�ѧ���������Ǽ�����ܺ͵��ӶԽ���γɻ�ѧ�����������ᡣ�磺
H�������� ����[��OH]���D�� H��OH
��(���ӶԽ�����)����(���ӶԸ�����)����Ӧ����
��ָ������������Ӧ�е����
��H3BO3��H2O![]() H����B(OH)
H����B(OH)![]() ���÷�Ӧ�еļ���________(�H3BO3����H2O��)��
���÷�Ӧ�еļ���________(�H3BO3����H2O��)��
��NaH��H2O===NaOH��H2�����÷�Ӧ�е�����________(�NaH��'��H2O��)��
���𰸡�NH3��NH3![]() NH
NH![]() ��NH
��NH![]() ADH2OH2O
ADH2OH2O
��������
(1)ˮ�ĵ���ʵ���������ӵ�ת�ƣ�H2O��H2O![]() H3O����OH������ˣ�Һ���а��ĵ��뼴����ת�ƣ��ɱ�ʾΪNH3��NH3
H3O����OH������ˣ�Һ���а��ĵ��뼴����ת�ƣ��ɱ�ʾΪNH3��NH3![]() NH
NH![]() ��NH
��NH![]() ��(2)�������У��ܽ�����ӵ���H2O��OH����HCO
��(2)�������У��ܽ�����ӵ���H2O��OH����HCO![]() ��CH3COO�������ͷ����ӵ���H2O��NH
��CH3COO�������ͷ����ӵ���H2O��NH![]() ��HCO
��HCO![]() ����˼ȿɿ������ֿɿ��������H2O��HCO
����˼ȿɿ������ֿɿ��������H2O��HCO![]() ����ѡAD��(3)������H2O������OH����H3BO3[B(OH)3]�е�Bԭ���γɻ�ѧ����OH���ṩ���Ӷԣ�H2O�Ǽ����H2O������NaH����ʽNa��[��H]������Ӧ��H���ṩ�ĵ��Ӷ���H2O�����H���γ�H2�еĻ�ѧ����NaH�ǼH2O���ᣬ����H2O��
����ѡAD��(3)������H2O������OH����H3BO3[B(OH)3]�е�Bԭ���γɻ�ѧ����OH���ṩ���Ӷԣ�H2O�Ǽ����H2O������NaH����ʽNa��[��H]������Ӧ��H���ṩ�ĵ��Ӷ���H2O�����H���γ�H2�еĻ�ѧ����NaH�ǼH2O���ᣬ����H2O��


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ�����ȷ����
A.������������Ȫˮ��ˮ��
B.�����������CO2��SO2��CO
C.�Σ������ơ��Ȼ�李�����
D.������ʣ�CH3COOH��H2O��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�������������ԭ�����͵���ʵ��
A. ̼��Ʋ�����ˮ������������
B. ��2NO2(g)![]() N2O4(g)��ɵ�ƽ����ϵ����ѹ����ɫ����
N2O4(g)��ɵ�ƽ����ϵ����ѹ����ɫ����
C. ��ѹ�ȳ�ѹ�����ںϳɰ��ķ�Ӧ
D. ���ȵĴ�����Һϴ����ʱ��ȥ��Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2005��ŵ������ѧ�������ʩ�˵��˷��ֽ�����Ŀ��������������Ϊ�dz���Ч��ϩ�����ֽ��������ҵ��ұ����Ļ�ѧԭ��Ϊ��2MoS2��7O2![]() 2MoO3��4SO2����MoO3��2NH3��H2O====��NH4��2MoO4��H2O������NH4��2MoO4��2HCl====H2MoO4����2NH4Cl����H2MoO4
2MoO3��4SO2����MoO3��2NH3��H2O====��NH4��2MoO4��H2O������NH4��2MoO4��2HCl====H2MoO4����2NH4Cl����H2MoO4![]() MoO3��H2O;���û�ԭ����MoO3��ԭ�ɽ����⡣
MoO3��H2O;���û�ԭ����MoO3��ԭ�ɽ����⡣
������˵����ȷ����
A. MoS2���ղ�����β����ֱ���ſ�
B. MoO3�ǽ��������Ҳ�Ǽ���������
C. H2MoO4��һ��ǿ��
D. ����H2��CO�����ֱ�ԭ������MoO3�������Ļ�ԭ�������ʵ���֮��Ϊ3��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼����������ָͨ��һ���ķ�������ҵ�����в�����CO2������������á��������NaOH��Һ��������CO2�������������ͼ��ʾ(��������������δ���)��
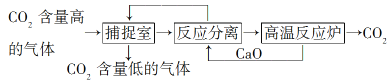
�����йظ÷�������������ȷ����(����)
���ܺ�С�Ǹ÷�����һ���ŵ�
�����������У����������ʿ���ѭ������
�ۡ���Ӧ���롱�����У��������ʵĻ����������������ᾧ
�ܸ÷����ɼ���̼�ŷţ�����������CO2���������Ʊ��״��Ȳ�Ʒ
A. �٢� B. �ڢ� C. �ۢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л������������Ϊ��ȷ���ǣ�
A.��̼Ԫ�صĻ�����һ�����л�������
B.�������ϩ��Ϊͬϵ��
C.�����Ӻ���̼̼˫�������Կ���ʹ���Ը��������ɫ
D.��������춡�黥Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ��Ӧ���ʵ���Ҫ������
A.��Ӧ�������B.��Ӧ�¶�
C.ʹ�ô���D.��Ӧ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�Ӱ뾶�Ĵ�С˳����ȷ����(����)
��2s22p2����3s23p3����2s22p4����3s23p2
A. �������������� B. ��������������
C. �������������� D. ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����( )
A. 136g���ڵ�KHSO4�к���2NA��������
B. 40gH218O��40gD2O��������������Ϊ20NA
C. 1molFe�ֱ���������ϡ�����ϡ���ᷴӦת�Ƶ�������Ϊ2NA
D. ��״���£�22.4LNO��11.2LO2��Ϻ�����ķ�������ΪNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com