
����Ŀ������˵��������ʵ���ǣ� ��
A. ��������ˮ���������c(H+)=10-12mol/L����Һ�м������۶��ܹ���������
B. ��0.2000 /L NaOH����Һ�ζ�HCl��CH3COOH�Ļ����Һ�����Һ���������Ũ�Ⱦ�ԼΪ0.1mol/L����������ʱ����Һ�е���δ����ȫ�к�
C. �������ͭ��Һһ��ʱ���������ͭ���岻����ʹ��Һ�ָ���ԭ����Ũ��
D. ��NaAlO2��Na2CO3�Ļ����Һ����εμ�����ֱ����������ʼû�г�������������������������ʧ
���𰸡�B
��������
A����������ˮ���������c(H��)=10-12mol��L-1������������ˮ�ĵ��룬����Ϊ�ᣬҲ����Ϊ����������Ϊ���ᣬ������Al��Ӧ������H2����A���������⣻
B��HClΪǿ�ᣬCH3COOHΪ���ᣬ�ζ�ʱ��������ΪHCl����NaOH��Ӧ����HCl�ζ�����ٵζ�CH3COOH�����CH3COOH��NaOH�ζ�������ʱ����Һ�е�����ΪNaCl��CH3COOH��CH3COONa��CH3COOHδ����ȫ�кͣ���B��ȷ��
C�����CuSO4��Һ������ܷ�ӦΪ2CuSO4+2H2O ![]() 2Cu+O2��+2H2SO4������CuO��ʹ��Һ�ָ���ԭ����Ũ�ȣ���C����
2Cu+O2��+2H2SO4������CuO��ʹ��Һ�ָ���ԭ����Ũ�ȣ���C����
D��AlO2-���H+����ǿ��CO32-�������Һ����ε������ᣬAlO2-����H+����AlO2-+H++H2O=Al(OH)3��������ʼʱ�������������������ɣ���D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ������Ũ�����Լ�ƿ��ǩ�ϵIJ������ݣ���ش����⡣
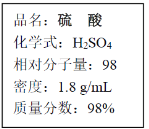
��1������������ʵ���Ũ����________mol/L��
��2��ijʵ����Ҫ90mL3.0mol/Lϡ���ᣬ���Ƹ���Һ�������㣬��Ҫ����Ͳ��ȡ___mLŨ���ᡣ
��3�����������ƹ���ʾ��ͼ�У��д�����ǣ���д��ţ�________��

��4�������������������ϡ����Ũ��ƫ�ߵ���________��
A ������ˮ����Ͳ�в���������ϴ���ϲ� B ����ƿϴ�Ӻ�δ�����ﴦ��
C ��Һδ����ȴ�Ͷ��� D δϴ���ձ��Ͳ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ����գ�
��1������![]() ������________��
������________��
��2������������е�O����18Oʱ���Ҵ������е�O����16Oʱ��������һ�������·�Ӧ����������ˮ����Է�������Ϊ______��
��3����ѧ������ϢϢ��ء�����������ȷ����___(����ĸ����)��
A����ͷԽ��Խ�� B����ե��֭������ˮ�����
C����֬��ˮ��ɱ�������� D�������еĵ��۾�ˮ��ɱ�ɾ�
��4��ij������C3H6O2�ĺ˴Ź�����(NMR)����3����,��ǿ�ȱ�Ϊ3��2��1����û�����Ľṹ��ʽ����Ϊ_______��д��һ�ּ��ɣ���
��5����������һ�־��п��������ס�����Ѫ��������Ե��㶹�ػ��������ӽṹ��ͼ��ʾ���ش��������⡣
![]()
�������صĻ�ѧʽΪ____����������������____��
��1mol�˻��������______molBr2��Ӧ����������____molNaOH��Ӧ��
��6����ȩ������������ͭ�ķ�Ӧ��ʾ�˼�ȩ�Ļ�ԭ�ԣ�������Ӧ�Ļ�ѧ����ʽͨ����ʾΪHCHO+2Cu(OH)2+NaOH![]() HCOONa+Cu2O��+3H2O��������������������ͭ�м���4.00mL��ȩˮ��Һ����ַ�Ӧ�������һ����ʵ����֤��ȩ���������ﲻ�Ǽ����Ρ�____�����ɹ�ѡ�õ��Լ�������ͭ��Һ����ȩ�����ᡢ����������Һ����
HCOONa+Cu2O��+3H2O��������������������ͭ�м���4.00mL��ȩˮ��Һ����ַ�Ӧ�������һ����ʵ����֤��ȩ���������ﲻ�Ǽ����Ρ�____�����ɹ�ѡ�õ��Լ�������ͭ��Һ����ȩ�����ᡢ����������Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ�й�����ĵ���ƽ�ⳣ�����������й�˵����ȷ���ǣ� ��
���ữѧʽ | CH3COOH | HCN | H2CO3 |
����ƽ�ⳣ�� | 1.8��10-5 | 4.9��10-10 | K1��4.3��10-7 K2��5.6��10-11 |
A. �����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH(NaCN)��pH(Na2CO3)��pH(CH3COONa)
B. ����������μ�ˮ������Һ�ĵ����ԡ�����ĵ���̶ȡ�pH����������С
C. NaCN��ͨ������CO2�����Ļ�ѧ��ӦΪ��NaCN+CO2+H2O=HCN+NaHCO3
D. ϡ��HCN��Һ�����У�![]() ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ȼ��֮һ�������������泥�NH4ClO4���Ĺ��������ȼʱ�����۱���������������������立�Ӧ��2NH4ClO4�TN2��+4H2O+Cl2��+2O2������Ӧ�ų������ȡ�
��1���÷�Ӧ�б�������Ԫ����___��___��
��2�����������뻹ԭ���������֮��Ϊ___��
��3���÷�Ӧ�������ɱ����2.24LCl2ʱ������ת����Ϊ___��
��4�������ɵ�ˮ�ڸ�����ҲΪ��̬�����������ƽ��Ħ������Ϊ__g/mol(С�������һλ)��
��5���������(K2FeO4)��һ��ǿ��������������ˮ������Ϊˮ��������������ز��ϡ�FeCl3��KClO��ǿ���������·�Ӧ����ȡK2FeO4���䷴Ӧ�����ӷ���ʽΪ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
�ش��������⣺
��1��ZԪ�������ڱ��е�λ��Ϊ___��
��2��������ʵ��˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����___��
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ�
c��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��3��X��Z��Ԫ�صĵ��ʷ�Ӧ����1molX����ۻ�����ָ������£�����687kJ����֪�û�������ۡ��е�ֱ�Ϊ-69���58�棬д���÷�Ӧ���Ȼ�ѧ����ʽ___��
��4��̼��þ�γɵ�1mol������Q��ˮ��Ӧ������2molMg(OH)2��1mol��������������̼��������Ϊ9��1�����ĵ���ʽΪ___��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��Ϊ�������������������������ʵ�ת�����̻ش�������⣺
Fe![]() A
A![]() B
B![]() C
C
��1����Ӧ������������������ԭ��Ӧ����________________������ţ���
��2����B����Һ�е��뼸��KSCN��Һ�ɹ۲쵽��������__________��
��3����Ӧ�������ӷ���ʽΪ _____________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��800��ʱ����2L���ܱ������з�����Ӧ��2NO(g)+O2(g)![]() 2NO2��n(NO)��ʱ��ı仯���±���ʾ��
2NO2��n(NO)��ʱ��ı仯���±���ʾ��
ʱ���Ms | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)�Mmol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1����0��3s�ڣ���NO��ʾ��ƽ����Ӧ������(NO)��_____________��
��2��ͼ�б�ʾNOŨ�ȱ仯��������_______(����ĸ����)��
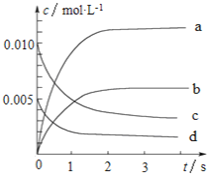
��3����ƽ��ʱNO��ת����Ϊ________��
��4����˵���÷�Ӧ�Ѵﵽƽ��״̬����_________(�����)��
A������������ɫ���ֲ���
B�����������ܶȱ��ֲ���
C������ (NO2)��2���� (O2)
D����������ƽ����Է����������ֲ���
��5�������µ�850�棬��ƽ���n(NO)��n(NO2)����Ӧ��________(��������Ӧ�����������淴Ӧ������)�ƶ���
��6������һ��������0.2molNO������������Ӧ����ƽ��ʱ��÷ų�������ΪakJ����ʱNOת����Ϊ80%����2molNO������ȫ��Ӧ�ų�������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����������У�����ȷ����
��F���Ľṹʾ��ͼ��![]()
���������ĵ���ʽ��![]()
��HClO�Ľṹʽ��H��Cl��O
��SO3��ˮ��Һ�ܵ��磬˵��SO3�ǵ����
��NaHSO3��ˮ�еĵ��뷽��ʽ��NaHSO3��Na����H����SO32-
��ͬ����������ת����ͬλ�ؼ��ת�����ǻ�ѧ�仯
A. 1�� B. 2�� C. 5�� D. 6��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com