
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为___。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是___;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式___。
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为___。Q与水反应的化学方程式为__。
【答案】第三周期,ⅦA族 ac Si(s)+2Cl2(g)=SiCl4(l) △H=-687kJ/mol 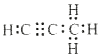 Mg2C3+4H2O=2Mg(OH)2+C3H4↑
Mg2C3+4H2O=2Mg(OH)2+C3H4↑
【解析】
由元素在周期表中的位置可知X为Si,Y为O,Z为Cl;
(1)根据元素的“构、位、性”进行判断;
(2) 根据同主族非金属性强弱的判断方法进行分析;
(3) 根据书写热化学方程式的方法进行求算;
(4)按烃分子中碳氢质量比、物质的量之比进行分析。
由元素在周期表中的位置可知X为Si,Y为O,Z为Cl;
(1)Z元素为氯元素,核电荷数为17,原子核外有三个电子层,最外层有7个电子,Z位于周期表中第三周期第ⅤⅡA族;
(2) a.Y单质与H2S溶液反应,溶液变浑浊,说明氧气的氧化性比硫强,则说明Y元素的非金属性比S元素的非金属性强;
b.在氧化还原反应中,1molY单质比1molS得电子多,氧化性强弱与得电子数多少没有必然关系,故不能说明Y与S非金属性的强弱;
c.元素的非金属性越强,氢化物的稳定性越强,Y和S两元素的简单氢化物受热分解,前者的分解温度高,说明Y的非金属性较强;
故答案为ac;
(3) 根据SiCl4的熔点和沸点,说明其室温下呈液态,根据书写热化学方程式的方法,该反应的热化学方程式为Si(s)+2Cl2(g)=SiCl4(l) △H=-687kJ/mol;
(4)该烃分子中碳氢质量比为9:1,碳氢物质的量之比为![]() =
=![]() ,结合碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,Q的化学式为Mg2C3,烃的化学式为C3H4,电子式为
,结合碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,Q的化学式为Mg2C3,烃的化学式为C3H4,电子式为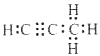 ,Q与水反应的化学方程式为Mg2C3+4H2O=2 Mg(OH)2+C3H4↑。
,Q与水反应的化学方程式为Mg2C3+4H2O=2 Mg(OH)2+C3H4↑。


科目:高中化学 来源: 题型:
【题目】二硫代磷酸锌( ![]() )是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
)是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
(1)二硫代磷酸锌结构中,P的杂化方式为__________________,C1、P、S的第一电离能由大到小的顺序为_____________________。
(2)Zn2+的价层电子排布式为________________,锌能够跟强碱溶液反应生成[Zn(OH)4]2-,不考虑空间构型,[Zn(OH)4]2-的结构可用示意图表示为__________________。
(3)硫元素能形成多种含氧酸,两分子硫酸脱去一分子水生成焦硫酸(H2S2O7),则1mol焦硫酸中含有硫氧键的数目为____________;用价层电子互斥理论判断并解释SO32-与SO42-键角的相对大小。
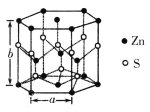
(4)纤锌矿的六方晶体结构如图所示,该晶胞的化学式为___________,其晶胞参数分别为a pm和b pm,则该晶体的密度为____________________g·cm-3(用含a、b、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,综合利用CO2对构建低碳社会有重要意义。
(1)已知: H2(g)+ ![]() O2(g) =H2O(g) ΔH=-241.8kJ·mol-1 CO2(g) = CO(g)+
O2(g) =H2O(g) ΔH=-241.8kJ·mol-1 CO2(g) = CO(g)+ ![]() O2(g) ΔH=+283.0kJ·mol-1 则反应:CO2(g)+H2O(g) =CO(g)+H2(g)+O2(g) ΔH=________。
O2(g) ΔH=+283.0kJ·mol-1 则反应:CO2(g)+H2O(g) =CO(g)+H2(g)+O2(g) ΔH=________。
(2)工业生产中可利用H2还原CO2制备清洁能源甲醇:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH<0
CH3OH(g)+H2O(g) ΔH<0
①保持温度、体积一定,能说明上述反应达到平衡状态的是_________。
A.容器内压强不变 B.3v正 (CH3OH)= v正 (H2)
C.容器内气体的密度不变 D.CO2与H2O的物质的量之比保持不变
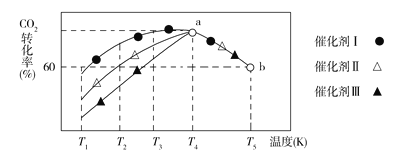
②将一定量的CO2和H2充入到某恒容密闭容器中,测得在不同催化剂作用下,相同时间内CO2的转化率随温度的变化如图所示,催化效果最好的是催化剂________(填“Ⅰ”“Ⅱ”或“Ⅲ”),该反应在a点达到平衡状态,a点的转化率比b点的高,其原因是________。
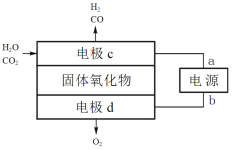
(3)固体氧化物电解池(SOEC)可用于高温电解CO2/H2O,既可高效制备合成气(CO和H2),又可实现CO2的减排,其工作原理如图。
①电源正极为________(填“a”或“b”),电极c上发生的电极反应式为________、_____。
②阴阳两极生成的气体的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.1 mol/L、体积均为V0的HX、HY溶液,分别加水稀释至体积V,pH随![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.常温下,由水电离出的c(H+)·c(OH -):a<b
C.相同温度下,电离常数K( HX):a>b
D.![]() =3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则
=3,若同时微热两种溶液(不考虑HX 、HY和H2O的挥发),则![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法符合事实的是( )
A. 常温下由水电离产生的c(H+)=10-12mol/L的溶液中加入铝粉都能够产生氢气
B. 用0.2000 /L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和
C. 电解硫酸铜溶液一段时间后,加入氧化铜固体不可能使溶液恢复到原来的浓度
D. 在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,开始没有沉淀,随后产生沉淀,最后沉淀消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,A是氯气的发生装置,B、C是净化气体的装置,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置。

(1)上述装置中有一处错误,请指出是______处(用字母表示)。
(2)通过F是为了除去_____________。
(3)写出D中发生反应的化学方程式_______。
(4)如果A中产生氯气3.36L(标准状况) [A中的反应为(MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O)]。请计算:。
MnCl2+Cl2↑+2H2O)]。请计算:。
①消耗MnO2的物质的量__________。②被氧化的HCl的物质的量____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应的平衡常数表达式为K=[c(CO2)·c(H2)] /[c(CO)·c(H2O)],在不同的温度下该反应的平衡常数值分别为:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述错误的是
A. 该反应的化学方程式是:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B. 上述反应的正反应是放热反应
C. 如果在1L的密闭容器中加入CO2和H2各1mol,再把温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态
D. 若平衡浓度关系符合c(CO2)/3c(CO)=c(H2O)/5c(H2),可判断此时温度是1000℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下:
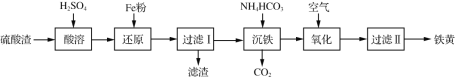
下列说法不正确的是
A. “酸溶”中加热或搅拌或适当增大硫酸浓度均可加快溶解速度
B. 滤渣的主要成分是SiO2和Fe
C. “沉铁”过程中生成Fe(OH)2的化学方程式为: FeSO4+2NH4HCO3===Fe(OH)2↓+ (NH4)2SO4+ 2CO2↑。
D. “氧化”Fe(OH)2浆液时,可用氯气代替空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-![]() NH3↑+ H2O
NH3↑+ H2O
B.氧化铁和稀硫酸反应:Fe2O3+6H+=2Fe2++3H2O
C.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
D.石灰石与硝酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com