
【题目】火箭的燃料之一是铝粉与高氯酸铵(NH4ClO4)的固体混合物,点燃时,铝粉被氧化。放热引发高氯酸铵反应:2NH4ClO4═N2↑+4H2O+Cl2↑+2O2↑,反应放出大量热。
(1)该反应中被氧化的元素是___和___;
(2)氧化产物与还原产物的质量之比为___;
(3)该反应中若生成标况下2.24LCl2时,电子转移数为___;
(4)若生成的水在高温下也为气态,则混合气体的平均摩尔质量为__g/mol(小数点后保留一位)。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,易溶于水,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:___。
【答案】N O 92:71 1.4NA 29.4 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
【解析】
该反应中相关元素的化合价为:![]() ,反应过程中,N、O元素化合价升高,Cl元素化合价降低,
,反应过程中,N、O元素化合价升高,Cl元素化合价降低,
(1)该反应中,N、O元素化合价升高,因此被氧化的元素为N、O,
故答案为:N;O;
(2)由方程式可知,氧化产物为N2和O2,还原产物为Cl2,有2mol NH4ClO4发生反应时,生成的氧化产物为1mol N2和2molO2,还原产物1molCl2,故氧化产物与还原产物的质量之比为(1mol×28g/mol+2mol×32g/mol):(1mol×71g/mol)=92:71,
故答案为:92:71;
(3)该反应进行过程中,Cl元素化合价从+7价降低为0价,反应每生成1mol Cl2,转移电子(+7-0)×2mol=14mol,因此若生成标况下2.24LCl2,即0.1mol Cl2时,转移电子数为1.4mol×NAmol-1=1.4NA,
故答案为1.4NA;
(4)若生成的水在高温下也为气态,则混合气体的平均摩尔质量为= 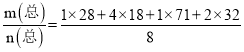 g/mol=29.4g/mol,
g/mol=29.4g/mol,
故答案为:29.4;
(5)由题干可知,反应后Fe元素化合价从+3价升高至+6价,变化3价,Cl元素从+1价降低至-1价,变化2价,根据氧化还原化合价升降守恒可知,Fe3+的系数为2,ClO-的系数为3,根据电荷守恒以及溶液为强碱性可配平离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O。


科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置
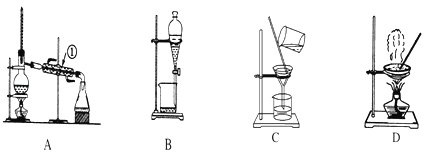
某化学兴趣小组利用以上装置,按以下实验方案,采取步骤(1)(2)(3)(4)等四步操作从海洋动物中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)
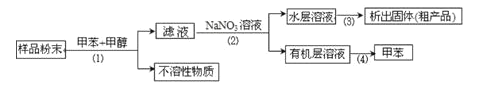
(1)装置A中仪器①的作用是________,使用装置A在流程中所对应的是________(填“操作(1)”“操作(2)”“操作(3)”或“操作(4)”,下同)。
(2)使用装置B在流程中所对应的是________在该操作中,振荡仪器时,为了避免因液体挥发而导致内部气压过大,还应进行的操作是________(填写具体的操作方法)。
(3)使用装置C在流程中所对应的是________,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________。
(4)使用装置D在流程中所对应的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。钛酸钡晶体的晶胞结构示意图如图所示,它的化学式是

A. BaTi8O12
B. BaTiO3
C. BaTi2O4
D. BaTi4O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表诞生150周年,目前周期表七个周期均已排满,共118种元素。短周期元素W、X、Y、Z在周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。
下列说法不正确的是
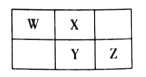
A. 最高价氧化物对应水化物的酸性:Z>Y
B. W的氢化物与Z的氢化物反应,产物的水溶液呈碱性
C. 在元素周期表中,117号元素与Z元素位于同一主族
D. 工业上常用YX2漂白纸浆、毛、丝等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子外围电子排布式:_______________________________。F的离子电子排布式:__________。
(2)写出X涉及化工生产中的一个化学方程式:______________________。
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:_____________。
(4)CE、FA的晶格能分别为786 kJ·mol-1、3 401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是___________________________。
(5)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为________________;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是____________________(只要求列出算式)。
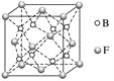
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通过称量![]() 样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是( )
样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是( )
A. 实验前试样未经干燥B. 试样中含有少量碳酸氢铵
C. 试样中含有少量氯化钠D. 加热过程中有试样迸溅出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L某一元酸(HA)溶液中![]() =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A. 溶液中水电离出的c(H+)=10-10 mol/L
B. 溶液中c(H+)+c(A-)=0.1 mol/L
C. 溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D. 与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
具有抗菌作用的白头翁衍生物H的合成路线如图所示:
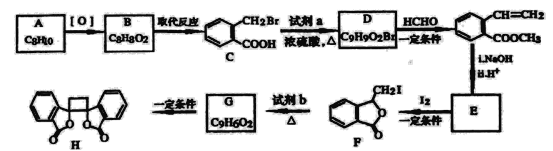
已知:
Ⅰ:R′CH2Br![]() R′HC=CH-R
R′HC=CH-R
Ⅱ: ![]()
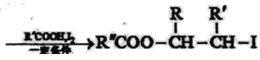
(1)A属于芳香烃,其名称是___________。
(2)写出符合下列条件的B的一种同分异构体:①苯环上只有一个取代基,②能发生银镜反应,③能发生水解反应,该物质的结构简式为___________。
(3)由C生成D的化学方程式是___________。
(4)由G生成H的反应类型是_________,1mol F与足量NaOH溶液反应,消耗__________mol NaOH。
(5)试剂b是_________。
(6)下列说法正确的是________(选填宇母序号)
a G存在顺反异构体
b l mol G最多可以与1mol H2发生加成反应
c l mol H与足量NaOH溶液反应,消耗2mol NaOH
(7)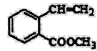 满足下面条件的同分异构体共有________种。
满足下面条件的同分异构体共有________种。
①含有苯环 ②含有2个-CHO ③苯环上有两个取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,pH=2的两种一元酸x和y,体积均为100mL,稀释过程中pH与溶液体积的关系如图所示。分别滴加NaOH溶液至滴定终点,消耗NaOH溶液的体积为Vx、Vy,则

A.x为弱酸,Vx<VyB.x为强酸,Vx>Vy
C.y为弱酸,Vx<VyD.y为强酸,Vx>Vy
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com