
【题目】粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:

经操作I得到粗胆矾,操作III得到精制胆矾。两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。
已知:![]() 、
、![]() 、
、![]() 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
|
|
| |
开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
(1)溶解、过滤需要用到玻璃棒,它的作用是________。
(2)写出加入3% H2O2后发生反应的离子方程式_______。(原溶液显酸性)。
(3)加稀氨水调节pH应调至范围______。下列物质可用来替代稀氨水的是___。(填字母)
A.NaOH B.Cu(OH)2C.CuO D.NaHCO3
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、________________。
(5)某学生用操作III所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
第一次实验 | 第二次实验 | |
坩埚质量(g) | 14.520 | 14.670 |
坩埚质量 | 17.020 | 18.350 |
第一次加热、冷却称量(g) | 16.070 | 16.989 |
第二次加热、冷却、称量(g) | 16.070 | 16.988 |
两次都无须再做第三次加热、冷却、称量,理由是______,该生此次实验的相对误差为__%(保留1位小数),产生实验误差的原因可能是___(填字母)。
A.加热前称量时坩埚未完全干燥 B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却 D.玻璃棒上沾有的固体未刮入坩埚
【答案】搅拌、引流 2Fe2++H2O2+2H+=2Fe3++2H2O 3.7~5.2 BC (NH4)2SO4或NH4HSO4 已达恒重 +4.2% AD
【解析】
由流程图可知,粗氧化铜中加入硫酸溶解,得到硫酸铜、硫酸铁以及硫酸亚铁的混合液以及不溶杂质,过滤,得到含有铜离子、铁离子以及亚铁离子的水溶液,向其中加入双氧水,可以将亚铁离子氧化为铁离子,加稀氨水调节pH,让铁离子全部沉淀,过滤得到的滤液是硫酸铜溶液,加入硫酸蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可以得到胆矾晶体。
(1)溶解、过滤需要用到玻璃棒,它的作用是搅拌、引流,故答案为:搅拌、引流;
(2)由于亚铁离子沉淀的pH较大,所以必须将其氧化成铁离子沉淀,因此加入双氧水的目的是氧化亚铁离子,反应的离子方程式为2Fe2++ H2O2+ 2H+= 2Fe3+ +2H2O,故答案为:2Fe2++ H2O2+ 2H+= 2Fe3+ +2H2O;
(3)要得到胆矾,就必须除去溶液中的铁离子,则根据沉淀时的pH值可知,调节溶液pH的目的是使Fe3+完全转变成Fe(OH)3沉淀;铁离子完全沉淀时的pH=3.7,而铜离子开始沉淀时的pH=5.2,所以溶液的pH应调节到3.7~5.2之间,由于在调节pH的同时,不能引入杂质,因此应该选择氧化铜或氢氧化铜来调节溶液的pH,故答案为:3.7~5.2;BC;
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、(NH4)2SO4或NH4HSO4,故答案为:(NH4)2SO4或NH4HSO4;
(5)根据表中的数据两次实验都已达恒重,故没必要再进行第三称量;由表格数据可知坩埚质量为![]() =14.595g,实验1所得晶体质量为(17.02-14.595)g=2.425g,水的质量为(17.02-16.07)g=0.95g,水的质量分数为
=14.595g,实验1所得晶体质量为(17.02-14.595)g=2.425g,水的质量为(17.02-16.07)g=0.95g,水的质量分数为![]() =0.3917,实验2所得晶体质量为(18.35-14.595)g=3.755g,水的质量为(18.35-16.99)g=1.36g,水的质量分数为
=0.3917,实验2所得晶体质量为(18.35-14.595)g=3.755g,水的质量为(18.35-16.99)g=1.36g,水的质量分数为![]() =0.3622,两次平均水的质量分数
=0.3622,两次平均水的质量分数![]() =0.3769,五水硫酸铜中水的理论质量数为0.36,相对误差
=0.3769,五水硫酸铜中水的理论质量数为0.36,相对误差![]() =0.042;由计算可知产生实验误差是偏大,即水的质量较多或剩余固体的质量较少,其原因可能是
=0.042;由计算可知产生实验误差是偏大,即水的质量较多或剩余固体的质量较少,其原因可能是
A.加热前称量时坩埚未完全干燥有了多余的水,故正确;
B.该胆矾中含有受热不分解的杂质会使结果偏低,故错误;
C.加热后坩埚放在干燥器中冷却,不会带来误差,故错误;
D.玻璃棒上沾有的固体未刮入坩埚,有一部分固体没有得到称量,相当于剩余的固体质量减小,故正确;
AD正确,故答案为:已达恒重;+4.2%;AD。


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】由氯苯制取1,2,3,4一四氯己烷,步骤如下
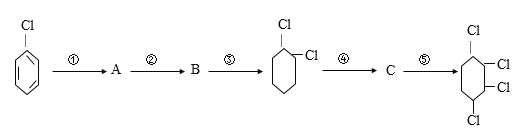
(1)填写每步所属的反应类型(a.取代反应b.加成反应 c.消去反应,只需填写字母):①_________、②____________、③___________、④________、⑤__________
(2)反应②所需要的试剂和条件是_________________________;
(3)反应④⑤的化学方程式是④______________⑤________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等.
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取.高温下制取纯硅有如下反应(方法Ⅰ):
①SiO2(s)+2C(s)Si(s)+2CO(g)
②Si(s)+2Cl2(g)SiCl4(g)
③SiCl4(g)+2H2(g)→Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有______ 种不同能级的电子,最外层p电子有______种自旋方向;SiO2晶体中每个硅原子与______个氧原子直接相连.
(2)单质的还原性:碳______硅(填写“同于”、“强于”或“弱于”).从平衡的视角而言,反应①能进行的原因是______.
(3)反应②生成的化合物分子空间构型为;该分子为______分子(填写“极性”或“非极性”).
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L.然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L.则:a______b(填写“大于”、“等于”或“小于”).
(5)在t秒内,反应②中反应速率v(SiCl4)=______(用含a、b的代数式表示).
(6)工业上还可以通过如下反应制取纯硅(方法Ⅱ):
④Si(粗)+3HCl(g)![]() SiHCl3(l)+H2(g)+Q(Q>0)
SiHCl3(l)+H2(g)+Q(Q>0)
⑤SiHCl3(g)+H2(g)![]() Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
提高反应⑤中Si(纯)的产率,可采取的措施有:______、______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,CH3COOH的电离常数Ka=1.8×10-5。常温下,往25mL氢氧化钠标准溶液中逐滴加入0.1mol·L-1的CH3COOH溶液,pH变化曲线如图所示:
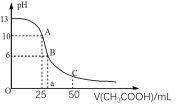
(1)该氢氧化钠溶液的物质的量浓度为__。
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:__。
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:______。
(4)B点所示溶液中,![]() =___。
=___。
(5)C点所示溶液为等浓度的CH3COONa和CH3COOH混合溶液,请判断该溶液中c(CH3COOH)__c(CH3COO-)。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
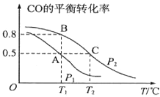
①A、B两点对应的压强大小关系是PA___PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是___。
③下列叙述能说明上述反应能达到化学平衡状态的是___(填代号)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=___。
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___v(逆)(填“>、<或=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干电池是日常生活中常用的电池,原料为Zn和MnO2。某工厂用软锰矿(含MnO2约70%及杂质Al2O3)和闪锌矿(含ZnS约80%及少量FeS杂质)共同生产。流程如下:

已知:①A是ZnSO4、MnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②Ⅳ中反应的方程式为:MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。
(1)混合物A中,属于还原产物的是______(填化学式)。
(2)加入X的作用是_____________________。已知溶液中各离子开始沉淀的pH如表所示,则加入X后,溶液pH应调整到_____(填字母)。
A.4.5 B.8.0 C.6.5 D.9.0
离子 | 开始沉淀pH | 完全沉淀pH |
Fe3+ | 2.3 | 3.2 |
Al3+ | 4.2 | 5.4 |
Zn2+ | 7.2 | 8.0 |
Mn2+ | 8.3 | 9.8 |
步骤Ⅱ加热的原因是____________________。适宜作为X加入步骤Ⅱ的物质为______(填字母)。
A.MnCO3 B.Zn2(OH)2CO3 C.NaOH D.KOH
(3)生产过程中除矿石外,还有哪些原料需要购买?____________(填化学式)。
(4)若要从步骤Ⅳ的过滤中得到芒硝晶体(Na2SO4·10H2O),则需要进行的实验操作有________、________、过滤、洗涤、干燥等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】40℃硝酸钾饱和溶液先升温至80℃,在恒温下蒸发部分溶剂至析出少量溶质,然后将溶液逐渐冷却至60℃.下列示意图中能正确表示整个过程中溶液浓度a%与时间t关系的是( )
A.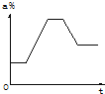 B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M的结构简式如图所示,与氢气发生加成反应得到物质甲,下列有关说法不正确的是

A.有机物M含有2种官能团
B.有机物M的分子式为C4H6O2
C.有机物M能发生取代反应、加聚反应
D.甲只含有一种官能团的链状同分异构体(不含甲本身)有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、Q原子序数依次增大,Y元素最外层电子数是其电子层数的3倍,Q与Y同主族,X与Y构成的化合物可引起光化学烟雾,Z、W、Q的最高价氧化物的水化物两两之间均能发生反应。下列说法正确的是( )
A.简单氢化物的沸点:Y<QB.W的氧化物可作耐高温材料
C.简单离子半径最大的为ZD.气态氢化物的稳定性:Y<X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com