
【题目】40℃硝酸钾饱和溶液先升温至80℃,在恒温下蒸发部分溶剂至析出少量溶质,然后将溶液逐渐冷却至60℃.下列示意图中能正确表示整个过程中溶液浓度a%与时间t关系的是( )
A.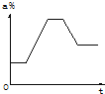 B.
B. C.
C. D.
D.
【答案】A
【解析】
试题分析:①将40℃时硝酸钾的饱和溶液先升温至80℃,温度升高,硝酸钾的溶解度增大,溶质和溶剂的质量都没有发生变化,所以此过程中溶液的浓度不变;②在80℃且恒温下蒸发部分溶剂至析出少量溶质前,该过程中溶剂不断减少,溶质的质量不变,所以溶液的浓度会不断增大;③80℃的温度下,当析出晶体时达到饱和,之后的溶液为硝酸钾饱和溶液,所以硝酸钾的溶液的浓度暂时不变;④最后将溶液由80℃逐渐冷却至60℃过程中,随着温度降低,硝酸钾的溶解度减小,此过程中会不断析出硝酸钾晶体,而溶剂的质量不变,则溶液的浓度逐渐减小;⑤温度降到60℃后,此时的溶液为硝酸钾饱和溶液,溶液的浓度不再变化,根据以上分析可知,满足以上变化的图象为A,故选A。


科目:高中化学 来源: 题型:
【题目】
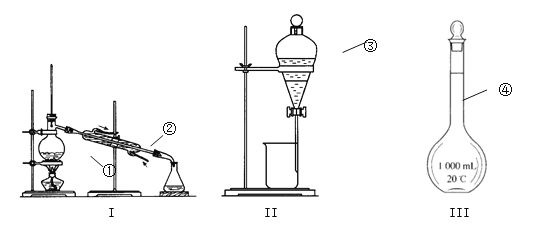
① ;② ;③ ;④ ;
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(3)若用四氯化碳萃取碘水中的碘,振荡静置如图Ⅱ,可观察到液体分层,上层为 层(填“H2O”或“CCl4”);下层呈 色。分液后再用装置Ⅰ进行分离的方法称作 ,在加热前,①中要加入少量碎瓷片,目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3·l0H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。
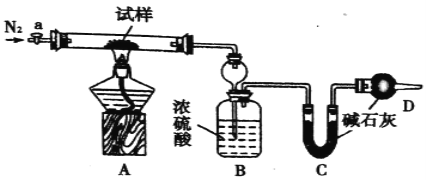
实验过程:
I.按图组装仪器,检查装置的气密性;
II.将m1 g试样放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3 g;
Ⅲ.关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为:________________;_______________。
(2)装置B的作用为_______________。装置C的作用为_______________。
(3)实验过程中通入N2的目的为__________。
(4)实验结束后发现装置A中硬质玻璃管右端有水珠,则w(NaHCO3)的计算式为:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业上从废铅酸电池的铅膏回收铅的过程中,可用碳酸盐溶液与铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)![]() PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K= 。
(2)室温时,向两份相同的样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在 溶液中PbSO4转化率较大,理由是 。
Ⅱ.Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3 (s)![]() Cr3+(aq)+3OH(aq)。
Cr3+(aq)+3OH(aq)。
常温下,Cr(OH)3的溶度积Ksp=1.0×1032,要使c(Cr3+)完全沉淀,溶液的pH应调至 。
Ⅲ.向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。溶度积为Ksp=c(Ag+)·c(Cl-)=1×10-10,试求:
(1)沉淀生成后溶液中c(Ag+)为________。
(2)沉淀生成后溶液的pH是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知N2(g) +3H2(g)![]() 2NH3(g) △H=-92.3kJ·mol-1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,达到平衡状态II,则下列说法正确的是________
2NH3(g) △H=-92.3kJ·mol-1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,达到平衡状态II,则下列说法正确的是________
A.两个平衡状态的平衡常数的关系:KI <KII
B.H2的百分含量相同
C.N2的转化率:平衡I <平衡II
D.反应放出的热量:QI=QII< 92.3 kJ
(2)若相同条件下,向第三个体积相同的密闭容器中充入一定量的N2、H2和NH3,要求反应从逆反应开始达到平衡,且平衡时氢气的体积分数仍为50%,则加入的氨气的物质的量的范围是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有A+、B3+、C3+ 三种金属阳离子的水溶液发生了如下一系列变化:
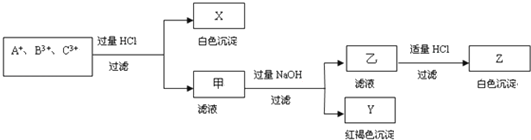
请通过分析回答(用化学符号填写):
(1)A+是______,B3+是____________,C3+是____________;
(2)X是____________,Y是____________,Z是____________;
(3)写出有关离子方程式:
①生成Y沉淀:_______________________;
②生成Z沉淀:_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活、社会可持续发展密切相关。下列说法不正确的是( )
A.光化学烟雾是氮氧化物受紫外线照射后与空气中的一些碳氢化合物作用后生成的一种有毒烟雾
B.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.航天飞机上使用的隔热陶瓷瓦,大多是以碳纤维做增强体的新型复合材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
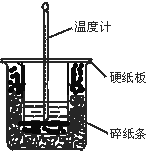
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验改用60 mL 0.50 mol· L-1盐酸跟50 mL 0.55 mol· L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com