
【题目】下列离子方程式的书写正确的是( )
A.大理石与盐酸反应:CO32﹣+2H+=CO2↑+H2O
B.铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag
C.氯气溶于水:Cl2+H2O═2H++Cl﹣+ClO﹣
D.硫酸与氢氧化钡溶液反应:2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关浓硫酸、浓盐酸、浓硝酸的认识不正确的是
A.浓硫酸、浓硝酸与金属反应时,分别是S、N得电子
B.蔗糖与浓硫酸混合后,白色蔗糖固体逐渐变成黑色疏松的碳,体现了浓硫酸的脱水性
C.浓盐酸、浓硝酸具有挥发性,而浓硫酸难挥发
D.常温下,浓硫酸或浓HNO3中投入Fe片,均会产生大量的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义。
(1)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0
N2(g)+2CO2(g) ΔH<0
①一定条件下,将体积比为1∶2的NO、CO气体置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___(填字母)。
A.体系压强保持不变 B.混合气体颜色保持不变
C.N2和CO2的体积比保持不变 D.v正(CO)=2v逆(N2)
②20min时,若改变反应条件,导致N2浓度发生如下图所示的变化,则改变的条件可能是______(填字母)。
A.加入催化剂 B.降低温度 C.增加CO2的量 D.缩小容器体积

(2)在一定条件下,将SO2和NO2通入绝热恒容密闭容器中,发生反应:SO2(g)+NO2(g) ![]() SO3(g) +NO(g),正反应速率随时间变化如图所示。由图可得出的正确结论是__(填字母)
SO3(g) +NO(g),正反应速率随时间变化如图所示。由图可得出的正确结论是__(填字母)

A.反应在c点达到平衡状态
B.反应物浓度:b点小于c点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2时,SO2的转化率:a~b段小于b~c段
(3)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2可制备二甲醚(DME)。观察图回答问题。

催化剂中n(Mn)/n(Cu)约为__________时最有利于二甲醚的合成。
(4)工业上可以用CO和H2生产燃料甲醇:CO(g)+2H2(g)![]() CH3OH(g)ΔH=-92.9kJ/mol,300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
CH3OH(g)ΔH=-92.9kJ/mol,300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
平衡 时的 数据 | CH3OH浓度/mol·L-1 | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收c kJ | ||
体系压强/Pa | p1 | p2 | p3 | |
反应物转化率 | α1 | α2 | α3 | |
下列说法中正确的是____________
A.2c1>c3 B.a+b=92.9 C.2p2<p3 D.α1+α3<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体中可能含有Na+、K+、Mg2+、Ba2+、 SO42-、CO32-、SO32-、SiO32-等离子,将其配成100mL溶液。学生研究性学习小组为了确认其成分,设计并完成了如图所示实验:

请回答下列问题:
(1)实验中最关键的“定容”操作:当液面接近容量瓶刻度线1-2cm处,________再将容量瓶塞盖好,反复上下颠倒,摇匀。
(2)根据以上实验可得出:一定存在的离子是________,一定不存在的离子是________
(3)下列实验结论符合事实的是________________
A.该固体中可能含有Na2SiO3、K2CO3
B.该固体中一定含有Na2SiO3、K2CO3
C.该固体中可能含有Na2SiO3、K2CO3、K2SO4
D.该固体中可能只含有Na2SiO3、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的热现象说法不正确的是( )
①放热反应发生时不必加热 ②化学反应一定有能量变化
③吸热反应需要加热后才能发生
④化学反应吸收或放出热量的多少与参加反应的物质多少有关
A.①②B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“即食即热型快餐”适合外出时使用,其内层是用铝箔包裹并已加工好的真包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线使这两种化学物质发生反应,放出的热量便可对食物进行加热,这两包化学物质最适合的选择是
A.浓硫酸和水B.生石灰和水C.熟石灰和水D.氯化钠和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.标准状况下,22.4L H2中所含质子数、中子数均为2NA
B.32g O2气体和32g O3气体的原子数之比为3:2
C.1L 1molL﹣1的盐酸中所含粒子总数为2NA
D.71g氯气与足量铁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
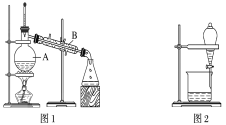
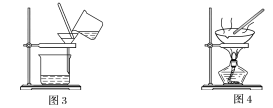
(1)装置图1中B的名称是________________,图2中漏斗的名称是________________。A中一般要加入碎瓷片,其作用是__________________________。下列关于以上实验操作说法一定正确的是_。
A.图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B.图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C.图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D.图4实验中,当加热至有较多固体析出时,即停止加热
(2)现有一瓶A和B的混合液,已知它们的性质如下表。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水和酒精 |
B | 17.9 | 290 | 1.26 |
据此分析,将A和B相互分离可选用上图中的图________________所示仪器。
(3)在图2所示实验中,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性的透明溶液中,下列离子组能够大量共存的是( )
A.Na+、K+、OH-、Cl-B.Mg2+、Cu2+、SO42-、Cl-
C.K+、Ba2+、Cl-、HCO3-D.NH4+、Ba2+、Fe3+、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com