
【题目】下列解释实验事实的化学方程式正确的是
A. FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
B. 90℃时,测得纯水中c(H+)·c(OH-)=3.8 ×10-13:H2O(l)![]() H+(aq)+OH-(aq)△H<0
H+(aq)+OH-(aq)△H<0
C. 氨水中滴入酚酞溶液.溶液变红:NH3·H2O=NH4++OH-
D. 向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700—900℃时,O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是
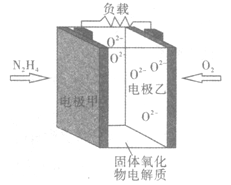
A. 电池总反应为N2H4+2O2=2NO+2H2O
B. 电池内的O2-由电极乙移向电极甲
C. 电极乙上反应的电极方程式为:O2+2e-=O2-
D. 电池外电路的电子由电极乙移向电极甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所涉及的物质均为中学化学中的常见物质,其中C、D均为气体单质,E是固体单质,A物质的焰色反应火焰为紫色,F是黑色晶体,它们存在如图转化关系,反应中生成的水及次要产物均的已略去。

(1)写出下列物质的化学式:C_____________,D______________,H____________。
(2)指出MnO2在相关反应中的作用:反应①中做_______剂,反应②中做_________剂。
(3)当①中有1molA完全反应时转移电子的物质的量是________mol。
(4)检验G中阳离子的方法_________________________________________ 。
(5)保存G溶液时为什么要加固体E_____________________________________。
(6)写出F→G+H的离子方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列颜色变化与氧化还原反应无关的是( )
A. FeCl3溶液滴入Mg(OH)2浊液,白色浊液转化为红褐色沉淀
B. AgNO3溶液滴入氯水中,产生白色沉淀,随后淡黄色褪去
C. Na放在坩埚里并加热,发生黄色火焰,生成淡黄色固体
D. H2C2O4溶液滴入KMnO4酸性溶液中,产生气泡,随后紫色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.蛋白质溶液属于胶体,能透过滤纸.
B.在水溶液中或熔融状态下能导电的物质是电解质
C.能电离出氢离子的化合物是酸
D.胶体带电荷,所以会产生电泳现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O5是常用的防腐剂和漂白剂。可利用烟道气中的SO2生产Na2S2O5,其流程如下:

下列说法正确的是( )
A. 上述流程中的Na2CO3饱和溶液和Na2CO3固体不可互换
B. Na2S2O5作防腐剂和SO2作漂白剂时,均表现还原性
C. 上述制备过程所涉及的物质中只有一种酸性氧化物
D. 实验室模拟“结晶脱水”时用到的仪器只有蒸发皿、玻璃棒、烧杯、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
(1)写出下图中仪器的名称:a.____,b.____。
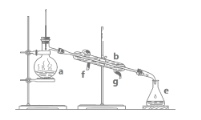
(2)若利用上图装置分离四氯化碳和酒精的混合物,还缺少的仪器是_______,将仪器补充完整后进行实验,温度计水银球的位置在_______处。冷凝水由____口流出(填f或g)。
(3)现需配制0.1mol/L NaOH溶液450mL,下图是某同学转移溶液的示意图。

①图中的错误是__________。
②根据计算得知,需称量NaOH的质量为_____。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)____。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
④若实验遇下列情况,溶液的浓度是偏大、偏小还是无影响.
A.溶解后没有冷却便进行定容__________________;
B.摇匀后发现液面低于标线,滴加蒸馏水至标线再摇匀___________________;
C.定容时俯视容量瓶的标线___________________;
D.容量瓶内壁附有水珠而未干燥处理___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,Na+物质的量浓度最大的是( )
A. 4 L、0.5 mol·L-1NaCl溶液 B. 1 L、0.3 mol·L-1Na2SO4溶液
C. 5 L、0.4 mol·L-1NaOH溶液 D. 2 L、0.15 mol·L-1、Na3PO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com