
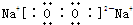 ,
,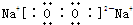 ;
;

科目:高中化学 来源: 题型:
| A、反应速率B>A |
| B、SO2的转化率B>A |
| C、平衡时SO2的百分含量B>A |
| D、平衡时容器的压强B>A |
查看答案和解析>>
科目:高中化学 来源: 题型:
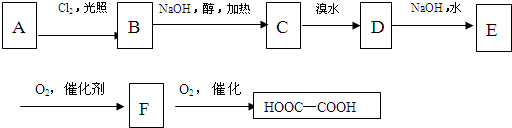
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醛 | B、丁醛 | C、戊醛 | D、已醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、b、a、e、d、c |
| B、e、d、a、b、c |
| C、a、b、d、c、e |
| D、c、d、e、a、b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(OH-)=c(H+) |
| D、pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(NaOH )>c(CH3COONa)>c(Na2CO3)>c(C6H5ONa ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
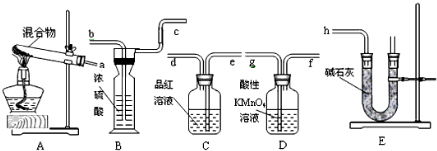
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com