
����Ŀ����һ�������ȵ��ܱշ�Ӧ���У�ֻ����������Ӧ:
A(g)+B(g)![]() 2C(g)����H1<0��
2C(g)����H1<0��
X(g)+3Y(g)![]() 2Z(g)����H2>0��
2Z(g)����H2>0��
������ز����Ҵﵽ��ѧƽ���(��������ı������Ĺ�)�����������������
A. ��ѹʱ��ͨ��������壬C�����ʵ�������
B. ��ѹʱ��ͨ��Z���壬��Ӧ�����¶�����
C. ����ʱ��ͨ��������壬����Ӧ���ʲ���
D. ����ʱ��ͨ��Z���壬Y�����ʵ���Ũ������
���𰸡�A
��������
���������A������ʱ��ͨ��������壬����Ӧ������Ũ�Ȳ��䣬����Ӧ���ʲ��䣬��ȷ��B������ʱ��ͨ��z���壬�ڶ���Ӧƽ�����淴Ӧ�ƶ���y�����ʵ���Ũ��������ȷ��C����ѹʱ��ͨ��z���壬�ڶ���Ӧƽ�����淴Ӧ�ƶ����¶����ߣ����µ�һ����Ӧ���淴Ӧ�ƶ������ƶ��������ָ���ԭ�¶ȣ���ƽ��ʱ�¶����ߣ���ȷ��D����ѹʱ��ͨ��������壬������ڶ�����Ӧƽ�����淴Ӧ�ƶ����¶����ߣ����µ�һ����Ӧ���淴Ӧ�ƶ���c�����ʵ�����С������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�������SOCl2��������ҽҩ��ũҩ��Ⱦ�Ϲ�ҵ��Ҳ�����л��ϳɹ�ҵ�����Ȼ�������֪��SOCl2������������±���ʾ��
��ɫ��״̬ | �۵� | �е� | ��ʴ�� | ˮ�� |
��ɫ����Һ�� | -105�� | 78�� | ǿ | ����ˮ�� |
��������ͼװ���Ʊ�SOCl2��
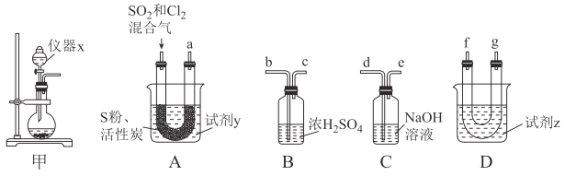
��ش��������⣺
���Ʊ�SO2��Cl2��
��1����ʵ��ѡ��װ�ü��Ʊ�SO2��Cl2��װ�ü�������x������Ϊ___������KMnO4��Ũ���ᷴӦ�Ʊ�Cl2����Ӧ�����ӷ���ʽΪ___��
���Ʊ�SOCl2��
�Ի���̿��Ϊ������SO2��C12���Ժ�S����180~200��ʱ��Ӧ�ϳ�SOCl2��ѡ��װ��A��B��C��D�����Ʊ����г֡�����װ����ȥ����
��2�������������ҵķ���װ��A��B��C��D������˳��Ϊ___���������ӿڵ���ĸ��ţ���
��3���Լ�yΪ___����ѡ����ĸ����ͬ�����Լ�zΪ___��
A����ˮ B���Ҵ� C��ʯ���� D����ˮ
��4��װ��A��U�ι��ڷ�����Ӧ�Ļ�ѧ����ʽΪ___��
��5��װ��C������Ϊ___����װ��A��ͨ���SO2��Cl2�����ʵ���֮��Ϊ1��3����װ��C�����ɵ���Ϊ___���ѧʽ���������ʵ����֤װ��C�����ɵ����к���SO42-��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ������У���H2��COֱ���Ʊ������ѣ�CH3OCH3��������̰������·�Ӧ��
i.CO(g)+2H2(g)![]() CH3OH(g) H1=90.1kJ��mol1
CH3OH(g) H1=90.1kJ��mol1
ii.2CH3OH(g)![]() CH3OCH3(g)+H2O(g) H2=24.5kJ��mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ��mol1
������������ͬʱ����H2��COֱ���Ʊ������ѵķ�Ӧ�У�COƽ��ת����������X ���仯��������ͼ��ʾ������˵����ȷ����
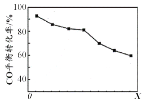
A . ��H2��COֱ���Ʊ������ѵķ�ӦΪ���ȷ�Ӧ
B. ����XΪѹǿ
C. X�������ѵIJ���һ������
D. X���÷�Ӧ��ƽ�ⳣ��һ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������I���б�����˿���Ĺ��ܣ��ɹ㷺���ڱ��滯ѧ������ҽѧ�����̡��ջ���Ʒ��������ϳ�·����ͼ��
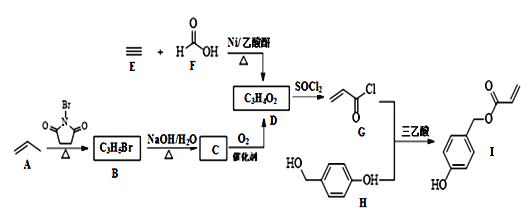
�ش��������⣺
��1��I�к��������ŵ�����Ϊ____��
��2����B����C�Ļ�ѧ����ʽΪ__��
��3����E��F��Ӧ����D�ķ�Ӧ����Ϊ____����G��H��Ӧ����I�ķ�Ӧ����Ϊ____��
��4������DΪ����ϳɸ߷��ӻ�����Ļ�ѧ����ʽΪ___��
��5��X��I�ķ���ͬ���칹�壬�ܷ���������Ӧ�����뱥��̼��������Һ��Ӧ�ų�CO2����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1��д�����ַ���Ҫ���X�Ľṹ��ʽ___��
��6�����ձ�����Ϣ����д����1��ϩΪԭ����ȡ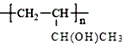 �ĺϳ�·������ͼ����ԭ����ѡ��___��
�ĺϳ�·������ͼ����ԭ����ѡ��___��
�ϳ�·������ͼʾ����ͼ��H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��FeCl3��Һ�е�����ƽ������ӷ�Ӧ��ijС��ͬѧ����������ʵ�顣
��1������50 mL 1.0 mol��L1��FeCl3��Һ������pHԼΪ0.7����c(H+) = 0.2 mol��L1��
�� �û�ѧ�������FeCl3��Һ�����Ե�ԭ�� ��
�� ����ʵ�鷽���У���ʹFeCl3��ҺpH���ߵ��� ������ĸ��ţ���
a. ��ˮϡ�� b. ����FeCl3����
c. �μ�ŨKSCN��Һ d. ����NaHCO3����
��2��С��ͬѧ��������FeCl3��Һ̽����������п�۵ķ�Ӧ��ʵ��������������£�
���� | ���� |
��Ӧƿ�м���6.5 gп�ۣ�Ȼ�����50 mL 1.0 mol��L1��FeCl3��Һ������ | ��Һ�¶�Ѹ���������Ժ���ֺ��ɫ������ͬʱ�����������ݣ���Ӧһ��ʱ����ã��ϲ���ҺΪdz��ɫ����Ӧƿ�ײ��к�ɫ���� |
�ռ����鷴Ӧ�����в��������� | �����ܿڿ������棬�б����� |
��֪��Zn��������Al���ƣ��ܷ�����Ӧ��Zn + 2NaOH = Na2ZnO2 + H2 ��
�� ���ʵ�������ƽ���ƶ�ԭ�����ͳ��ֺ��ɫ������ԭ�� ��
�� �����ӷ���ʽ���ͷ�Ӧ����ҺΪdz��ɫ��ԭ�� ��
�� �������ɫ���壬������ʵ��֤ʵ�����к��е���Ҫ���ʡ�
i. ��ɫ������Ա�����������
ii. ���ɫ�����м���������NaOH��Һ���������ݣ�
iii. ��ii��ʣ�����������ˮϴ�Ӻ���ϡ���ᣬ�����������ݣ�
iv. ��iii��Ӧ�����Һ�еμ�KSCN��Һ���ޱ仯��
a. ��ɫ������һ�����е������� ��
b. С��ͬѧ��Ϊ����ʵ����ȷ����ɫ�������Ƿ���Fe3O4�������� ��
��3��Ϊ��һ��̽������1.0 mol��L1 FeCl3��Һ��Fe3+��H+�����Ե����ǿ��������ʵ�鲢�۲쵽��Ӧ��ʼʱ�������£�
���� | ���� |
��5 mL 1.0 mol��L1��FeCl3��Һ��0.65 gп�ۻ�� | ��Һ�¶�Ѹ����������ʼʱ����û������ |
�� ��0.65 gп�ۻ�� | ��Һ������������������ |
С��ͬѧ�ó����ۣ���1.0 mol��L1 FeCl3��Һ�У�Fe3+�������Ա�H+��ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����S2����Fe2+��Br����I����0.1mol����Һ��ͨ���״���µ�Cl2��ͨ��Cl2���������Һ��������ӵ����ʵ�����ϵͼ��ȷ���ǣ�������
A.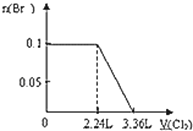 B.
B.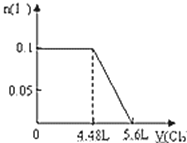
C.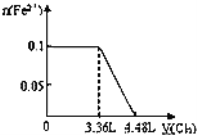 D.
D.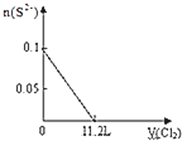
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������������������ȷ����
A. ���³�ѹ�£�11.2L������̼���е�ԭ��������1.5NA
B. 100mL1mol��L-1FeCl3��Һ������Fe3+����ĿΪ0.1NA
C. ��״���£�22.4LCl2ͨ��������ʯ�������Ʊ�Ư�ۣ�ת�Ƶĵ�����Ϊ2NA
D. ���³�ѹ�£�48gO2��O3����ﺬ�е���ԭ����Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2(g)+O2(g)=2NO(g)�������仯��ͼ��ʾ����֪���Ͽ�1mol N2(g)�л�ѧ��������946kJ�������Ͽ�1mol O2(g)�л�ѧ��������498kJ������
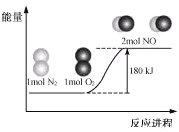
����˵����ȷ����
A. N2(g)+O2(g)=2NO(g) ��H��-180![]()
B. NO(g)=1/2N2(g)+1/2O2(g) ��H��+90![]()
C. �Ͽ�1mol NO(g)�л�ѧ����Ҫ����632kJ����
D. �γ�1 mol NO(g)�л�ѧ�����ͷ�90kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����ijһ��ѧԪ�ء�

���������գ���Ԫ�ط��Ż�ѧʽ����
(1)Ԫ��B��Ԫ�����ڱ��е�λ���ǵ�____���ڵ�_____�壬A��B��C����Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳����_________________��
(2)D�����ӵĽṹʾ��ͼΪ_____________��D��E�н����Խ�ǿ��Ԫ����________��D�����ڿ�����ȼ�տ����ɵ���ɫ��ĩX��D2O2����X������������ߺ�DZˮͧ�еĹ���������ѡ�ú��ʵĻ�ѧ�Լ�����ͼ��ʾʵ��װ��֤��X���ṩ���������á�
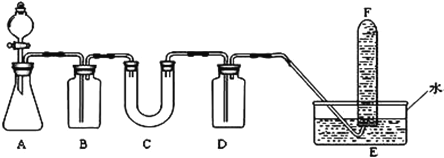
(3)װ��Aʹ��ʯ��ʯ��Ũ���ᷴӦ��ȡCO2��װ��B�б���NaHCO3��Һ�������dz�ȥ_____________��
(4)װ��C��X��CO2��Ӧ�Ļ�ѧ����ʽ��_____________________��װ��Dʢ��NaOH��Һ�������dz�ȥ____________��
(5)Ϊ�����Թ�F�ռ������壬����____________����������_________����֤��X������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com