
����Ŀ��������������ˮ��ɱ����������������ʱ�����һЩ����Ӱ�죬������ǿ�ʼ�о�һЩ��������ˮ��������ijѧϰС��������Ϸ���NCl3����Ϊɱ������������С��������ͼ��ʾ��װ���Ʊ�NCl3 �� ��̽��NCl3��Ư���ԣ�NCl3������������£�
�������� | �Ʊ�ԭ�� | ��ѧ���� |
��ɫ��״Һ�壬�۵�Ϊ��40�棬�е�Ϊ71�棬��������ˮ���������л��ܼ����ܶ�Ϊ1.65g/mL | Cl2��NH4Clˮ��Һ�ڵ����·�Ӧ | 95�汬ը����ˮ�з���ˮ�� |
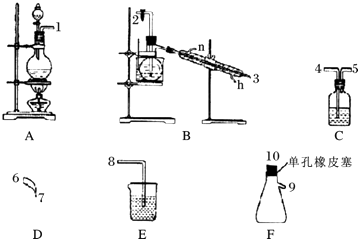
�ش��������⣺
��1������ʵ��Ŀ�ģ��ӿ����ӵ�˳��Ϊ1������2��3��6��7����
��2��Cװ����ʢ�ŵ��Լ�Ϊ����ʳ��ˮ��Eװ����ʢ�ŵ��Լ�Ϊ ��
��3��Aװ���з�����Ӧ�����ӷ���ʽΪ ��
��4��Bװ���з�����Ӧ�Ļ�ѧ����ʽΪ �� ��Bװ��������ƿ�г��ֽ϶���״Һ��رսӿ�2���Ļ���������ˮԡ���ȵ��¶�Ϊ ��
��5����Fװ�õ���ƿ���н϶��ɫ��״Һ�����ʱ���ø���ྻ�IJ�����պȡ��Һ��ε�����ĺ�ɫʯ����ֽ�ϣ���ֽ����ɫ����ȡ��Һ�����50��60����ˮ�У�Ƭ�̺�ȡ����ˮ�ٵε�����ĺ�ɫʯ����ֽ�ϣ���ֽ�ȱ�������ɫ����Ϸ�Ӧ����ʽ�������� ��
���𰸡�
��1��4��5��10��9��8
��2��NaOH��Һ
��3��MnO2+4H++2Cl�� ![]() Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
��4��3Cl2+NH4Cl�TNCl3+4HCl��71��95��
��5��NCl3+3H2O ![]() 3HClO+NH3��NCl3������Ư���ԣ�NCl3����ˮ��ˮ������NH3?H2Oʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ
3HClO+NH3��NCl3������Ư���ԣ�NCl3����ˮ��ˮ������NH3?H2Oʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ
���������⣺��1��Aװ���Ʊ��������Ʊ��������к���HCl��ˮ�������ñ���ʳ��ˮ��ȥHCl��Bװ����Cl2��NH4Clˮ��Һ�ڵ����·�Ӧ�õ�NCl3 �� ���������������ռ�NCl3 �� ���������������Һ����β������ֹ��Ⱦ�������������ӿ����ӵ�˳��Ϊ��1��4��5��2��3��6��7��10��9��8�����Դ��ǣ�4��5 10��9��8����2���������Ȼ��ⶼ�����������Ⱦ������ֱ���ŷţ�����������������Һ���գ�����E��ʢ������������Һ�����Դ��ǣ�NaOH��Һ����3������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ�����ӷ���ʽ��MnO2+4H++2Cl�� ![]() Mn2++Cl2��+2H2O�����Դ��ǣ�MnO2+4H++2Cl��
Mn2++Cl2��+2H2O�����Դ��ǣ�MnO2+4H++2Cl�� ![]() Mn2++Cl2��+2H2O����4��Bװ����Cl2��NH4Clˮ��Һ�ڵ����·�Ӧ�õ�NCl3 �� ������HCl����Ӧ����ʽΪ��3Cl2+NH4Cl�TNCl3+4HCl�����������NCl3 �� NCl3�ķе�Ϊ71�棬��95�汬ը������Ӧ���������¶�Ϊ71��95�棬���Դ��ǣ�3Cl2+NH4Cl�TNCl3+4HCl��71��95�棻3Cl2+NH4Cl�TNCl3+4HCl�� 71��95�棻��5��NCl3������Ư���ԣ���ˮ��Ӧ���ɴ�����Ͱ�������ѧ����ʽ��NCl3+3H2O
Mn2++Cl2��+2H2O����4��Bװ����Cl2��NH4Clˮ��Һ�ڵ����·�Ӧ�õ�NCl3 �� ������HCl����Ӧ����ʽΪ��3Cl2+NH4Cl�TNCl3+4HCl�����������NCl3 �� NCl3�ķе�Ϊ71�棬��95�汬ը������Ӧ���������¶�Ϊ71��95�棬���Դ��ǣ�3Cl2+NH4Cl�TNCl3+4HCl��71��95�棻3Cl2+NH4Cl�TNCl3+4HCl�� 71��95�棻��5��NCl3������Ư���ԣ���ˮ��Ӧ���ɴ�����Ͱ�������ѧ����ʽ��NCl3+3H2O ![]() 3HClO+NH3����������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������������ӣ���Һ�Լ��ԣ�ʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ�� ���Դ��ǣ�NCl3+3H2O
3HClO+NH3����������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������������ӣ���Һ�Լ��ԣ�ʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ�� ���Դ��ǣ�NCl3+3H2O ![]() 3HClO+NH3��NCl3������Ư���ԣ�NCl3����ˮ��ˮ������NH3H2Oʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ��
3HClO+NH3��NCl3������Ư���ԣ�NCl3����ˮ��ˮ������NH3H2Oʹ��ɫʯ����ֽ���������ɵ�HClO��ʹ��Ư����ɫ��
�����㾫����������Ĺؼ���������������ʵ�����Ʒ������֪ʶ������ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ˮ�е���ķ���ʽ��ȷ����
A. NaHCO3=Na++H++CO32-
B. K2SO4=2K++SO42-
C. NH4NO3=NH3+H++NO3-
D. Al2(SO4)3=2Al+3+3SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������A12O3�������100mLNaOH��Һ�У�����ȫ���ܽ�����������Һ����μ���1.0 molL-1���ᣬ���ó��������ʵ����������������Ĺ�ϵ��ͼ��ʾ����������Һ����ı仯����������˵����ȷ����

A. ԭNaOH��Һ��Ũ��Ϊ1.0mol/L B. ԭA12O3������Ϊ0.51g
C. V0����ֵΪ35 D. �������ﵽ���ʱ����Һ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1L0.1molL��1NH4Cl��Һ�У����ϼ������NaOH��NH4+��NH3H2O�ı仯������ͼ��ʾ������������仯�Ͱ��Ļӷ���������˵����ȷ���ǣ� �� 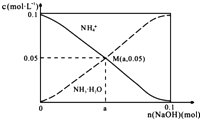
A.M����Һ��ˮ�ĵ���̶ȱ�ԭ��Һ��
B.��M��ʱ��n��OH������n��H+��=��a��0.05��mol
C.����NaOH�ļ��룬 ![]() ��������
��������
D.��n��NaOH��=0.05molʱ��Һ���У�c��Cl������c��Na+����c��NH4+����c��OH������c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��������������ɵ�����ʵ��װ�ã�������Ӥ����Һ����߹����Լ�������˵���������

A. װ��P2O5�����E�������ڸ��ﰱ��
B. A��Bװ���������ռ�Cl2�����������ռ�NO
C. C��Dװ�ÿ�������β���������ܷ�ֹҺ�嵹�������巢��װ����
D. F װ�ÿ����ںϳɰ�ʵ���У���װ��Ũ������Ը����ϲ��ܴ��¹۲�H2��N2�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ���������������Լ��ͷ�������ȷ���� �� ��
A. Cu��Fe������ϡ���ᣬ���� B. CO2��SO2��������������Һ��ϴ��
C. NaCl��Һ���⣩���ƾ�����ȡ����Һ D. N2(O2)�������建��ͨ�����ȵ�ͭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�� ��101kpaʱ�����顢��Ȳ�ͱ�ϩ��ɵĻ����32mL�����������ϲ���ȫȼ�գ���ȥˮ�������ָ���ԭ�����¶Ⱥ�ѹǿ��������������С��72mL��ԭ���������Ȳ���������Ϊ�� ��
A.12.5%
B.25%
C.50%
D.75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������:MnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2������˵���������(����)
MnCl2��2H2O��Cl2������˵���������(����)
A. ��ԭ����HCl����������MnO2
B. ÿ����1 mol Cl2��ת�Ƶ��ӵ����ʵ���Ϊ2 mol
C. ÿ����1 mol MnO2����ԭ�����õ�HClΪ4 mol
D. ���ɵ�Cl2�к���HCl���ʣ��ñ���ʳ��ˮ��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ÿ�����֤�ǽ����Եı仯���ɡ�

��1������A������Ϊ_____________________�������D��������______________________��
��2��ʵ����������ҩƷNa2S��KMnO4��Ũ���ᡢMnO2����ѡ�����ҩƷ���ʵ����֤�ȵķǽ����Դ�����װ��A��B��C����װҩƷ�ֱ�Ϊ________��_______��_______��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ����ӷ���ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com