
【题目】环戊二烯可用于制备二茂铁 [Fe(C5H5)2];二茂铁分子是一种金属有机配合物,结构如图所示,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。下列说法正确的是
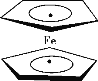
A.1 mol环戊二烯( ![]() )中含有5 mol σ键
)中含有5 mol σ键
B.环戊二烯分子中所有原子共平面
C.二茂铁分子中存在配位键
D.Fe2+的价电子排布式为3d44s2
科目:高中化学 来源: 题型:
【题目】根据要求,回答下列问题
I.氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应均为2H2+O2 = 2H2O。
(1)工作时,电解质溶液中的阴离子移向_______极(填“正”或“负”)。
(2)酸式氢氧燃料电池的电解质溶液是稀硫酸,其正极的电极反应为________。
(3)碱式氢氧燃料电池的电解质溶液是KOH溶液,其负极的电极反应为_______。
II.通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示,O2-可在固体电解质中自由移动。
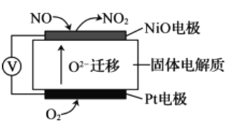
(1)NiO电极上发生的是________反应(填“氧化”或“还原”)。
(2)外电路中,电子是从_________电极流出(填“NiO”或“Pt”)。
(3)Pt电极的电极反应为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将100 mL 1 mol·L-1的氨水与100 mL a mol·L-1盐酸等体积混合,忽略反应放热和体积变化,下列有关推论不正确的是
A. 若混合后溶液pH=7,则c(NH4+)=c(Cl-)
B. 若a=2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C. 若a=0.5,则c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D. 若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.标准状况下,将22.4 LHCl溶于1 L水,可配成1 mol/L的稀盐酸
B.把200 mL3 mol/L的MgCl2溶液跟100 mL3 mol/L的KCl溶液混合后,溶液中的Cl-的物质的量浓度仍然是3 mol/L
C.用胆矾(CuSO45H2O)配制500 mL5 mol/L的CuSO4溶液,需胆矾40 g
D.将0.1 mol NaCl配成100 mL溶液,从中取出10 mL,所取出溶液的物质的量浓度为1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是一种重要的工业原料,在160℃分解生成异氰酸和氨气,化学方程式为CO(NH2)2![]() 2HCNO+NH3↑。回答下列问题:
2HCNO+NH3↑。回答下列问题:
(1)上述反应所涉及的各元素中,原子半径最大的是________(填元素符号),其原子核外电子共占据________个原子轨道。
(2)上述元素中有三种元素处于同周期,则:
①最简单气态氢化物的稳定性由大到小的顺序是________(用化学式表示)。
②元素的第一电离能由大到小的顺序是________(用元素符号表示,下同)。
③元素的电负性由大到小的顺序是________________。
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
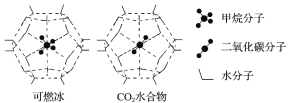
【题目】(1)一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的两种作用力是_____________________________。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是_____。
(2) H2O与CH3CH2OH可以任意比例互溶,除因为它们都是极性分子外,还因为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅在氧气中完全燃烧的化学方程式为:Si+O2![]() SiO2,1 mol Si完全燃烧生成SiO2放出992kJ的热量。已知断裂1mol Si-Si键、1mol O=O键和1mol Si-O键吸收的能量分别为176kJ、496kJ、460kJ。晶体结构知识告诉我们,1mol SiO2中含有4mol Si-O键,则1molSi中含有Si-Si键的物质的量为( )
SiO2,1 mol Si完全燃烧生成SiO2放出992kJ的热量。已知断裂1mol Si-Si键、1mol O=O键和1mol Si-O键吸收的能量分别为176kJ、496kJ、460kJ。晶体结构知识告诉我们,1mol SiO2中含有4mol Si-O键,则1molSi中含有Si-Si键的物质的量为( )
A. 1mol B. 2mol C. 3mol D. 4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 mol/L的NaHSO3溶液中有如下关系:c(Na+)>c(HSO3-) >c(SO32-) >c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为
A.SO32-+H2O![]() HSO3-十OH—B.HSO3-十H2O
HSO3-十OH—B.HSO3-十H2O![]() H2SO3十OH-
H2SO3十OH-
C.HSO3-十OH—![]() SO32—十H2OD.H2SO3+OH-
SO32—十H2OD.H2SO3+OH-![]() HSO3-十H2O
HSO3-十H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com