
| A、用酚酞作指示剂时滴定的总反应为:Na2CO3+HCl═NaHCO3+NaCl |
| B、用甲基橙作指示剂时滴定的总反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O |
| C、可用碱式滴定管量取所需要的Na2CO3溶液 |
| D、若酸式滴定管没有用标准溶液润洗,则所测得的碳酸钠溶液浓度偏低 |
| c(HCl)?V(HCl) |
| V(NaOH) |
| c(HCl)?V(HCl) |
| V(NaOH) |


科目:高中化学 来源: 题型:
| A、它们的分子个数比为1:1 |
| B、它们的原子个数比为5:4 |
| C、它们的电子个数比为1:1 |
| D、它们的体积比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NH4+、Cl-、CO32- |
| B、Fe3+、Mg2+、SO42-、NO3- |
| C、Ba2+、Ca2+、Br-、SO42- |
| D、Zn2+、Ca2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
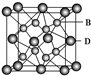 有A、B、C、D、E五种元素,其相关信息如下:
有A、B、C、D、E五种元素,其相关信息如下:| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C基态原子的2p轨道中有3个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有2个运动状态不同的电子 |
| E | E的+1价离子的M能层中所有能级各轨道都有电子且没有未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温、高压 |
| 催化剂 |
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl晶体、BaSO4 |
| B、液态的醋酸、酒精 |
| C、铜、二氧化硫 |
| D、熔融的KNO3、硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、abR |
| B、a+ba+2R |
| C、a+b-2a+2R |
| D、a+b-2a-2R |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-═AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| C、在碳酸氢镁溶液中加入过量氢氧化钠溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| D、向NH4HCO3溶液中加过量的NaOH溶液并加热NH4++OH-═△NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
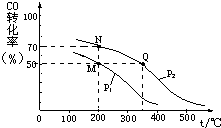 开发新能源和三废处理都是可持续发展的重要方面.CO在催化剂作用下可以与H2反应生成甲醇:
开发新能源和三废处理都是可持续发展的重要方面.CO在催化剂作用下可以与H2反应生成甲醇:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com