
【题目】某化学课外活动小组通过实验研究NO2的性质。
已知:2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O
利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。

(1)E装置中制取NO2反应的化学方程式是________________________________。
(2)制取氨气时若只用一种试剂,从下列固体物质中选取___________
a.NH4HCO3 b.NH4C1 c.Ca(OH)2 d.NaOH
(3)若NO2能够被NH3还原,预期观察到C装置中的现象是____________________。
(4)实验过程中气密性良好,但未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
① NH3还原性较弱,不能将NO2还原;② 在此条件下,NO2的转化率极低;
③_______________________________________
(5)此实验装置存在一个明显的缺陷是________________________
(6)为了验证NO2能被Na2O2氧化,该小组同学选用B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如右图所示),重新组装,进行实验。

① 装置的合理连接顺序是 _____________
② 实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中反应的化学方程式为____________________。
【答案】 Cu + 4HNO3 (浓) === Cu(NO3)2 + 2NO2↑+ 2H2O a C装置中混合气体颜色变浅 在此条件下,该反应的化学反应速率极慢 缺少尾气吸收装置 EDBF 2NO2 + Na2O2 = 2NaNO3
【解析】试题分析:(1)E装置中铜与浓硝酸反应生成Cu(NO3)2、NO2、H2O;(2)NH4HCO3分解生成氨气、水、二氧化碳; NH4C1分解生成氨气、氯化氢,但氨气、氯化氢又能生成NH4C1 ;Ca(OH)2 、NaOH不能生成氨气;(3)二氧化氮是红棕色气体,如果能被氨气还原,生成无色气体氮气;(4)化学反应速率极慢或NO2的转化率极低导致反应现象不明显;(5)二氧化氮是有毒气体,氨气是有刺激性气味的气体,所以都不能直接排入空气;(6)①验证NO2能被Na2O2氧化,首先要用E装置制取二氧化氮,因为制取的二氧化氮气体中含有水蒸气,水能和过氧化钠反应而造成干扰,所以要用D装置除去水蒸气,然后较纯净的二氧化氮通过B装置,未反应的二氧化氮有毒不能直接排空,所以最后要进行尾气处理,选用F装置处理尾气;②B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成,说明NO2 与Na2O2反应生成NaNO3。
解析:(1)E装置中铜与浓硝酸反应生成Cu(NO3)2、NO2、H2O,反应方程式是Cu + 4HNO3 (浓) === Cu(NO3)2 + 2NO2↑+ 2H2O;(2)NH4HCO3分解生成氨气、水、二氧化碳; NH4C1分解生成氨气、氯化氢,但氨气、氯化氢能生成NH4C1 ;Ca(OH)2 、NaOH不能生成氨气,所以制取氨气用碳酸氢铵,故选a;(3)二氧化氮是红棕色气体,如果能被氨气还原,生成无色气体氮气,现象是C装置中混合气体颜色变浅;(4)造成未能观察到C装置中的预期现象可能原因是:在此条件下,该反应的化学反应速率极慢或NO2的转化率极低导致反应现象变化不明显;(5)二氧化氮是有毒气体,氨气是有刺激性气味的气体,所以都不能直接排入空气,装置的明显缺陷是缺少尾气处理装置;(6)①验证NO2能被Na2O2氧化,首先要用E装置制取二氧化氮,因为制取的二氧化氮气体中含有水蒸气,水能和过氧化钠反应而造成干扰,所以要用D装置除去水蒸气,然后较纯净的二氧化氮通过B装置,未反应的二氧化氮有毒不能直接排空,所以最后要进行尾气处理,选用F装置处理尾气,所以仪器的连接顺序是EDBF;②B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成,说明NO2与Na2O2反应生成NaNO3,反应方程式是2NO2 + Na2O2 = 2NaNO3。


科目:高中化学 来源: 题型:
【题目】金属元素及其化合物在科学研究和生产生活中有着广泛的用途
(1)氢气还原氧化铜时,产生的红色物质,冷却后加入稀硫酸发现溶液呈淡蓝色,写出该现象发生的离子方程式__________________________。
(2)取铝合金(含铝90%)1.5 g 与适量的 盐酸恰好完全反应(合金中其它成分不参加反应)。滤去不溶物,向滤液加入0.6 molL-1 的氨水使Al3+ 恰好完全沉淀。上述铝合金和盐酸反应的过程中生成氢气_____L(标准状况)。使Al3+ 恰好完全沉淀时,消耗氨水____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学化学常见的化合物,A、B、C均含有元素X。它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中不正确的是 ( )
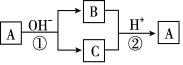
A. X元素可能为Al B. X元素一定为非金属元素
C. A可能是Cl2 D. 反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜(含少量锌、金、银等杂质)的精炼原理,其中乙装置中X为阳离子交换膜.请按要求回答相关问题: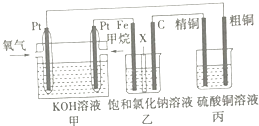
(1)甲烷燃料电池正极反应式是 .
(2)乙装置中阳离子通过X膜向极(填“Fe”或“C”)移动,石墨(C)极的电极反应式为 .
(3)若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为g,硫酸铜溶液的浓度将(填“增大”、“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 油脂是高级脂肪酸的甘油酯
B. 油脂与氢气发生加成反应,可以得到固态油脂
C. 油脂在酸性或碱性条件下,可以发生皂化反应
D. 油脂没有固定的熔、沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们的饮食追求是“吃得营养,吃出健康”,下列相关说法不正确的是( )
A.每天都应摄入一定量的蛋白质
B.油脂会使人发胖,故禁食油脂
C.过多摄入微量元素不利于健康
D.每天食用少量纤维素有利于健康
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是:
A. 漂白粉被氧化了
B. 漂白粉和空气中的二氧化碳充分反应生成了次氯酸
C. 有色布条被空气中的氧气氧化
D. 漂白粉溶液失去了部分水分,浓度增大了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体成分。
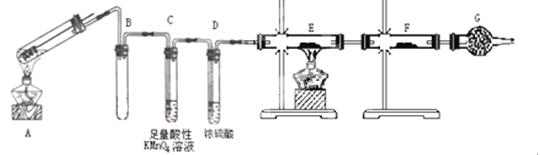
(1)填写装置的作用:B___________,C___________,G___________。
(2)证明有S02生成的实验现象是_____________________。
(3)可以证明所产生的气体中含有H2的实验现象是:E中:___________,F中:_________。如果去掉装置D,还能否根据F中的现象判断气体中有H2?_________(填能”或“不能”),原因是_________________________。
(4)反应后A的溶液中含有Fe3+和Fe2+,检验其中Fe2+的方法是____________。
(5)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体。原因是___________________________;要确认有CuSO4生成,待试管冷却后,____________。写出铜与浓硫酸反应的离子方程式________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com