
【题目】亚硝酸氯(ClNO)是有机合成中的重要试剂。亚硝酸氯可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K1
2NaNO3(s)+2NO(g)+Cl2(g) K1
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K2
NaNO3(s)+ClNO(g) K2
③2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
则K1,K2,K3之间的关系为K3=______________。
(2)T℃时,2NO(g)+Cl2(g)![]() 2ClNO(g)的正反应速率表达式为v正= k cn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正= k cn(ClNO),测得速率和浓度的关系如下表:
序号 | c(ClNO)/mol·L-1 | v/mol·L-1·s-1 |
① | 0.30 | 3.6×10-8 |
② | 0.60 | 1.44×10-7 |
③ | 0.90 | 3.24×10-7 |
n=____________;k=____________(注明单位)。
(3)在2L的恒容密闭容器中充入4molNO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图A:


①温度为T1时,能作为该反应达到平衡的标志的有 ;
a.容器体积保持不变
b.容器压强保持不变
c.平衡常数K保持不变
d.气体颜色保持不变
e.v(ClNO)= v(NO)
f.NO与 ClNO的物质的量比值保持不变
②反应开始到10min时Cl2的平均反应速率v(Cl2)=____________;
③温度为T2时,10min已经达到平衡,该反应的平衡常数K=____________(注明单位)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数φ随n(NO)/n(Cl2)的变化图象如图B,则A、B、C三状态中,NO的转化率最小的是__________点,当n(NO)/n(Cl2)=2.8时,达到平衡状态ClNO的体积分数φ可能是D、E、F三点中的_________点。
【答案】(1)K22/K1
(2)n=2;k=4.0×10-7mol-1·L·s-1(注明单位)。
(3)①bdf;②0.05mol·L-1·min-1;③2L/mol(注明单位)。
(4)C点 F点。
【解析】
试题分析:
(1)已知:①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g)
NaNO3(s)+ClNO(g)
将②×2-①可得③:2NO(g)+Cl2(g)![]() 2ClNO(g),平衡常数K3=K22/K1。
2ClNO(g),平衡常数K3=K22/K1。
(2)根据数据,结合正反应速率表达式为v正=k·cn(ClNO)可知,3.60×10-8mo1/(L·s)=k×(0.3mo1/L)n,1.44×10-7mo1/(L·s)=k×(0.6mo1/L)n,解得n=2,k=4.0×10-7L/(mo1·s);
(3)根据图A可知,温度越高,c(ClNO)越小,说明2NO(g)+Cl2(g)![]() 2ClNO(g)为放热反应,且正反应方向的气体系数减小。
2ClNO(g)为放热反应,且正反应方向的气体系数减小。
①a.2L的恒容密闭容器,容器体积始终保持不变,不能作为该反应达到平衡的标志;b.随着反应进行,容器总压强逐渐减小,当容器压强保持不变时,说明反应已经达到平衡状态;c.平衡常数K只与温度有关,温度为T1时,K保持不变,不能作为该反应达到平衡的标志;d.气体颜色保持不变,即说明c(Cl2)保持不变,反应已经达到平衡状态;e.NO和ClNO的系数相同,则有任何时候v(ClNO)= v(NO),不能作为该反应达到平衡的标志;f.NO与 ClNO的物质的量比值保持不变,说明反应已经达到平衡状态;故选bdf。
②反应开始到10min时,c(C1NO)=1mol/L,则v(C1NO)= ![]() =0.1mol/(L·min),则Cl2的平均反应速率v(Cl2)=
=0.1mol/(L·min),则Cl2的平均反应速率v(Cl2)=![]() v(C1NO)=0.05mol/(L·min);
v(C1NO)=0.05mol/(L·min);
③ 2NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
起始(mol/L) 2 1 0
反应(mol/L) 1 0.5 1
平衡(mol/L) 1 0.5 1
T2时该反应的平衡常数K=![]() =
=![]() =2L/mol;
=2L/mol;
(4)n(NO)/n(C12)的比值越大,NO的转化率越小,NO的转化率最小的是C点。根据曲线的变化趋势,当n(NO)/n(C12)=2.8,达到平衡状态ClNO的体积分数是F。


科目:高中化学 来源: 题型:
【题目】利用图示装置收集以下8种气体(图中烧瓶的位置不得变化)①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2

(1)若烧瓶是干燥的,则由B口进气收集的气体有________(写序号);
(2)若烧瓶充满水,可收集的气体有________,这时气体由________进入。
(3)若烧瓶是干燥的,则由A口进气,可收集的气体有________。
(4)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有____,这时气体由________口进入。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在10mL浓度均为0.1mol/L的NaOH和CH3COONa混合溶液中滴加0.1mol/L的盐酸,所得滴定曲线如图所示。下列说法正确的是
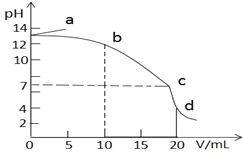
A. a点溶液加水稀释,![]() 逐渐增大
逐渐增大
B. b→c段发生反应的离子方程式是:CH3COO- + H+ = CH3COOH
C. c点时水的电离程度最大
D. d点溶液中c(Na+)=c(Cl-)>c(CH3COOH)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A+B==C+D的能量变化如图所示,下列说法正确的是

A. 该反应为吸热反应
B. 该反应只有在加热条件下才能进行
C. 反应物的总能量高于产物的总能量
D. 形成产物C和D的化学键所放出的总能量高于断开反应物A 和B的化学键所吸收的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。

请回答下列问题:
(1)D中含有的官能团是_______________(写名称)②的反应类型是___________。
F的化学名称是_______________,
(2)D分子间生成六元环的化学方程式为_____________________________。
(3)反应②的化学方程式是______________________________________。
(4)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为______________________________。
(5)分子式C9H10O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体有__________________种(不考虑立体异构)。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线_____________ (无机试剂任选)。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由环己烷可制得1, 4 – 环己二醇,下列有7步反应(其中无机产物都已略去)。试回答:

(1) 上述反应 (填编号)属于取代反应。
(2) 化合物的结构简式:
B ,C ;
(3) 反应④所用试剂和条件是 ;
(4) 写出反应②、⑤的化学方程式:
反应② ;
反应⑤ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com