
����Ŀ��Ԫ�����ڱ��е�������Ԫ��������3d���ӵ�Ӱ�죬���ʵĵݱ�����������Ԫ�����в�ͬ��
��1���������ڹ���Ԫ�ص������������γɶ��ֶ����������
�� CO���Ժͺܶ���ɽ����γ��������ʻ�����Fe(CO)5�ݣ��ʻ�����Ni(CO)4�ݡ�CO������Cԭ������һ�Թ¶Ե��ӣ�C��Oԭ�Ӷ�����8�����ȶ��ṹ��CO�ĽṹʽΪ ����CO��Ϊ�ȵ����������Ϊ (�ѧʽ)��
�� ����������CO�����������ȣ�����Һ̬Ni(CO)4���ӡ�423Kʱ��Ni(CO)4�ֽ�ΪNi��CO���Ӷ��Ƶøߴ��ȵ�Ni�ۡ����Ʋ�Ni(CO)4���������� ��
A��ˮ B�����Ȼ�̼ C���� D����������Һ
��2����������Ԫ�صĵ�һ��������ԭ��������������������������ġ��صĻ�̬ԭ�ӵĵ����Ų�ʽ�� ��Ga�ĵ�һ������ȴ���Ե���Zn��ԭ���� ��
��3���ü۲���ӶԻ�������Ԥ��H2Se��BBr3������ṹ���������۶���ȷ���� ��
A��ֱ���Σ�������
B��V��������
C��ֱ���Σ�ƽ��������
D��V�Σ�ƽ��������
���𰸡�
��1�� ��C��O��CN- ���� bc
��2��1s22s22p63s23p63d104s24p1��Znԭ�ӵļ۵����Ų�ʽΪ3d104s2����ϵ�������ϵͣ�ԭ�ӽ��ȶ�����Zn�ĵ�һ�����ܴ���Ga
��3��d
��������
�����������1����CO������Cԭ������һ�Թ¶Ե��ӣ�C��Oԭ�Ӷ�����8�����ȶ��ṹ����CO�ĽṹʽΪC��O���ȵ�������ԭ�����ͼ۵���������ͬ���� N2��CN-��CO��ԭ��������2���۵���������10����Ϊ�ȵ�������
�ʴ�Ϊ��C��O��CN-��
��Ni��CO��4��Ni��ȡSP3�ӻ�������������ṹ���������ڷǼ��Է��ӣ�������������ԭ�����Ǽ������������ڷǼ����ܼ����������Ȼ�̼�ǷǼ��Է��ӣ�����Ni��CO��4�����ڱ������Ȼ�̼��
�ʴ�Ϊ��bc��
��2������31��Ԫ�أ���ԭ�Ӻ�����31�����ӣ�4S�ܼ�����С��3d�ܼ������������������ԭ������������4s�ܼ�����3d�ܼ�������ͭ�ĺ�������Ų�ʽΪ1s22s22p63s23p63d104s24p1��Znԭ�ӵļ۵����Ų�ʽΪ3d104s2���۵�����3d��4s���Ϊȫ����״̬��ԭ�ӽ��ȶ�����Zn�ĵ�һ�����ܴ���Ga��
�ʴ�Ϊ��1s22s22p63s23p63d104s24p1��Znԭ�ӵļ۵����Ų�ʽΪ3d104s2����ϵ�������ϵͣ�ԭ�ӽ��ȶ�����Zn�ĵ�һ�����ܴ���Ga��
��3��H2S���ӵ�����ԭ��Sԭ���Ϻ���2���� ��������ԭ���ϵŵ��Ӷ���=![]() =4������������ӵ�VSEPRģ�����������ͣ���ȥ�µ��ӶԺ�ʵ������ռ乹����V�ͣ�
=4������������ӵ�VSEPRģ�����������ͣ���ȥ�µ��ӶԺ�ʵ������ռ乹����V�ͣ�
BF3���ӵ�����ԭ��Bԭ���Ϻ���3���� ��������ԭ���ϵŵ��Ӷ���=![]() =3������BF3���ӵ�VSEPRģ����ƽ�������ͣ�����ԭ����û�й¶Ե��ӣ�������ռ乹�;���ƽ����������
=3������BF3���ӵ�VSEPRģ����ƽ�������ͣ�����ԭ����û�й¶Ե��ӣ�������ռ乹�;���ƽ����������
��ѡ��d��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼��������������ԭ��֮һ,ijͬѧ���õ�����ͬ��ʯ��ʯ������̼��ơ������ͼ��ʾ�ļס�������·�ߣ��������ʲ����뷴Ӧ��ÿһ����Ӧ��ȫ��������������ȷ����
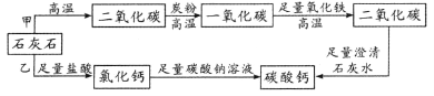
A���ס��ҷ����Ƶ�̼���������ȣ�������Ӧ�������̡����̸���
B���ס����������Ƶ�̼���������ȣ��ҷ�����������ȫ�ɿ�
C�������Ƶ�̼������ҷ�����2�����¶ȸߡ���Ӧ���ʿ죬���ҷ�����
D�������Ƶ�̼������ҷ�����2��,���ҵIJ�������Ӧ������,�ۺ������ȼ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��Ȼ�����ṩ���ܹ�Ϊ�������õĵ�ˮ��Դ�����ḻ�����ҵ�ˮ��Դȱ�������������Ͼ�������ĺ�ˮ����ԼΪ1.3��109�ڶ֣�����������ˮ��Դ�⡣���������ǽ��귢չ������һ�ֽϺõĺ�ˮ������������ԭ������ͼ��ʾ��
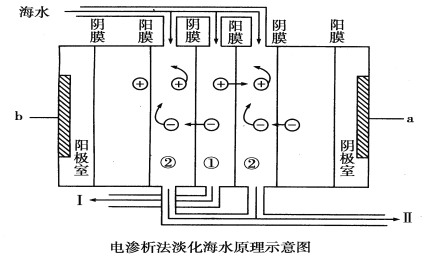
�ش��������⣺
��1�����еĺ�ˮ________(������������������)ֱ��ͨ�뵽װ���У�������_______________________��
��2��a�ǵ�Դ��________����b�ǵ�Դ��________����
��3������________��(������ˮ������Ũˮ��)�������ų�����________(������ˮ������Ũˮ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�CuCl2��2H2O�Ʊ�CuCl�����������̽����
�����ϲ��ġ�
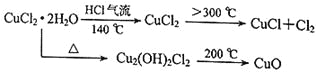
��ʵ��̽������С������ͼ��ʾװ�ý���ʵ�飨�г������ԣ���
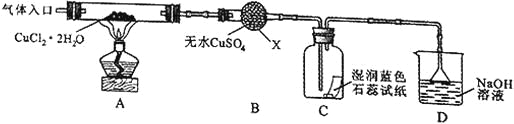
��ش��������⣺
��1������X��������__________��
��2��ʵ��������Ⱥ�˳����a��______��e��������ı�ţ���
a�����װ�õ������Ժ����ҩƷ b��Ϩ��ƾ��ƣ���ȴ
c�����������������ͨ�����HCl d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��3����ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯��_______��
��4��װ��D�з�����������ԭ��Ӧ�����ӷ���ʽ��________________��
��5����Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����������Ϣ������
����������CuCl2���������ԭ����________________��
����������CuO���������ԭ����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ������˵���д�������� ��
A��32 g O2�����ķ�����ĿΪNA
B��1 mol H2O���е�H2O������ĿΪNA
C��1 mol H2O���е���ԭ����ĿΪNA
D��0.5NA��O2���ӵ����ʵ�����0.5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������г�����һЩԭ�ӵ�2p�ܼ���3d�ܼ��е����Ų�����������жϣ�Υ��������ԭ������________��Υ���˺��ع������________��

��2��ijԪ�صļ���̬(���ȶ�״̬)ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s13p33d2�����Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ________��������������Ӧˮ����Ļ�ѧʽ��________��
��3���÷�����>������<������������ʾ���и����ϵ��
����һ�����ܣ�Na________Mg��Mg________Ca��
���縺�ԣ�O________F��F________Cl��
�������ߵͣ�ns________(n��1)s��ns________np��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е�Ԫ�����в������Ƚ�����Ƶ���
A�����ʳ��ˮ���ռ� |
B���ϳɰ��еĴ��ϳ� |
C�����������еĴ����� |
D������еİ���ˮ̼�ữ |
����ˮɹ�ε�±ˮ�л����Ȼ�þ����±ˮΪԭ������þ��һ�й�����������ͼ��ʾ��
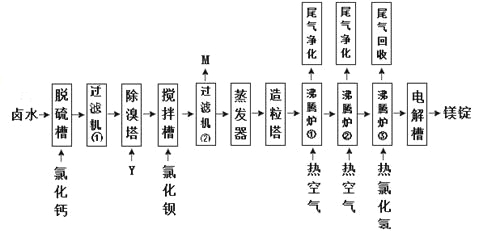
�ش��������⣺
��1������ۡ�����۾������ѳ�±ˮ�еģ������ӷ��ţ���M����Ҫ�ɷ��ǣ��ѧʽ����
��2������������Ҫ�����ӷ���ʽΪ��
��3������¯����������Ҫ�����ǡ�����¯��ͨ�����Ȼ������ҪĿ���ǡ�
��4�������������ĵ缫��Ӧ����ʽΪ��
��5����������������Ϊ���ò����ֱ�����ڱ����������еġ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���2.3������ȫȼ�պ�IJ�������ͨ��Ũ������NaOH��Һ���ֱ�����2.7����4.4�������л���ķ���ʽ���� ��
A��C2H6O B��C2H4O
C��C2H6 D��C2H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ɢϵ�з�ɢ��������С����
A. ��������Һ B. Fe��OH��3���� C. ����ֲ���ͺ�ˮ��� D. ��ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com