
50 mL 0.50 mol��L-1������50 mL 0.55 mol��L-1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش���������: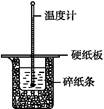
(1)��ʵ��װ���Ͽ�,ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
(2)�ձ���������ֽ���������� ��
(3)���ձ����粻��Ӳֽ��,��õ��к�����ֵ (�ƫ��ƫС������Ӱ�족)��
(4)ʵ���и���60 mL 0.50 mol��L-1�����50 mL 0.55 mol��L-1 NaOH��Һ���з�Ӧ,������ʵ�����,���ų������� (���ȡ�����ȡ�)�������к��� (���ȡ�����ȡ�),��������: ��
(5)����ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ��,��õ��к��ȵ���ֵ�� ,��50 mL 0.50 mol��L-1 NaOH��Һ��������ʵ��,��õ��к��ȵ���ֵ�� (���ƫ��ƫС������Ӱ�족)��
 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д� ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��H+(aq)+OH-(aq)= H2O(l) ��H="-57.3" kJ/ mol�����������кͷ�Ӧ�зų���������
��1����20 g NaOH��ɵ�ϡ��Һ��������ϡ���ᷴӦ���ܷų� kJ��������
��2����0.1 mol Ba(OH)2��ɵ�ϡ��Һ��������ϡ���ᷴӦ���ܷų� kJ��������
��3����1 mol����ϡ��Һ������NaOHϡ��Һ��Ӧ���ų������� ������ڡ�����С�ڡ����ڡ���57.3 kJ�������� ��
��4��1 L 0.1 mol/L NaOH��Һ�ֱ���ٴ�����Һ����Ũ���ᡢ��ϡ����ǡ�÷�Ӧʱ���ų��������ֱ�ΪQ1��Q2��Q3����λ��kJ�����������ɴ���С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
I����ҵ�Ͽ���CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)
CH3OH(g)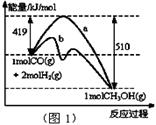
��1����ͼ1����ʾ��Ӧ�������ı仯������ ���a��b������ʾʹ���˴������÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2���������ݻ����䣬���д�ʩ������COƽ��ת���ʵ���_____��
| A�������¶� |
| B����CH3OH(g)����ϵ�з��� |
| C������He��ʹ��ϵ��ѹǿ���� |
| D���ٳ���1 mol CO��2 mol H2 |
 BaCO3(s)+SO42��(aq)��
BaCO3(s)+SO42��(aq)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��������Ҫ�Ļ�����Ʒ֮һ��
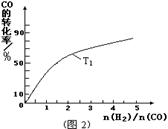
��1���ϳɰ��õ��������Լ���Ϊԭ���Ƶá��йػ�ѧ��Ӧ�������仯����ͼ��ʾ��
��Ӧ�٢ڢ�Ϊ_________��Ӧ������ȡ����ȡ�����CH4(g)��H2O(g)��Ӧ����CO(g)��H2(g)���Ȼ�ѧ����ʽΪ__________________��
�� �� ��
��2���ð�����ȡ����[CO(NH2)2]�ķ�ӦΪ��2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)��
CO(NH2)2(l)+H2O(g)��
��ij�¶��£����ݻ�Ϊ10L���ܱ�������ͨ��2mol NH3��1molCO2����Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=___________�����¶���ƽ�ⳣ��K�ļ�����Ϊ____________��
��Ϊ��һ�����CO2��ƽ��ת���ʣ����д�ʩ���ܴﵽĿ�ĵ���_____________
| A�����NH3��Ũ�� | B������ѹǿ |
| C����ʱת�����ɵ����� | D��ʹ�ø���Ч�Ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
����һ���������ɫ�����Դ����������ȡ�봢��������Դ����������о��ȵ㡣����FeO/Fe3O4ѭ�����⣬��֪��
H2O(g)+3FeO(s) Fe3O4(s)+4H2(g) ��H=akJ/mol ��I��
Fe3O4(s)+4H2(g) ��H=akJ/mol ��I��
2Fe3O4(s) 6FeO(s)+O2(g) ��H=bkJ/mol ��II��
6FeO(s)+O2(g) ��H=bkJ/mol ��II��
��������ͼ�ֱ��ʾFeO��ת���ʣ�ͼ-1 )��һ���¶�ʱ��H2����������[ϸ����(ֱ��0.25 mm)���ֿ���(ֱ��3 mm)](ͼ-2)��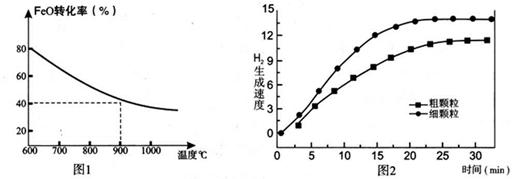
��1����Ӧ��2H2O(g)=2H2(g)+O2(g) ��H= (�ú�a��b����ʽ��ʾ)��
��2��������Ӧb��0��Ҫʹ�����ⷽ����ʵ�����壬����Դ���ü��ɱ��ĽǶȿ��ǣ�ʵ�ַ�ӦII�ɲ��õķ����ǣ� ��
��3��900��Cʱ�������������Ϊ2.0L�ܱ������зֱ�Ͷ��0.60molFeO��0.20mol H2O(g)��������ϸ����FeO���������ôֿ���FeO��
����ϸ����FeO�ʹֿ���FeOʱ��H2�������ʲ�ͬ��ԭ���ǣ� ��
��ϸ����FeOʱH2O(g)��ת���ʱ��ôֿ���FeOʱH2O(g)��ת���� �����С������ȡ�����
������¶��¸÷�Ӧ��ƽ�ⳣ��K��д��������̣�������λ��Ч���֣���
��4������������ͼ3�л�����1000��C����ϸ����FeOʱ��H2O(g)ת������ʱ��仯ʾ��ͼ��������Ӧ�ı�ע����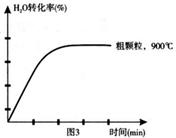
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��50 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺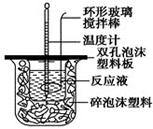
��1���ձ�����������ĭ���ϵ�������___________________________
��2�����β���������ܷ��û������ʽ�������棿_____(��ܡ����ܡ�)��
��ԭ����_______________________________________________________��
��3��ʵ��ʱ����������Һ��Ũ��Ҫ��0.55 mol/L��ԭ����______________________��
ʵ����������60 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ���з�Ӧ�� ������ʵ����ȣ����ų�������_______ _____(���ȡ�������ȡ�)����ʵ���������ȷ���������к���________________(���ȡ�������ȡ�)��
��4����֪��ϡ��Һ�У�ǿ���ǿ����кͷ�Ӧ����1 mol H2Oʱ���ų�57.3 kJ����������������Ӧ���Ȼ�ѧ����ʽΪ��__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��¯������ұ��������Ҫ��������������Ҫ��ӦΪ��
Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ��H =" a" kJ mol��1
2Fe(s)+3CO2(g) ��H =" a" kJ mol��1
��1����֪��
��Fe2O3(s)+3C(ʯī) = 2Fe(s)+3CO(g) ��H1 =" +" 489.0 kJ mol��1
��C(ʯī)+CO2(g) = 2CO(g) ��H2 =" +" 172.5 kJ mol��1
��a = kJ mol��1��
��2��ұ������Ӧ��ƽ�ⳣ������ʽK = ���¶����ߺ�Kֵ ������������䡱��С������
��3����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
| | Fe2O3 | CO | Fe | CO2 |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 2.0 | 1.0 | 1.0 |
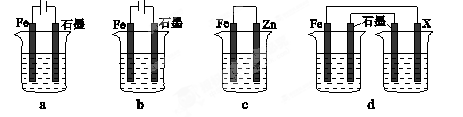
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
Ӱ�컯ѧ��Ӧ������ƽ��������ж�棬��Ũ��ѹǿ�¶ȴ����ȡ������й�˵������ȷ����
| A��������������ʱ���ı�ѹǿ�ܸı����巴Ӧ�����ʣ�����һ���ı�ƽ�� |
| B������Ũ���ܼӿ컯ѧ��Ӧ���ʣ�ԭ��������Ũ�Ⱦ������˷�Ӧ��ϵ�л���ӵİٷ��� |
| C���¶�����ʹ��ѧ��Ӧ���ʼӿ����Ҫԭ���������˷�Ӧ��ϵ�л���ӵİٷ��� |
| D����������ܽ��ͷ�Ӧ����Ļ�ܣ�ʹ��Ӧ���ʼӿ죬ƽ�ⳣ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ϡ����ķ�Ӧ�У���֪10 sĩ�����Ũ�ȼ�����0.6 mol��L-1,�������Ƿ�Ӧ��������Һ����ı仯����10 s��������������ƽ����Ӧ�����ǣ�����
| A��0.02 mol��L-1��s-1 | B��1.8 mol��L-1��s-1 | C��1.2 mol��L-1��s-1 | D��0.18 mol��L-1��s-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com