
【题目】乙烯的产量是衡量一个国家石油化工发展水平的重要标志之一,以乙烯为原料合成的部分产品如图所示。下列有关说法正确的是
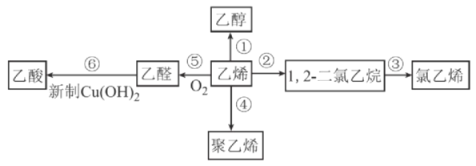
A.氧化反应有①⑤⑥,加成反应有②③
B.氯乙烯、聚乙烯都能使酸性KMnO4溶液褪色
C.反应⑥的现象为产生砖红色沉淀
D.可用乙醇萃取Br2的CCl4溶液中的Br2
【答案】C
【解析】
反应①为乙烯与水发生加成反应生成乙醇,反应②为乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应③为1,2-二氯乙烷发生消去反应生成氯乙烯,反应④为乙烯发生加聚反应生成聚乙烯,反应⑤为乙醇发生催化氧化生成乙醛,反应⑥为乙醛被新制氢氧化铜悬浊液氧化生成乙酸,据此解答。
反应①为乙烯与水发生加成反应生成乙醇,反应②为乙烯与氯气发生加成反应生成1,2-二氯乙烷,反应③为1,2-二氯乙烷发生消去反应生成氯乙烯,反应④为乙烯发生加聚反应生成聚乙烯,反应⑤为乙醇发生催化氧化生成乙醛,反应⑥为乙醛被新制氢氧化铜悬浊液氧化生成乙酸,
A. 根据以上分析知,氧化反应有⑤⑥,加成反应有①②,A项错误;
B. 氯乙烯有碳碳双键,能被酸性KMnO4溶液氧化,从而使酸性KMnO4溶液褪色,聚乙烯没有碳碳双键,不能被酸性KMnO4溶液氧化,则不能使酸性KMnO4溶液褪色,B项错误;
C. 乙醛被新制氢氧化铜悬浊液氧化生成乙酸,氢氧化铜被还原生成氧化亚铜砖红色沉淀,C项正确;
D. 乙醇与CCl4互溶,则不能用乙醇萃取Br2的CCl4溶液中的Br2,D项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,X和Z两元素的原子序数之和等于W元素的原子序数。下列说法正确的是( )
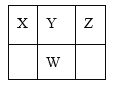
A.X、W分别与Y都能形成两种或两种以上的化合物,这些化合物都是酸性氧化物
B.X、Y、Z都能形成10电子的氢化物,其中Z的最简单氢化物沸点最高
C.X、Y、W与氢四种元素能组成离子化合物,该化合物一定能发生水解
D.X和W两元素的氧化物对应的水化物的酸性:X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】妈妈教小鲁蒸馒头:先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是___。
A.受热易分解 B.水溶液显碱性 C.属于碱 D.可与酸反应
(2)小鲁探究用Na2CO3调节面团酸度,而不用NaHCO3的原因。
①Na2CO3与NaHCO3质量均为1g时,消耗H+的物质的量更多的是___。
②以Na2CO3或NaHCO3为例,计算消耗H+的物质的量,写出计算过程。___
(3)小鲁实际操作时,发现面团发得不好,面团内的气孔少,略有酸味。妈妈指导小鲁将Na2CO3改用NaHCO3,继续揉面,上锅蒸后果然蒸出了松软的馒头。解释NaHCO3的作用___。
(4)某品牌复合膨松剂的说明书如图所示。

其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]化合物J是制备降血脂药贝利贝特的中间体,制备J的一种合成路线设计如下:
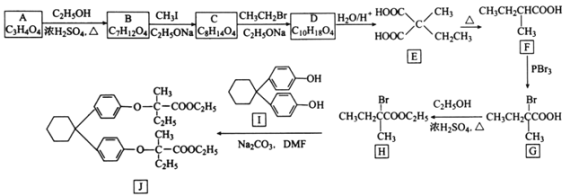
回答下列问题:
(1)A的化学名称是________________。
(2)G生成H的反应类型是________________;J的分子式为________________。
(3)C的结构简式为________________________。
(4)化合物I可由芳香化合物C6H6O和环状化合物C6H10O在醋酸和盐酸催化下制备得到,该反应的化学方程式为________________________________________。
(5)R与E互为同分异构体且与E具有相同的官能团种类和数目,则R的结构有________种。其中对应的核磁共振氢谱图中有四组峰,且峰面积比为4:3:2:1的结构简式为________。
(6)苯氧乙酸乙酯(![]() )是一种农药,设计由苯酚和乙醇为起始原料制备苯氧乙酸乙酯的合成路线:________________(无机试剂任选)。
)是一种农药,设计由苯酚和乙醇为起始原料制备苯氧乙酸乙酯的合成路线:________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某恒容密闭容器中加入1.6 mol L-1的NO2后,会发生如下反应:2NO2(g)N2O4(g) △H =-56.9kJmol-1。其中N2O4的物质的量浓度随时间的变化如图所示,下列说法不正确的是

A.升高温度,60s后容器中混合气体颜色加深
B.0-60s内,NO2的转化率为75%
C.0-60s内,v(NO2)=0.02mol L-1 s-1
D.a、b两时刻生成NO2的速率v(a)>v(b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器内,进行反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)。
CO2(g)+H2(g)。
得到如下两组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
①实验1中以v(CO2)表示的反应速率为___。
②该反应的逆反应为___(填“吸”或“放”)热反应。
(2)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:

①由图可知反应在t1、t3、t7时都达到平衡,而在t2、t8时都改变了条件,试从以下措施中选出适宜的改变条件:t2___、t8___。(此处两空均填下列选项字母序号)
a.增加CO的物质的量 b.加催化剂 c.升高温度 d.压缩容器体积 e.将CH3OH气体液化 f.充入氦气
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆应速率与时间的关系曲线___。
(3)已知反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度___(填“高于”或“低于”)___时均可自发进行。
N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度___(填“高于”或“低于”)___时均可自发进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。
![]()
请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。
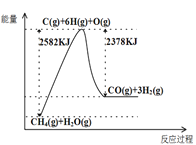
(1)该过程的热化学方程式是__________。
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1_______T2(填“>”“<”或“=”),并说明理由__________。

(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为______________。
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:
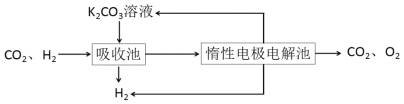
依据图示信息回答:
(4)吸收池中发生反应的离子方程式是_________。
(5)写出电解池中阳极发生的电极反应式________;结合化学用语说明K2CO3溶液再生的原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g)![]() CH3OH(g) H1=90.1kJ·mol1
CH3OH(g) H1=90.1kJ·mol1
ii.2CH3OH(g)![]() CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如右图所示。下列说法正确的是
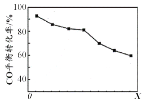
A . 由H2和CO直接制备二甲醚的反应为放热反应
B. 条件X为压强
C. X增大,二甲醚的产率一定增大
D. X增大,该反应的平衡常数一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素E是一种人体必需的脂溶性维生素,现已广泛应用于医药、营养品、化妆品等。天然的维生素E由多种生育酚组成,其中α-生育酚(化合物E)含量最高,生理活性也最高。下面是化合物E的一种合成路线,其中部分反应略去。
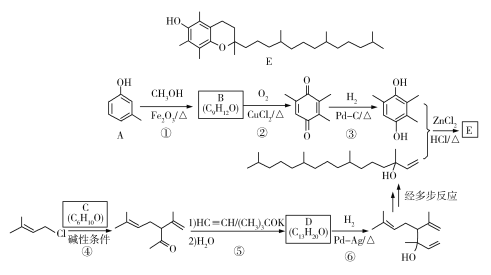
已知以下信息:a) 
b) 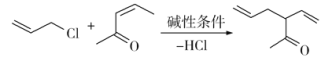
c) 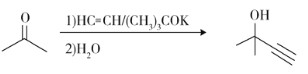
回答下列问题:
(1)A的化学名称为_____________。
(2)B的结构简式为______________。
(3)反应物C含有三个甲基,其结构简式为______________。
(4)反应⑤的反应类型为______________。
(5)反应⑥的化学方程式为______________。
(6)化合物C的同分异构体中能同时满足以下三个条件的有_________个(不考虑立体异构体,填标号)。
(ⅰ)含有两个甲基;(ⅱ)含有酮羰基(但不含C=C=O);(ⅲ)不含有环状结构。
(a)4 (b)6 (c)8 (d)10
其中,含有手性碳(注:连有四个不同的原子或基团的碳)的化合物的结构简式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com