
【题目】下列离子方程式中,不能正确表达反应颜色变化的是( )
A.向氯水中通入SO2气体,溶液浅黄绿色消失:Cl2 + SO2 + 2 H2O = 4H+ + 2Cl- + SO42-
B.向AgNO3溶液中加入一定量HCl溶液,后加入Na2S溶液,白色沉淀变黑色:2AgCl + S2- = Ag2S + 2Cl-
C.向氢氧化铁胶体中加入HI酸溶液,首先出现红褐色沉淀,后沉淀消失,溶液变为黄色:2Fe(OH)3 + 6H+ + 2I- = 2Fe2+ + I2 + 6H2O
D.向CrO42-中加入H2SO4溶液,颜色由黄色变为橙色:2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
【答案】C
【解析】
根据题中子方程式可知,本题考查离子方程式的书写和现象,运用离子方程式的书写步骤和物质的颜色分析。
A. 向氯水中通入SO2气体,Cl2 + SO2 + 2 H2O = 4H+ + 2Cl- + SO42-,Cl2被消耗,溶液黄绿色消失, A项正确;
B. 向AgNO3溶液中加入一定量HCl溶液,先生成AgCl 白色沉淀,后加入Na2S溶液,因为Ag2S的溶解度比AgCl的溶解度小,所以2AgCl + S2- = Ag2S + 2Cl-,白色固体变成黑色固体, B项正确;
C. 向氢氧化铁胶体中加入HI酸溶液,胶体聚沉出现红褐色沉淀,因Fe(OH)3 + 3H+ = 2 Fe3+ +3H2O ,沉淀消失,生成成Fe3+,溶液变为黄色,C项错误;
D. CrO42-显黄色,Cr2O72-显橙色,向CrO42-中加入H2SO4溶液时2CrO42-+2H+![]() Cr2O72-+H2O ,颜色由黄色变为橙色,D项正确;
Cr2O72-+H2O ,颜色由黄色变为橙色,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】室温时,用0. 100 mol·L—1盐酸滴定50. 0mL Na2CO3溶液(不考虑CO2从溶液中逸出).滴定曲线如图所示:
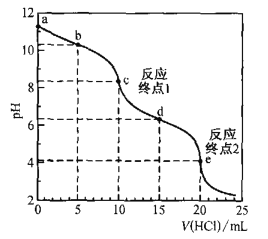
下列说法错误的是
A.a点溶液中:c(Na2CO3)=0.020 mol·L—1
B.b点溶液中:c(Na+)>c(HCO3— )>c(CO32—)
C.c点溶液中:c(Na+)+c(H+)=2c(CO32—) +c(HCO32—)+c(OH—)
D.室温时,H2CO3的一级电离平衡常数Kal的数量级为10—7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g) +![]() O2(g) = H2O(l)△H = -285.8 kJ / mol
O2(g) = H2O(l)△H = -285.8 kJ / mol
②C(s) + O2(g) = CO2(g)△H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g)△H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是______(填序号,下同),属于吸热反应的是____。
(2)1 mol H2完全燃烧生成液态水,放出的热量为____kJ。
(3)写出下列反应的热化学方程式
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量;
_______________________________________________
②2 molCu(s) 与适量O2(g)反应生成CuO(s),放出314 kJ热量;
_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M、N、Q的转化关系为,下列说法正确的是( )
![]()
A. M至N的反应类型是取代反应 B. N的同分异构体有6种
C. 可用酸性KMnO4溶液区分N与Q D. 0.3molQ与足量金属钠反应生成0.15NA个H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. WZ的水溶液呈碱性
B. 元素非金属性的顺序为X>Y>Z
C. Y的最高价氧化物的水化物是中强酸
D. 该新化合物中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列化学实验示意图及表中实验现象,从理论上分析得出的结论正确的是

选项 | 实验 | 实验现象 | 结论 |
A | a | 左烧杯中铁表面有气泡,右烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
B | b | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | c | 白色固体先变为淡黄色,后变为黑色 | 溶解度:AgCl < AgBr < Ag2S |
D | d | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,1mol N2与3mol H2完全反应生成2molNH3的能量变化曲线如图,下列叙述正确的是
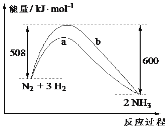
A.形成6 mol N—H键,吸收600 kJ能量
B.b曲线是加入催化剂时的能量变化曲线
C.该反应的ΔH=-92 kJmol-1
D.加入催化剂,能提高N2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__,装置B中玻璃棒的作用是__,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__,①中加入沸石的作用是__,冷却水的方向是__。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__(填代表装置图的字母,下同);除去自来水中的Cl等杂质,选择装置__。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加__,不产生白色沉淀表明Cl已除净。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NOx能与Na2O2反应;NO和NO2均能与酸性KMnO4溶液反应生成NO3ˉ和Mn2+。
I.用下图所示装置(略去夹持仪器)可制得少量亚硝酸钠(2NO+Na2O2=2NaNO2)。

(1)B、D的仪器名称是________,D的作用是________。
(2)通NO前,需先通一段时间N2,目的是________,
(3)E中主要反应的离子方程式为________,
(4)常温下,测得实验前后C的质量差值为0.30g,则制得NaNO2________g。
Ⅱ.NO2和Na2O2都有较强氧化性,为探究NO2与Na2O2反应的产物,提出如下假设:
假设i.NO2氧化Na2O2;假设ii.Na2O2氧化NO2。
甲同学设计如图所示实验装置:

请回答下列问题:
(5)单向阀在实现气体单向流通的同时,还有一个作用是___________。
(6)待试管G中收集满气体,向试管G中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃,甲同学据此认为假设i正确。乙同学认为该装置不能达到实验目的,为达到实验目的,应在F、G之间增加一个M装置,M中应盛装__________(可供选择的试剂:碱石灰,浓硫酸饱和氯化钠溶液);乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得到结论:假设ⅱ正确。
请做出正确判断,写出NO2和Na2O2反应的化学方程式__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com