
【题目】某强酸性溶液X中可能含有Fe2+、Al3+、NH![]() 、CO
、CO![]() 、SO
、SO![]() 、SO
、SO![]() 、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
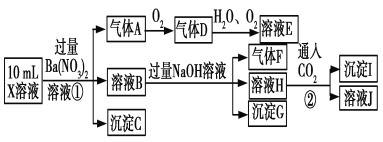
下列说法正确的是
A.气体A是NO2
B.X中肯定存在Fe2+、Al3+、NH![]() 、SO
、SO![]()
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是Al3+和Cl-
【答案】D
【解析】
试题分析:强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子;溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子;溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3或BaCO3,H为NaAlO2,说明溶液中Al3+离子不能确定,不能确定是否含有的离子是Cl-,A、A是NO,A错误;B、依据分析可知:溶液中一定存在:Fe2+、NH4+、SO42-,B错误;C、溶液E为HNO3,气体F为NH3,二者能反应生成硝酸铵,C错误;C、铝离子可能存在,可能存在氯离子,D正确;答案选D。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钠是重要的防腐剂。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。 (夹持装置和A中加热装置已略,气密性已检验)。
查阅资料:①HNO2为弱酸,室温下存在反应3HNO2==HNO3+2NO↑+H2O;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
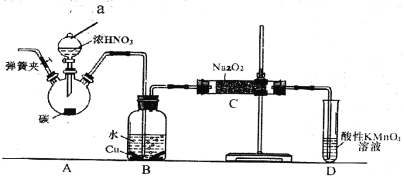
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠。
回答下列问题:
(1)装置中仪器a的名称为___________;D装置的作用是_______________。
(2)A中反应的化学方程式是___________________,C中反应生成NaNO2的化学方程式是____________。
(3)检验C中产物有亚硝酸钠的正确操作是__________
a.取少量生成物溶于水充分振荡,滴加酚酞试液,若溶液变红,则含有NaNO2。
b.取少量生成物溶于稀硫酸,若产生无色气体并在液体上方变为红棕色,则含有NaNO2。
(4)经检验C产物中亚硝酸钠含量较少。
①甲同学认为C中产物不仅有亚硝酸钠,还可能有其它固体物质。为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂应是________(写名称).
②乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是______________。
(5)NaNO2有毒,国家规定肉制品中NaNO2含量不能超过30mg/kg。从1000g隔夜熟肉, 中提取NaNO3和NaNO2后,配成溶液,再用0.00500mol/L的高锰酸钾(酸性)溶液滴定,消耗高锰酸钾溶液16.00mL,由此计算隔夜熟肉中NaNO2的含量是________mg/kg 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组准备用如下图所示的装置进行实验。现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
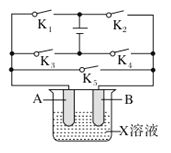
A电极 | B电极 | X溶液 | |
甲 | Cu | Zn | H2SO4 |
乙 | Pt | Pt | CuCl2 |
丙 | Fe | Cu | ? |
(1)甲同学在实验中将电键K5闭合,Zn电极上的电极反应式为______________。
(2)乙同学准备进行电解CuCl2溶液的实验,则电解时的总反应方程式为___________________。实验时应闭合的电键的组合是________(从下列五项中选择所有可能组合,第(3)小题也在这五项中选择)。
A.K1和K2
B.K1和K3
C.K1和K4
D.K2和K3
E.K2和K4
(3)丙同学准备在Fe上镀Cu,选择了用某种盐来配制电镀液,则该盐中应含的阳离子为________,实验时,应闭合的电键的组合是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年9月15日22时04分12秒,天宫二号空间实验室在酒泉卫星发射中心发射成功。2016年10月19日凌晨,神舟十一号飞船与天宫二号自动交会对接成功。天宫上的太阳能电池板的半导体材料是
A. 硅 B. 二氧化硅 C. 铝硅合金 D. 铜硅合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应属于吸热反应的是
A. 浓H2SO4溶于水 B. 生石灰溶于水
C. 镁与稀盐酸反应 D. NH4Cl固体与Ba(OH)2·8H2O混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题。
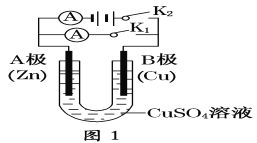

(1)根据图1回答:
①若断开K1,闭合K2,A电极可观察到的现象是________________;B极的电极反应式为___________________。
②若断开K2,闭合K1。
A电极可观察到的现象_________________________;
B极的电极反应式为__________________________。
(2)根据图2回答:
①将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应式为________________,电解反应的离子方程式为_________________。
②实验完成后,铜电极增重128 g,石墨电极产生标准状况下的气体体积________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某200 mL氯化镁和氯化铝混合液中c(Mg2+)为0.3 mol/L,c(Cl-)为1.2 mol/L。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol/L NaOH溶液的体积为
A.70 mL B.60mL C.80 mL D.128 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液、胶体和浊液这三种分散系的本质区别是( )
A. 是否为大量分子和离子的集合体
B. 分散质粒子的大小
C. 能否通过滤纸或半透膜
D. 是否均一、稳定、透明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应Zn+2FeCl3===ZnCl2+2FeCl2设计一个原电池。
(1)在下图方格内画出实验装置图,
(2)指出正极材料为__________,电极反应式为______________________;
负极材料为____________,电极反应类型为_________________________。
(3)外电路中的电子是从____________极流向__________极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com