
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献,他以饱和食盐水、NH3、CO2为原料先制得NaHCO3,进而生产出纯碱。回答下列问题:
某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)
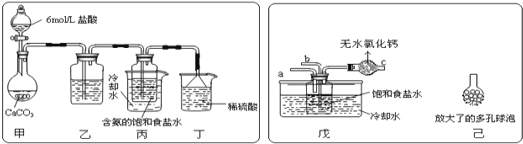
(1)丁装置中稀硫酸的作用是____。
(2)另一位同学用图中戊装置(其他装置未画出)进行实验。实验时,须先从___管通入NH3气体。
(3)有同学建议在戊装置的b管下端连接己装置,理由是_____。
(4)如表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水):
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析丙、戊装置中使用冷却水或者冰水的原因:____。
(5)该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为ag。再将晶体加热到质量不再变化时,称量所得粉末质量为mg。然后进行如图所示实验:
![]()
①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是___(填字母)。
a 在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
b 在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
c 在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②所得晶体中碳酸氢钠的纯度为___。
【答案】吸收未反应的氨气 a 增大气体与溶液接触面积,提高CO2吸收率 温度越低,碳酸氢钠的溶解度越小,便于析出 c ![]() ×100%或
×100%或![]() ×100%
×100%
【解析】
(1)实验过程中氨气可能有剩余,而稀硫酸能与氨气反应,所以稀硫酸的作用是吸收末反应的NH3。故答案为:吸收未反应的氨气;
(2)制取碳酸氢钠时先要得到含氨的饱和食盐水,氨气极易溶于水,二氧化碳能溶于水,所以应先通入氨气,所以a端通入,从而保证了从b通入二氧化碳时,二氧化碳被充分反应。故答案为:a;
(3)b管下端连接己装置,反应物二氧化碳与溶液的接触面积增大,提高了二氧化碳的吸收率。故答案为:增大气体与溶液接触面积,提高CO2吸收率;
(4)B装置中的试管内是溶有氨和氯化钠的饱和溶液,通入二氧化碳气体会发生反应生成碳酸氢钠和氯化铵,依据表中数据分析可知温度越低,碳酸氢钠的溶解度越小,所以温度越低越有利于碳酸氢钠的晶体析出。故答案为:温度越低碳酸氢钠溶解度越小,便于析出;
(5)测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为ag,此时为碳酸氢钠粗品质量,操作I将晶体加热到质量不再变化时,所得粉末为碳酸钠和杂质,然后溶解,加入氯化钙溶液,氯化钙跟碳酸钠反应生成碳酸钙,将生成的碳酸钙过滤、洗涤、干燥,称量为ng。
①为判断滴加的氯化钙溶液过量,可在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液看是否有沉淀生成,故答案为:c;
②发生反应的化学方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O,Na2CO3+CaCl2=CaCO3↓+H2O+2NaCl,得到的碳酸钙需要经过过滤、洗涤、干燥后方可称量。
Na2CO3+CO2↑+H2O,Na2CO3+CaCl2=CaCO3↓+H2O+2NaCl,得到的碳酸钙需要经过过滤、洗涤、干燥后方可称量。
方法一:设样品中碳酸氢钠的质量为x,由上两式可得关系式:
2NaHCO3~~~CaCO3
84×2 100
x n
x=![]() g,碳酸氢钠的质量分数为
g,碳酸氢钠的质量分数为 。
。
方法二:设为样品中碳酸氢钠的质量为xg,将碳酸氢钠晶体加热到质量不再变化时,依题意可知,固体减重质量为水和二氧化碳质量和为(a-m)g,依据反应:
2NaHCO3![]() Na2CO3+CO2↑+H2O m
Na2CO3+CO2↑+H2O m
84×2 62
xg (a-m)g
碳酸氢钠质量为x=![]() g,纯度=
g,纯度=![]() ×100%;
×100%;
故答案为:![]() 或
或![]() ×100%。
×100%。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)与对应的选项相符合的是( )


A.向1 L浓度均为0.1 mol·L-1的Ba(OH)2、NaAlO2混合溶液中加入0.1 mol·L-1的稀H2SO4
B.向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的稀NaOH溶液
C.向烧碱溶液中滴加明矾溶液
D.向AlCl3溶液中滴加过量氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对一含有Al3+的未知溶液进行了如下分析:(1)滴加少量NaOH溶液,无明显变化;(2)继续滴加NaOH溶液,有白色胶状沉淀生成;(3)滴加过量的NaOH溶液,白色胶状沉淀明显减少。实验小组经定量分析,得出如图所示沉淀的物质的量与滴加NaOH溶液体积的关系。下列说法错误的是( )

A. 该未知溶液中至少含有3种阳离子
B. NaOH溶液的物质的量浓度为5 mol·L-1
C. 若另一种离子为二价阳离子,则a=10
D. 若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容器中加入足量的碳酸钙,发生反应CaCO3(s)![]() CaO(s)+CO2(g),达到平衡,下列说法正确的是
CaO(s)+CO2(g),达到平衡,下列说法正确的是
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度为原来的2倍
B.CaCO3(s)加热分解生成CaO(s)和CO2(g),△S<0
C.将体积增大为原来的2倍,再次达到平衡时,气体的密度变小
D.保持容器体积不变,充入He,平衡向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上氟气可作为火箭燃料中的氧化剂。1886年法国化学家![]() 通过电解氟氢化钾
通过电解氟氢化钾![]() 的氟化氢无水溶液第一次制得氟气。已知:
的氟化氢无水溶液第一次制得氟气。已知:![]() ,制备氟气的电解装置如下图所示。下列说法错误的是( )
,制备氟气的电解装置如下图所示。下列说法错误的是( )

A. 钢电极与电源的负极相连
B. 氟氢化钾在氟化氢中可以电离
C. 阴极室与阳极室必须隔开
D. 电解过程需不断补充的X是KF。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向HCl、AlCl3混合溶液中逐滴加入NaOH溶液,生成沉淀的量随NaOH溶液加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )

A. M点对应的溶液中:K+、Fe2+、SO42-、NO3-
B. N点对应的溶液中:K+、NH4+、Cl-、CO32-
C. S点对应的溶液中:Na+、SO42-、HCO3-、NO3-
D. R点对应的溶液中:Na+、SO42-、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.电解精炼铜时,若转移2NA个电子,则阳极减少的质量为64g
B.合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率
C.![]() 在常温下能自发进行,则该反应的△H>0
在常温下能自发进行,则该反应的△H>0
D.常温下,![]() 。欲使溶液中
。欲使溶液中![]() ,需调节溶液的
,需调节溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)在标准状况下,有物质①44.8LH2,②24gCH4,③1molH2O,④3.01×1023个N2,含分子数最多的是______(填序号,下同),含电子数最多的是________,质量最大的是______,体积最小的是______;密度由小到大的顺序为________________。
(2)0.5mol某固体A的质量是40g,A的摩尔质量为_________。
(3)质量之比为8∶7的两种气体O2、CO,其分子数之比为_______________;氧原子数之比为____________;相同条件下的体积之比为________。
(4) 4.8g碳在一定量的氧气中燃烧,反应后生成CO和CO2的总质量为12.8g。则在同温同压下,生成的CO和CO2的体积比为__________。
(5)由NaHS,MgSO4,NaHSO3组成的混合物中,硫元素的质量分数为a%,则混合物中氧元素的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、某校化学小组学生利用如图所列装置进行“铁与水反应”的实验。(图中夹持及尾气处理装置均已略去)
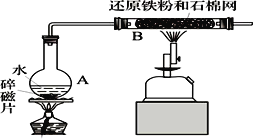
(1)烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_____________________________。装置B中发生反应的化学方程式是________________________________。
(2)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法____________________________________。
Ⅱ、利用电解实验可以制得纯净的Fe(OH)2白色沉淀,如图所示,已知两电极的材料分别为石墨和铁。
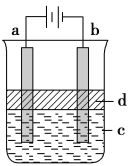
(1)a电极的材料应为__________,电极反应式为__________________。
(2)d为苯,其作用是________________。
(3)当电解一段时间后看到白色Fe(OH)2沉淀,然后向溶液中通入空气,可观察的现象是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com