
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)Z、M、W三种元素离子半径由大到小的顺序是____(填相应的离子符号)。
(2)用电子式表示M2W的形成过程___________
(3)由M、Z两元素形成的原子个数比为1∶1化合物的化学键类型是______
(4)由X、Y、Z、W四种元素组成的一种盐A,已知:①1molA能与足量NaOH浓溶液反应生成标准状况下22.4L气体。②A能与盐酸反应产生气体B,该气体能与溴水反应。写出A的化学式____,该气体B与溴水反应的离子方程式 ____。
【答案】r(S2-)>r(O2-)>r(Na+) ![]() 离子键,非极性键 NH4HSO3 SO2+Br2+2H2O=4H++2Br-+SO42-
离子键,非极性键 NH4HSO3 SO2+Br2+2H2O=4H++2Br-+SO42-
【解析】
原子序数由小到大排列的四种短周期元素X、Y、Z、W,在周期表中X是原子半径最小的元素,则X为H元素;Y、Z左右相邻,Z、W位于同主族,结合原子序数可知Y、Z处于第二周期,W处于第三周期,设Y的原子序数为a,则Z的原子序数为a+1,W的原子序数为a+9,四种元素的原子序数之和为32,则:1+a+a+1+a+9=32,解得a=7,则Y为N元素、Z为O元素、W为S元素;M元素与X同主族,与W同周期,则M为Na元素。
根据上述分析可知:X为H元素;Y为N元素、Z为O元素、W为S元素, M为Na元素。
(1)Z、M、W三种元素分别是N、O、S元素。N3-、O2-的核外有2个电子层,核电荷数越大,离子半径越小;S2-核外有3个电子层,离子核外电子层数越多,离子半径越大,所以三种离子由大到小的顺序是r(S2-)>r(O2-)>r(Na+);
(2) M2W为Na2S,该物质是离子化合物,2个Na+与S2-通过离子键结合,用电子式表示M2W的形成过程为![]() ;
;
(3)M、Z分别表示Na、O两种元素,由Na与O两元素形成的原子个数比为1∶1化合物为Na2O2,该化合物为离子化合物,Na+与O22-离子间通过离子键结合,O22-的O原子间通过非极性共价键结合,因此化合物Na2O2中含有的化学键为离子键、非极性共价键;
(4)由H、N、O、S四种元素组成的一种离子化合物A,则A为铵盐,①1molA能与足量NaOH浓溶液反应生成标准状况下22.4L气体,氨气为1mol,即1molA含有1mol铵根离子;②A能与盐酸反应产生气体B,该气体能与溴水反应,B为SO2,可推知A为NH4HSO3,二氧化硫与溴水反应得到HBr与硫酸,反应离子方程式为:SO2+Br2+2H2O=4H++2Br-+SO42-。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 某气体能使品红溶液褪色,则该气体是SO2
B. 等质量的铜按a,b两种途径完全转化为硝酸铜,途径a,b消耗的硝酸一样多:途径a:Cu![]() CuO
CuO![]() Cu(NO3)2;途径b:Cu
Cu(NO3)2;途径b:Cu![]() Cu(NO3)2
Cu(NO3)2
C. 用分别蘸有浓氨水和浓盐酸的玻璃棒相互靠近会产生白烟,也可用浓硫酸代替浓盐酸
D. 把过量Cu放入少量的稀硝酸中至完全反应后,再加入稀硫酸可以产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 足量的Fe在Cl2中燃烧只生成FeCl3
B. 铁的化学性质比较活泼,它能和水蒸气反应生成H2和Fe(OH)3
C. 用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2
D. 向某溶液中加NaOH溶液得白色沉淀,且颜色逐渐变为红褐色,说明该溶液中只含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛是生产金属钛及其化合物的重要中间体。某校化学课外活动小组准备利用下图装置制备四氯化钛(部分夹持仪器已略去)。
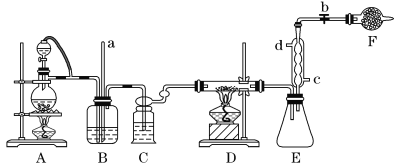
资料表明:室温下,四氯化钛为无色液体,熔点:-25 ℃,沸点:136.4 ℃。在空气中发烟生成二氧化钛固体。在650~850 ℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。回答下列问题:
(1)检查该装置气密性的方法是_______________________________________________。
(2)实验中B装置的作用是____________________。
(3)写出D装置中物质制备的化学方程式________________________________;写出四氯化钛在空气中发烟的化学方程式______________________________。
(4)E处球形冷凝管的冷却水应从________(填“c”或“d”)口通入。
(5)F装置中盛装的物质是________。
(6)该实验设计略有缺陷,请指出其不足之处:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J分别代表相关反应的一种物质。已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。
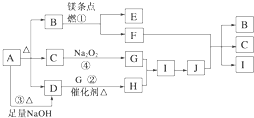
请填写以下空白:
(1)A的化学式________;B的结构式________;D的电子式________;
(2)写出反应①②的化学方程式:
①________________________________________________,
②_________________________________________。
(3)写出反应③的离子方程式:________________________________________。
(4)J与F反应的化学方程式: _________________________________________。
(5)在反应④中,当生成标况下3.36 L G时,转移电子数为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关天然产物水解的叙述不正确的是( )
A.可用碘水检验淀粉水解是否完全
B.油脂在酸性条件下水解与在碱性条件下水解程度不同,但产物完全相同
C.蛋白质水解的最终产物均为氨基酸
D.纤维素水解与淀粉水解得到的最终产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42-、CO32-、I-、Cl-中的一种或多种,进行如图所示的实验,下列说法正确的是 ( )
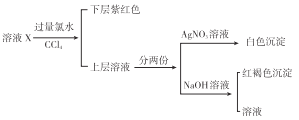
A. 溶液X中有Fe3+、SO42-
B. 溶液X中有Fe2+、I-可能有SO42-、Cl-
C. 溶液X中有I-、Cl-,无CO32-
D. 溶液X中有I-,Fe2+和Fe3+两种离子中至少有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题: H++ Mn![]() + H2C2O4→ CO2↑+Mn2++
+ H2C2O4→ CO2↑+Mn2++
(1)配平以上离子方程式,并在□中填上所需的微粒_____________________________。
(2)该反应中的还原剂是_____(填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是________________________。
②溶解沉淀时______(填“能”或“不能”)用稀盐酸,原因是__________。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙 _____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com