
【题目】X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素X的最高价氧化物的电子式为 ;元素Z的离子结构示意图为 。
(2)单质X和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为 。Y、W的氢化物沸点高的是 (写化学式),原因是 。
(3)元素W位于周期表的第 族, 其非金属性比元素R弱,用原子结构的知识解释原因 。
(4) Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为 。
【答案】(1)![]() ;
;
(2)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;NH3;分子之间存在氢键;
CO2↑+4NO2↑+2H2O;NH3;分子之间存在氢键;
(3)第三周期第VA;P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱;
(4)Al2O3+3C+ N2 ![]() 2AlN+3CO。
2AlN+3CO。
【解析】试题分析:X、Y、Z、W、R是短周期元素,原子序数依次增大,X原子核外各层电子数之比为1:2,X有2个电子层,X是C元素。 Y的氧化物和R的氧化物均能形成酸雨,则Y为N元素、R为S元素;W和R是同周期相邻元素,则W为P元素;Y原子和Z原子的核外电子数之和为20,则Z原子核外电子数=20-7=13,则Z为Al元素。(1)元素X的最高价氧化物是CO2,其电子式为![]() ;(2)单质X和元素Y的最高价氧化物对应水化物HNO3的浓溶液在加热时会发生氧化还原反应,产生CO2、NO2和水,发生反应的化学方程式为C+4HNO3(浓)
;(2)单质X和元素Y的最高价氧化物对应水化物HNO3的浓溶液在加热时会发生氧化还原反应,产生CO2、NO2和水,发生反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;N、P是同一主族的元素,元素的氢化物的化学式分别是NH3、PH3,由于在氨的分子之间存在氢键,增加了分子之间的吸引力,使物质的熔沸点升高,所以Y、W的氢化物沸点高的是NH3;(3)元素W是P,在元素周期表中位于第三周期第VA;P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱,故P的非金属性比元素S弱;(4)N和Al组成的化合物AlN,被大量用于制造电子元件.工业上用氧化铝、碳、氮气在高温下制备,其中氧化铝和碳的物质的量之比为1:3,说明还生成CO,则该反应的化学方程式为:Al2O3+3C+ N2
CO2↑+4NO2↑+2H2O;N、P是同一主族的元素,元素的氢化物的化学式分别是NH3、PH3,由于在氨的分子之间存在氢键,增加了分子之间的吸引力,使物质的熔沸点升高,所以Y、W的氢化物沸点高的是NH3;(3)元素W是P,在元素周期表中位于第三周期第VA;P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱,故P的非金属性比元素S弱;(4)N和Al组成的化合物AlN,被大量用于制造电子元件.工业上用氧化铝、碳、氮气在高温下制备,其中氧化铝和碳的物质的量之比为1:3,说明还生成CO,则该反应的化学方程式为:Al2O3+3C+ N2 ![]() 2AlN+3CO。
2AlN+3CO。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO![]() 、CO
、CO![]() 等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液体积变化的图像如图所示,下列说法正确的是( )
等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液体积变化的图像如图所示,下列说法正确的是( )
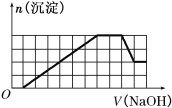
A.原溶液中含有的阳离子是H+、Fe3+、Al3+
B.原溶液中一定含有SO![]() 和Na+
和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1∶1
D.反应最后形成的溶液中含有的溶质为Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:①SiO2 + 2C![]() Si + 2CO
Si + 2CO
精炼硅:②Si + 3HCl![]() SiHCl3 + H2
SiHCl3 + H2
③SiHCl3 + H2![]() Si + 3HCl
Si + 3HCl
化学反应与能量变化如图所示,回答下列问题:
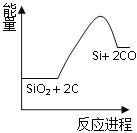
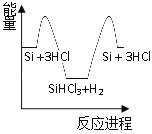
(1)反应①是_________反应(填“吸热”或“放热”),反应②是_________反应(填“吸热”或“放热”)。
(2)反应③破坏反应物中的化学键所吸收的能量_________形成生成物中化学键所放出的能量(填“大于”或“小于”)。
(3)研究物质变化时,人们可以从不同角度、不同层面来认识物质变化时所引起的化学键及能量变化。据此判断下列说法错误的是_________(双选)。
A.金属钠和氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量降低
B.等量的硫蒸气和硫固体分别完全燃烧,前者放出的能量多
C.氮气分子内部存在着很强的共价键,故通常状况下氮气的化学性质很活泼
D.由石墨制取金刚石是吸热反应,可知金刚石比石墨稳定
E.由放热反应H2 + Cl2 ==== 2HCl来说,断裂1mol H—H键和1molCl—Cl键所吸收的能量小于形成2molH—Cl键所放出的能量
(4)在研究化学反应中的能量变化时,我们通常做下面的实验:
在一个小烧杯里,加入20g已经研磨成粉末的氢氧化钡晶体【Ba(OH)2.8H2O】,将小烧杯放在事先已滴有3—4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,并立即用玻璃棒迅速搅拌。写出实验过程中发生反应的化学方程式_________,该反应中反应物总能量_________生成物的总能量(填“大于”或“小于”),实验过程中立即用玻璃棒迅速搅拌的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为___________;
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g)![]() H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
(4)Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
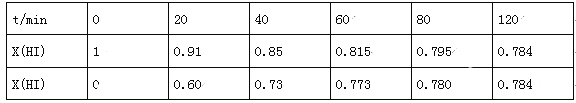
①根据上述实验结果,该反应的平衡常数K的计算式为:___________;
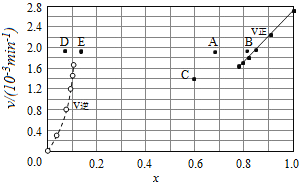
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为___________(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=___________min-1.
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为___________(填字母).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~M有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与NaHCO3溶液反应,F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色,D能发生银镜反应,M与足量的NaOH溶液反应后的产物,其一氯代物只有一种。
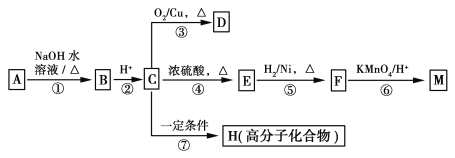
已知: (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)
请回答:
(1)B的结构简式为________________________。
(2)反应①~⑦中,属于氧化反应的是________(填反应序号)。
(3)写出反应④的化学方程式______________________________________________。
(4)D与新制Cu(OH)2悬浊液反应的化学方程式为______________________________。
(5)A的相对分子质量在180~260之间,从以上转化中不能确认A中的某一官能团,下列确定该官能团的哪些实验方法是正确的________。
a.取少量A于试管中,再加入苯振荡,观察分液后上层溶液颜色
b.取少量A于试管中,再加入NaOH溶液共热,待冷却后加入稀硝酸调节至酸性,最后滴入AgNO3溶液,观察沉淀颜色
c.取少量A于试管中,再滴入AgNO3溶液,再加入稀硝酸,观察沉淀颜色
d.取少量A于试管中,再加入NaOH的醇溶液共热,待冷却后加入稀硝酸调节至酸性,最后滴入AgNO3溶液,观察沉淀颜色
(6)符合下列条件的F的同分异构体共有________种。
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1∶1∶2∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的综合利用对于改善大气质量和能源充分利用有重要的意义。
(1)下列说法正确的是 (填序号)。
a.煤是由有机物和少量无机物组成的复杂混合物
b.煤在燃烧过程中会生成一氧化碳、二氧化碳、氮氧化物、烟尘等有害物质
c.可利用生石灰、熟石灰、石灰石等固硫剂使煤在燃烧过程中生成稳定的硫酸盐
d.煤的干馏属于化学变化,煤的气化和液化都属于物理变化
(2)煤的气化过程中产生的有害气体H2S用氨水吸收生成正盐的离子方程式是
。
(3)燃煤烟气的一种脱硫方案-火碱-石灰-石膏法流程图1如下:
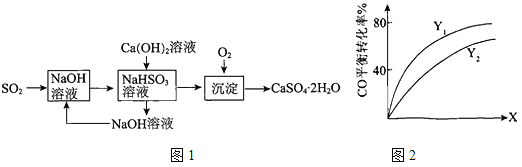
①常温下,用NaOH溶液吸收SO2得到pH=6的NaHSO3溶液,该溶液中离子浓度的大小顺序是
。
②氢氧化钙与NaHSO3反应的化学方程式是 。
(4)煤的间接液化法合成二甲醚的三步反应如下:
Ⅰ.2H2(g)+CO(g) ![]() CH3OH(g) △H=-90.8kJ·mol-1
CH3OH(g) △H=-90.8kJ·mol-1
Ⅱ.2CH3OH(g) ![]() CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
Ⅲ.CO(g) + H2O(g) ![]() CO2(g) + H2(g) △H=-41.3 kJ·mol-1
CO2(g) + H2(g) △H=-41.3 kJ·mol-1
① 总反应热化学方程式:3H2(g)+ 3CO(g) ![]() CH3OCH3(g)+ CO2(g) △H=
CH3OCH3(g)+ CO2(g) △H=
② Y(Y1、Y2),X可分别代表压强或温度。如图2表示Y一定时,总反应中CO的平衡转化率随X的变化关系。判断Y1、Y2的大小关系,并简述理由:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯的球棍模型如图所示(图中球与球之间连线表示 单键或双键)。
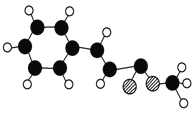
(1)肉桂酸甲酯的分子式为 。
(2)肉桂酸甲酯能发生的反应类型是 (填字母代号)。
A.加成反应 B.酯化反应 C.消去反应 d 取代反应
(3)肉桂酸甲酯与NaOH溶液反应生成的相对分子质量较小的有机物的结 构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
活动一:查阅资料
NaNO2有毒,具有氧化性和还原性,NaNO2溶液显碱性,肉类在放置过程中,NaNO3逐渐转化为NaNO2,国家规定肉制品中NaNO2含量不能超过30 mg/kg。
活动二:鉴别NaNO2与食盐
(1)NaNO2与食盐的外观相似,易被当成食盐误用,分析以下两种鉴别方法:
① 能否各取少许固体用舌头品尝?_____。(选填“能”或“不能”)
② 用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是NaNO2具有___性。
活动三:探究NaNO3与NaNO2的相互转化
(2)制取NaNO2与NaNO3混合溶液的装置如图所示。
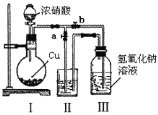
已知:2NO2+2NaOH=NaNO2+NaNO3+H2O。
① 写出装置I中发生反应的化学方程式___________________________________。
② 水_______(选填“能"或“不能”)作为装置II中的试剂,理由是_________________。
③ 装置III中反应完全后,接下来的操作是_________________________________。
(3)将NaNO2与NaNO3混合溶液露置于空气,隔夜后,测得溶液的pH减小,则溶液中NaNO2的含量_______(选填“增多”、“减少"或“不变”),原因可能是______________(用化学方程式解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):

(1) 哪一时间段(指①0~1、②1~2、③2~3、④3~4、⑤4~5 min,下同)反应速率最大 ,(填序号,下同) ,原因是 。
(2) 哪一段时段的反应速率最小 ,原因是 。
(3) 求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,不要求写出计算过程) 。
(4) 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:[A.蒸馏水 B.NaCl溶液 C Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com