
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为___________;
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g)![]() H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
(4)Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
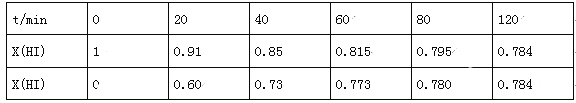
①根据上述实验结果,该反应的平衡常数K的计算式为:___________;
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为___________(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=___________min-1.
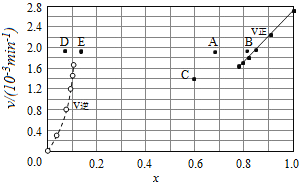
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为___________(填字母).
【答案】
(1)MnSO4;
(2)4.7×10-7;
(3)299kJ;
(4)①![]() ;②
;②![]() ;1.95×10-3;③A;E
;1.95×10-3;③A;E
【解析】
试题分析:(1)海藻中的碘元素以碘化物形式存在,反应中I元素发生氧化反应,Mn元素被还原,还原产物应为硫酸锰,故答案为:MnSO4;
(2)当AgCl开始沉淀时,说明溶液中的c(I-)和c(Cl-)均已达到饱和状态,因此可以根据溶度积表达式进行计算,溶液中![]() =
=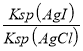 =
=![]() =4.7×10-7,故答案为:4.7×10-7;
=4.7×10-7,故答案为:4.7×10-7;
(3)设1molHI(g)分子中化学键断裂时需吸收的能量为x kJ,则:2x kJ-436kJ-151kJ=11kJ,解得x=299,故答案为:299kJ;
(4)①表中第一列,由HI分解建立平衡,表中第二列向逆反应进行建立平衡,由第一列数据可知,平衡时HI物质的量分数为0.784,则氢气、碘蒸汽总物质的量分数为1-0.784=0.216,而氢气、与碘蒸汽物质的量分数相等均为0.108,反应前后气体体积不变,用物质的量分数代替浓度计算平衡常数,则平衡常数K=![]() =
=![]() ,故答案为:
,故答案为:![]() ;
;
②到达平衡时,正、逆反应速率相等,则k正x2(HI)=k逆x(H2)x(I2),则k逆=k正×![]() =
=![]() ,
,
在t=40min时,正反应建立平衡的x(HI)=0.85,则v正=k正x2(HI)=0.0027min-1×0.852=1.95×10-3min-1,故答案为:![]() ;1.95×10-3;
;1.95×10-3;
③对于2HI(g)![]() H2(g)+I2(g)反应建立平衡时:升高温度,正、逆反应速率均加快,因此排除C点,正反应为吸热反应,升高温度,平衡向吸热反应方向移动,因此平衡正向移动,再次平衡时HI的物质的量分数减小,因此排除B点,故选A点;对于H2(g)+I2(g)
H2(g)+I2(g)反应建立平衡时:升高温度,正、逆反应速率均加快,因此排除C点,正反应为吸热反应,升高温度,平衡向吸热反应方向移动,因此平衡正向移动,再次平衡时HI的物质的量分数减小,因此排除B点,故选A点;对于H2(g)+I2(g)![]() 2HI(g)反应建立平衡时:升高温度,正、逆反应速率均加快,升高温度,平衡向吸热反应方向移动,因此平衡逆向移动,再次平衡时H2的物质的量分数增大,故选E点;因此反应重新达到平衡,v正~x(HI)对应的点为A,v逆~x(H2)对应的点为E,故答案为:A;E。
2HI(g)反应建立平衡时:升高温度,正、逆反应速率均加快,升高温度,平衡向吸热反应方向移动,因此平衡逆向移动,再次平衡时H2的物质的量分数增大,故选E点;因此反应重新达到平衡,v正~x(HI)对应的点为A,v逆~x(H2)对应的点为E,故答案为:A;E。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据化学反应中的能量变化关系回答下列问题:
(1)断开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,求:
①1molN2生成NH3需______(填“吸收”或“放出”)能量______kJ;
②1molH2生成NH3需______(填“吸收”或“放出”)能量______kJ。
(2)航天飞船可用肼(N2H4)作动力源。已知1mol液态肼和足量的液态过氧化氢反应生成氮气和水蒸气时放出641.6kJ热量,化学方程式如下:N2H4+2H2O2===N2↑+4H2O。
①该反应中肼作 (填氧化或还原)剂;
②该反应的反应物总能量 (填高于或低于)生成物的总能量;
③此情况下,液态肼燃烧生成0.5molN2时放出的热量为 kJ;
④肼(N2H4)分子中存在的化学键有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景。
(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH =-44.0 kJ/mol
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为________
(2)某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。
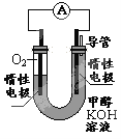
①工作一段时间后,测得溶液的pH 。(填“增大”“减小”“不变”)
②该电池负极的电极反应为 。
(3)某金属的相对原子质量为52.00,用上述电池电解该金属的一种含氧酸盐的酸性水溶液时,阳极每放出3 360 mL(标准状况)氧气,阴极析出金属10.4 g,在该含氧酸盐中金属的化合价为 ,
在该实验中,若不考虑能量的损失,电池中消耗甲醇的质量最少是 g(结果精确至0.1 g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
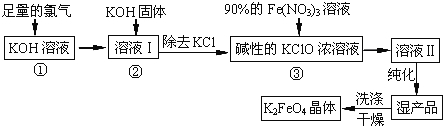
(1)反应①应在温度较低的情况下进行.因在温度较高时KOH 与Cl2 反应生成的是KClO3.写出在温度较高时KOH 与Cl2反应的化学方程式 ;
(2)在反应液I中加入KOH固体的目的是 (填编号);
A.与反应液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,其离子反应是: FeO42﹣+ H2O= Fe(OH)3(胶体)+ O2↑+
完成并配平上述反应的离子方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2S 可用于制防污涂料,其可由热的铜在硫蒸气或H2S 中反应制得。
(1)铜元素在元素周期表中的位置为 ____________,Cu+的核外电子排布式为_________,基态铜原子核外电子共有__________种运动状态。
(2)Cu2S在一定条件下可被氧化为CuSO4。
①在SO42—中S原子的杂化轨道类型为________;SiO44—、PO43—与 SO42—互为________;其中Si、P、S第一电离能由大到小顺序为________________ ;
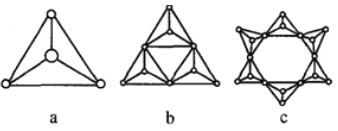
②硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元,硅氧四面体可以用图a 表示,图中b、c 是硅氧四面体结合成环状结构的两个例子,若在环状结构中硅的原子数为n,写出环状结构中硅酸根离子的通式_______________。
(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH),二者部分物理性质如下:
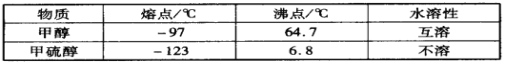
甲醇和甲硫醇在熔沸点和水溶性方面性质差异的原因是__________________________。
(4)某化合物由S、Fe、Cu 三种元素组成,其晶胞结构如下图所示(1 pm=10-10cm),该晶胞上下底面为正方形,侧面与底面垂直,则该晶体的密度ρ=_________g/cm3(保留三位有效数字)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由环己烷可制得1,4-环己二醇,流程如下(其中无机产物都已略去),试回答:

(1)反应_________属于取代反应(填反应序号).
(2)化合物的结构简式:B______________,C_______________.
(3)反应⑥所用试剂和条件是________________________.
(4)写出反应②、⑤的化学方程式:反应②________________反应⑤__________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素X的最高价氧化物的电子式为 ;元素Z的离子结构示意图为 。
(2)单质X和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为 。Y、W的氢化物沸点高的是 (写化学式),原因是 。
(3)元素W位于周期表的第 族, 其非金属性比元素R弱,用原子结构的知识解释原因 。
(4) Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某人设计淀粉利用方案如图所示。其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
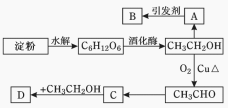
(1)C6H12O6的名称是________,A的电子式为_________,C中含有官能团名称 ;
(2)A→B反应类型____________;C→D反应类型____________。
(3)写出下列转化的化学方程式:
① A→B:______________________________________________________;
② A→CH3CH2OH:______________________________________;
③ C→D:_____________________________________________________;
④ CH3CH2OH→CH3CHO:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物
(1)工业上尿素由CO2和NH3合成,写出其方程式 ___________________________.
(2)当氨碳比![]() 时,CO2的转化率随时间的变化关系如图所示。
时,CO2的转化率随时间的变化关系如图所示。

①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”)。
②NH3的平衡转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com