
【题目】石油裂化和裂解过程得到的CH2=CH2,在一定条件下可以聚合成高分子化合物。含有 结构的化合物与CH2=CH2一样,可以在一定条件下聚合成高分子化合物。
结构的化合物与CH2=CH2一样,可以在一定条件下聚合成高分子化合物。
(1)广泛用作农用薄膜的聚氯乙烯塑料,是由CH2=CHCl在催化剂、加热的条件下聚合成的,其化学方程式是________________。
(2)电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯( ),它是由________________(写结构简式)聚合而成的。
),它是由________________(写结构简式)聚合而成的。
(3)CH2=CHCl与聚苯乙烯的单体在一定条件下可发生加聚反应,所得产物的结构简式为________________。
科目:高中化学 来源: 题型:
【题目】常温下,两种溶液① 0.1 mol/L NH3·H2O ② 0.1 mol/L NH4Cl 中:
(1)溶液①的 pH_______7(填“>”、“<”或“=”),其原因是_________(用离子方程式表示)。
(2)溶液②呈_______性(填“酸”、“碱”或“中”)。水解反应是吸热反应,升温可以_______(填“促进”或“抑制”)NH4Cl 的水解。
(3)两种溶液中 c(![]() ) 的大小为_____(填字母)。
) 的大小为_____(填字母)。
a.两种溶液中 c(![]() ) 都等于 0.1 mol/L
) 都等于 0.1 mol/L
b.两种溶液中 c(![]() ) 都小于 0.1 mol/L
) 都小于 0.1 mol/L
c.NH4Cl 溶液中 c(![]() ) 小于 NH3·H2O 溶液中 c(
) 小于 NH3·H2O 溶液中 c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有CH4、C2H4、C2H6三种有机化合物:
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是__________。
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是__________。
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是__________,生成水最多的是__________。
(4)在120℃、1.01×105Pa时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图二的碎纸片补充到图一中,可得到一个完整的离子方程式。对该离子方程式说法正确的是

A. 配平后的化学计量数依次为3、1、2、6、3
B. 若有1mol的S被氧化,则生成2mol S2-
C. 氧化剂与还原剂的物质的量之比为1:2
D. 2mol的S参加反应有3mol的电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在工业生产和日常生活中有重要用途。
在工业生产和日常生活中有重要用途。
I.工业上用钛矿石![]() ,含FeO、
,含FeO、![]() 、
、![]() 等杂质
等杂质![]() 经过下述反应制得:
经过下述反应制得:

其中,步骤![]() 发生的反应为:
发生的反应为:![]() 。
。
![]() 净化钛矿石时,是否需要除去杂质FeO?答: ______
净化钛矿石时,是否需要除去杂质FeO?答: ______ ![]() 填“需要”或“不需要”
填“需要”或“不需要”![]() 。
。
![]() 净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: ______; ______。
净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: ______; ______。
![]() 可通过下述两种方法制备金属钛:
可通过下述两种方法制备金属钛:
“方法一”是电解![]() 来获得Ti:将处理过的
来获得Ti:将处理过的![]() 作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
![]() 阴极反应的电极反应式为 ______。
阴极反应的电极反应式为 ______。
“方法二”是先将![]() 与
与![]() 、C反应得到
、C反应得到![]() ,再用镁还原得到
,再用镁还原得到![]() 。因下述反应难于发生:
。因下述反应难于发生:
![]() 所以不能直接由
所以不能直接由![]() 和
和![]() 反应
反应![]() 即氯化反应
即氯化反应![]() 来制取
来制取![]() 。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
![]() 已知:
已知:![]()
![]() 。请写出
。请写出![]() 与
与![]() 、C反应制各
、C反应制各![]() 的热化学方程式: ______。
的热化学方程式: ______。
![]() 从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因_______________。
从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌![]() 是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图所示。
是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图所示。
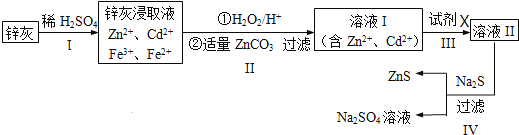
![]() 为提高锌灰的浸取率,不宜采用的方法是______
为提高锌灰的浸取率,不宜采用的方法是______![]() 填序号
填序号![]() 。
。
![]() 研磨
研磨 ![]() 多次浸取
多次浸取 ![]() 升高温度
升高温度 ![]() 加压
加压 ![]() 搅拌
搅拌
![]() 步骤Ⅱ中
步骤Ⅱ中![]() 的作用是______,所得滤渣的主要成分是______
的作用是______,所得滤渣的主要成分是______![]() 写化学式
写化学式![]() 。
。
![]() 步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为______。
步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为______。
![]() 步骤Ⅳ还可以回收
步骤Ⅳ还可以回收![]() 来制取
来制取![]() 。
。
![]() 检验ZnS固体是否洗涤干净的方法是______。
检验ZnS固体是否洗涤干净的方法是______。
![]() 可由等物质的量的
可由等物质的量的![]() 和
和![]() 在高温、催化剂条件下制取,化学反应方程式为______。
在高温、催化剂条件下制取,化学反应方程式为______。
![]() 若步骤Ⅱ加入的
若步骤Ⅱ加入的![]() 为b mol,步骤Ⅲ所得Cd为d mol,最后得到V L,c
为b mol,步骤Ⅲ所得Cd为d mol,最后得到V L,c ![]() 的
的![]() 溶液。则理论上所用锌灰中含有锌元素的质量为______。
溶液。则理论上所用锌灰中含有锌元素的质量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和氯化钠溶液制取氢氧化钠的工艺流程:
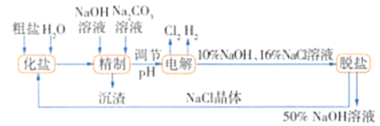
依据图中所给信息,完成下列填空:
(1)电解时发生反应的化学方程式为________________。
(2)粗盐含Ca2+、Mg2+等杂质,加入NaOH溶液、Na2CO3溶液的目的就是除去这些杂质,但如果精制时发现其中SO42-含量也较高,必须添加含钡离子的试剂除去SO42-,该试剂可以是________(填序号)。
a. Ba(OH)2溶液 b.Ba(NO3)2溶液 c.BaCl2溶液
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为________(填序号)。
a.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂
b.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液
c.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)在不同条件下分解产物不同,200℃ 时在Cu表面分解的机理如图1。已知200℃ 时:反应 I: 3N2H4(g)=N2(g)+4NH3(g) △Hl=-32.9 kJ·molˉ1 反应II: N2H4(g)+H2(g)=2NH3(g) △H2=-41.8 kJ·molˉ1,下列说法不正确的是
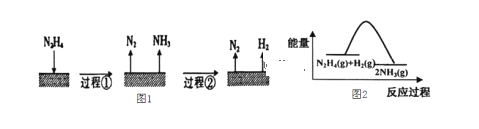
A.图l所示过程①、②都是放热反应
B.反应Ⅱ的能量过程示意图如图2所示
C.断开3 mol N2H4(g)中的化学键吸收的能量小于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量
D.200℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2(g) △H=+50.7 kJ·molˉ1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com