
| 操 作 步 骤 | 实验现象 | 结 论 |
| 步骤I:取少量待检液于试管中, 。 | | 溶液中含有Fe2+ |
| 步骤II:取少量待检液于试管中, 。 | | 溶液中含有NH4+ |
| 操作步骤 | 实验现象 |
| 先滴加几滴0.1mol/L KSCN溶液,再滴加适量的新制氯水,振荡 | 开始时无明显现象;然后溶液呈(血)红色 |
| 滴加适量的NaOH浓溶液,加热,将蘸有浓盐酸的玻璃棒靠近试管口。 | (溶液中产生气泡,管口) 产生白烟 |


科目:高中化学 来源:不详 题型:单选题
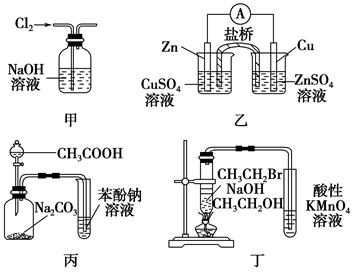
| A.图甲:除去Cl2中含有的少量HCl |
| B.图乙:构成锌—铜原电池 |
| C.图丙:根据实验现象推知酸性CH3COOH>H2CO3>C6H5OH |
| D.图丁:验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
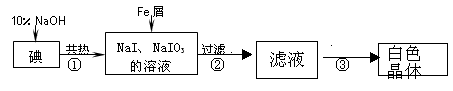
| 实验方案 | 实验现象 | 结论 |
| 将白色晶体溶于水,并滴2滴淀粉溶液 | 得到无色溶液 |  |
| 取少量溶液液于试管A中, . | 溶液显蓝色 | 溶液中含IO3一 |
| 另取少量溶液液于试管B中, . | . | 溶液中含大量0H一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
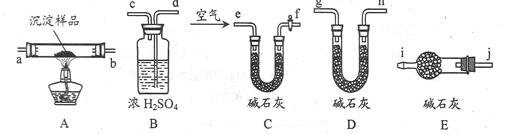
| 实验步骤 | 预期现象 | 结论 |
| ①称量B、D的质量分别为ml、m2,将装置按 f→a→b→___→___→___→___→j→i顺序连接。 | | |
| ②称取一定质量的沉淀______________________,然后___________________,冷却后再称量B、D的质量分别为m3、 m4 | (1)若m1 = m3,m2 < m4 (2)若m1___m3,m2___m4 (3)若ml___m3,m2___m4 | (1)假设1成立 (2)假设2成立 (3)假设3成立 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验方法 | 解释或结论 |
| A | 检验CH2=CH-CHO中含碳碳双键 | 将丙烯醛溶液滴入溴水中,溴水褪色 | 丙烯醛中碳碳双键与溴单质发生了加成反应 |
| B | 确认某无机酸浓溶液的溶质 | 用蘸有浓氨水的玻璃棒放于试剂瓶口,有大量白烟 | 该无机酸一定为盐酸 |
| C | 鉴别一份红棕色气体成分 | 湿润的淀粉碘化钾试纸插入气体中,试纸变蓝 | 该气体一定为Br2 |
| D | 探究高级脂肪酸甘油酯水解的条件 | 高级脂肪酸甘油酯中加入NaOH溶液加热后不再分层 | 高级脂肪酸甘油酯发生皂化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
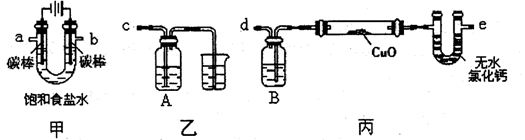
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤③⑥ | B.①④②③⑤⑥ |
| C.①④②⑥③⑤ | D.①⑤③④⑥② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验编号 | T/K | 催化剂的用量/ g | KMnO4酸性溶液的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和______探究催化剂对该反应速率的影响 |
| ② | | | | |
| ③ | | | | |
| ④ | | 0 | |
| KMnO4酸性溶液 的浓度 / mol?L-1 | 溶液褪色所需时间 t / min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com