
| A.①②④⑤③⑥ | B.①④②③⑤⑥ |
| C.①④②⑥③⑤ | D.①⑤③④⑥② |


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| | 实验内容 | 实验目的 |
| A | 将SO2通入品红溶液中,品红褪色;加热褪色后品红溶液,溶液恢复红色 | 证明亚硫酸的不稳定性 |
| B | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下KSP(BaSO4)>KSP(BaCO3) |
| C | 常温下测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于CH3COOH |
| D | 将浓硫酸和碳混合加热,直接将生成的气体通入足量的澄清石灰水,石灰水变浑浊 | 检验气体产物中CO2的存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 操 作 步 骤 | 实验现象 | 结 论 |
| 步骤I:取少量待检液于试管中, 。 | | 溶液中含有Fe2+ |
| 步骤II:取少量待检液于试管中, 。 | | 溶液中含有NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
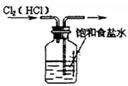 |  | 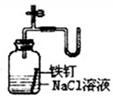 | 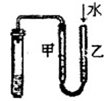 |
| ①除去Cl2中的HCl杂质 | ②用铜和稀硝酸制取少量NO | ③证明铁生锈时空气参与反应 | ④检验装置气密性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.图1探究NaHCO3的热稳定性 |
| B.图2证明铁生锈与空气有关 |
| C.图3定量测定H2O2的分解速率 |
| D.图4证明CH3CH2OH发生消去反应生成了乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
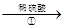 浸出液
浸出液
 滤液
滤液
 滤液
滤液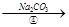
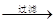 滤饼
滤饼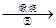 ZnO
ZnO查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
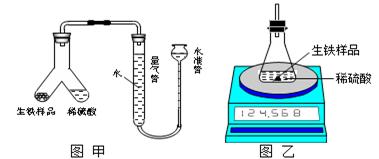
| 反应前:整套装置+ 稀硫酸质量/g | 反应前: 生铁样品质量/g | 反应后:整套装置+ 锥形瓶中剩余物的质量/g |
| a | m | b |
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入生铁样品的质量/g | 1.43 | 2.86 | 8.58 |
| 生成气体的体积/L(标准状况) | 0.56 | 1.12 | 2.24 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com