
【题目】从明矾[KAl(SO4)2·12H2O]制备Al、K2SO4和H2SO4的流程如下:

明矾焙烧的化学方程式为:4KAl(SO4)2·12H2O+3S![]() 2K2SO4+2Al2O3+9SO2↑+48H2O
2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂是_________________。
(2)步骤②中,为提高浸出率,可采取的措施有_____________。
A.粉碎固体混合物 B.降低温度 C.不断搅拌 D.缩短浸泡时间
(3)从水浸后的滤液中得到K2SO4晶体的方法是__________。
(4)步骤③电解的化学方程式是_______________,电解池的电极是用碳素材料做成,电解过程中,阳极材料需要定期更换,原因是:_________。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,则该电池的正极电极反应式是_________________________________。
(6)焙烧a吨明矾(摩尔质量为b g/mol),若SO2的转化率为96%,可生产质量分数为98%的H2SO4质量为______________________吨(列出计算表达式)。
【答案】KAl(SO4)2·12H2O AC 蒸发结晶 ![]() 阳极中碳被氧化成CO2(CO) NiO(OH)+H2O+e-=Ni(OH)2+OH-
阳极中碳被氧化成CO2(CO) NiO(OH)+H2O+e-=Ni(OH)2+OH- ![]() 或
或![]()
【解析】
(1)反应4KAl(SO4)2·12H2O+3S![]() 2K2SO4+2Al2O3+9SO2↑+48H2O中,明矾中部分S元素的化合价由+6价降为+4价,S单质中S的化合价由0价升至+4价,因此反应中的氧化剂是明矾(KAl(SO4)2·12H2O),还原剂是单质S。
2K2SO4+2Al2O3+9SO2↑+48H2O中,明矾中部分S元素的化合价由+6价降为+4价,S单质中S的化合价由0价升至+4价,因此反应中的氧化剂是明矾(KAl(SO4)2·12H2O),还原剂是单质S。
(2)步骤②是水浸明矾焙烧后的固体混合物,因此要提高浸出率,往往需要增大接触面积、充分溶解,因此粉碎固体混合物、不断搅拌都是可行的,答案选AC。
(3)焙烧后的固体混合物是K2SO4和Al2O3,水浸后的溶液则是易溶于水的K2SO4溶液,从硫酸钾溶液中获得K2SO4晶体的方法是:蒸发结晶。
(4)电解熔融氧化铝制备铝单质,反应方程式为![]() ;在电解过程中阴极得到单质铝,阳极得到O2,由于阳极电极材料是C单质,所以在高温环境下,碳素材料会被氧气氧化为CO或CO2,从而导致阳极碳素电极受损,要定期更换。
;在电解过程中阴极得到单质铝,阳极得到O2,由于阳极电极材料是C单质,所以在高温环境下,碳素材料会被氧气氧化为CO或CO2,从而导致阳极碳素电极受损,要定期更换。
(5)以Al和NiO(OH)为电极构成的碱性电池,单质Al做负极,NiO(OH)为正极,放电时正极得到电子被还原,从Ni的化合价变化可以得出得失电子数目,所以充分运用电荷守恒、原子守恒,再结合反应环境可以得正极的电极反应式为NiO(OH)+H2O+e-=Ni(OH)2+OH-。
(6)n[KAl(SO4)2·12H2O]=![]() mol,根据方程式4KAl(SO4)2·12H2O+3S
mol,根据方程式4KAl(SO4)2·12H2O+3S![]() 2K2SO4+2Al2O3+9SO2↑+48H2O,明矾煅烧生成的n(SO2)=
2K2SO4+2Al2O3+9SO2↑+48H2O,明矾煅烧生成的n(SO2)=![]() n[KAl(SO4)2·12H2O]=
n[KAl(SO4)2·12H2O]=![]() ×
×![]() mol,根据S守恒,生成的硫酸物质的量n(H2SO4)=
mol,根据S守恒,生成的硫酸物质的量n(H2SO4)=![]() ×
×![]() mol×96%,则生产质量分数为98%的H2SO4的质量
mol×96%,则生产质量分数为98%的H2SO4的质量![]() ×
×![]() mol×96%÷98%×98g/mol=
mol×96%÷98%×98g/mol=![]() g=
g=![]() 吨。
吨。


科目:高中化学 来源: 题型:
【题目】如下图,向Ⅰ中充入1molX、1molY,向Ⅱ中充入2molX、2molY,起始时Ⅰ、Ⅱ的体积相等都等于a L,在相同温度和催化剂存在的条件下,两容器中各自发生下述反应,X(g)+Y(g)![]() 2Z(g)+W(g) ΔH<0。Ⅰ保持恒压,Ⅱ保持恒容,达平衡时,Ⅰ的体积为1.4a L。下列说法错误的是
2Z(g)+W(g) ΔH<0。Ⅰ保持恒压,Ⅱ保持恒容,达平衡时,Ⅰ的体积为1.4a L。下列说法错误的是
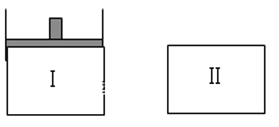
A.Ⅰ容器中X的转化率为80%
B.从起始到平衡所需时间:Ⅰ>Ⅱ
C.平衡时Y体积分数:Ⅰ<Ⅱ
D.平衡时的压强:PⅡ>2PⅠ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向10mL ![]() 的HR溶液中逐滴滴入
的HR溶液中逐滴滴入![]() 的
的![]() 溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是
溶液,所得溶液pH及导电性变化如下图。下列分析不正确的是![]()
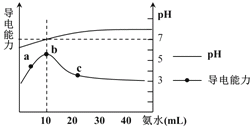
A.![]() 点导电能力增强说明HR为弱酸
点导电能力增强说明HR为弱酸
B.b点溶液![]() 说明
说明![]() 没有水解
没有水解
C.c 点溶液存在![]() 、
、![]()
D.![]() 任意点溶液均有
任意点溶液均有![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁黑(Fe3O4)是常见的铁系颜料。一种制取铁黑的实验流程如图所示:

制取铁黑的反应原理可表示为:![]()
(1)保存FeSO4溶液时,常在试剂瓶中加入铁粉,其目的是______________________________。
(2)加入氨水调pH时,发生反应的离子方程式_______________________________________。
(3)Fe(OH)2在空气被氧化为Fe(OH)3,写出反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
(1)铝灰中氧化铝与硫酸反应的化学方程式为 。
(2)用图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为 (填选项编号)。
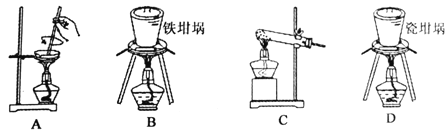
(3)在实验流程中,加30%的H2O2溶液发生的离子反应方程式为 。
(4)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为 。
(5)若用调节pH溶液“沉铁”,则得到Fe(OH)3,已知:25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O![]() Fe(OH)3+3H+的平衡常数为 。
Fe(OH)3+3H+的平衡常数为 。
(6)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
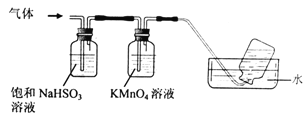
①集气瓶中收集到的气体是 (填化学式)。
②KMnO4溶液褪色,发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿![]() 主要成分为
主要成分为![]() ,还有少量的
,还有少量的![]() 等杂质
等杂质![]() 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:

(1)![]() 和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
(2)沉淀M中除含有泥沙外,一定还含有_______,固体N是_______;
(3)滤液X中,含铝元素的溶质的化学式为______,它属于_____![]() 填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐”![]() 类物质;
类物质;
(4)实验室里常往![]() 溶液中加入___________
溶液中加入___________![]() 填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液”![]() 来制取
来制取![]() ;
;
(5)将铝粉和氧化铁的混合物点燃,反应放出大量的热量,生成的液态的铁用来焊接铁轨。请写出反应的化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法不正确的是( )

A.这些离子中结合H+能力最强的是B
B.A,B,C,D,E五种微粒中A最稳定
C.C→B+D的反应,反应物的总键能大于生成物的总键能
D.B→A+D是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com