
【题目】工业上用铝土矿![]() 主要成分为
主要成分为![]() ,还有少量的
,还有少量的![]() 等杂质
等杂质![]() 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:

(1)![]() 和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
和II步骤中分离溶液和沉淀的操作为_________,所用到的玻璃仪器是:________;
(2)沉淀M中除含有泥沙外,一定还含有_______,固体N是_______;
(3)滤液X中,含铝元素的溶质的化学式为______,它属于_____![]() 填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐”![]() 类物质;
类物质;
(4)实验室里常往![]() 溶液中加入___________
溶液中加入___________![]() 填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液”![]() 来制取
来制取![]() ;
;
(5)将铝粉和氧化铁的混合物点燃,反应放出大量的热量,生成的液态的铁用来焊接铁轨。请写出反应的化学方程式:______________________________________。
【答案】过滤 烧杯、漏斗、玻璃棒 Fe2O3 Al2O3 NaAlO2 盐 氨水 ![]()
【解析】
铝土矿中加入浓NaOH溶液,![]() 和氢氧化钠不反应,氧化铝与NaOH反应生成NaAlO2,步骤I利用过滤除去
和氢氧化钠不反应,氧化铝与NaOH反应生成NaAlO2,步骤I利用过滤除去![]() ,沉淀M为氧化铁等不溶物,滤液X含有偏铝酸钠;步骤II通入二氧化碳将AlO2-转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝。
,沉淀M为氧化铁等不溶物,滤液X含有偏铝酸钠;步骤II通入二氧化碳将AlO2-转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝。
(1)I和II步骤分离固体与溶液的方法为过滤,所用的玻璃仪器为:烧杯、漏斗、玻璃棒;
故答案为:过滤;烧杯、漏斗、玻璃棒
(2)由工艺流程可知,沉淀M中还含有![]() ,固体N为
,固体N为![]() ,
,
故答案为:![]() ;
;![]() ;
;
(3)由工艺流程可知,滤液X中,含铝元素的溶质的化学式为:![]() ,NaAlO2属于盐,
,NaAlO2属于盐,
故答案为:![]() ;盐;
;盐;
(4)氢氧化铝溶于强碱,实验室通常用弱碱氨水与铝盐制备氢氧化铝沉淀,反应的方程式为![]()
故答案为:氨水;
(5)铝和氧化铁反应生成铁和氧化铝的方程式为:![]() ,
,
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A. 用湿润的pH试纸测稀碱液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从明矾[KAl(SO4)2·12H2O]制备Al、K2SO4和H2SO4的流程如下:

明矾焙烧的化学方程式为:4KAl(SO4)2·12H2O+3S![]() 2K2SO4+2Al2O3+9SO2↑+48H2O
2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂是_________________。
(2)步骤②中,为提高浸出率,可采取的措施有_____________。
A.粉碎固体混合物 B.降低温度 C.不断搅拌 D.缩短浸泡时间
(3)从水浸后的滤液中得到K2SO4晶体的方法是__________。
(4)步骤③电解的化学方程式是_______________,电解池的电极是用碳素材料做成,电解过程中,阳极材料需要定期更换,原因是:_________。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,则该电池的正极电极反应式是_________________________________。
(6)焙烧a吨明矾(摩尔质量为b g/mol),若SO2的转化率为96%,可生产质量分数为98%的H2SO4质量为______________________吨(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1 盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法正确的是( )

A.常温下,Kb(NH3·H2O)约为1×10-3
B.b=20.00
C.R、Q两点对应溶液均呈中性
D.R到N、N到Q所加盐酸体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下正戊烷(CH3CH2CH2CH2CH3)发生两种裂解反应:
Ⅰ.CH3CH2CH2 CH2CH3 (g)CH3CH===CH2(g)+CH3 CH3 (g) ΔH1=+274.2 kJ·mol-1
Ⅱ.CH3CH2CH2CH2CH3(g)CH3CH2CH3(g)+CH2===CH2(g) ΔH2=+122.7 kJ·mol -1
回答下列问题:
(1)在恒温恒压的密闭容器中,充入一定量的正戊烷发生裂解反应,起始时容器体积为 a L,一段时间反应达到平衡后容器体积变为 b L,此时正戊烷的转化率 α(正戊烷)=_________;向反应体系中充入一定量的水蒸气(水 蒸气在该条件下不参与反应),再次平衡后正戊烷的转化率将_____(填“增大”“减小”或“不变”),原因为_______________。
(2)温度为 T ℃时,往压强恒为 100 kPa 的密闭容器中充入 1 mol·L-1 CH3CH=CH2和 2 mol·L-1 CH3CH3发生反应:CH3CH===CH2(g)+CH3CH3(g) CH3CH2CH3(g)+CH2===CH2(g)ΔH3。测得 CH3CH2CH3 的物质的量浓度随时间 t 的变化如图中曲线Ⅰ所示。
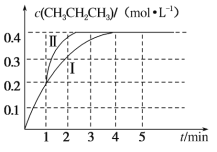
①ΔH3=_____。
②该反应的平衡常数 Kp=_____。(Kp 为以分压表示的平衡常数,分压=总压×物质的量分数,计算结果 保留 2 位小数)。
③若在 1 min 时,改变某一反应条件,曲线Ⅰ变为曲线Ⅱ,则改变的条件为_____。
(3)将 0.1 mol CH3CH3完全燃烧后的气体通入 100 mL 3 mol·L-1的 NaOH 溶液中,充分反应后所得溶液中离子浓度的大小顺序为_____。
(4)以稀硫酸为电解质溶液,CH3CH3 燃料电池的负极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机制药工业中常用以下方法合成一种药物中间体(G):


(1)G的分子式是___。
(2)化合物A中含氧官能团的名称为___。
(3)由C→D的反应类型为___;化合物E的结构简式为___。
(4)写出B→C的反应的化学方程式:___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应;
②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9;
③分子中含有氨基。
(6)已知:RCN![]() RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备
RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备![]() 的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH![]() CH2
CH2![]() CH2
CH2![]() CH3CH2Cl
CH3CH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4是中学常见的强氧化剂,用固体碱熔氧化法制备KMnO4的流程和反应原理如图:

反应原理:
反应I:3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
反应Ⅱ:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3
(墨绿色) (紫红色)
已知25℃物质的溶解度g/100g水
K2CO3 | KHCO3 | KMnO4 |
111 | 33.7 | 6.34 |
请回答:
(1)下列操作或描述正确的是___
A.反应Ⅰ在瓷坩埚中进行,并用玻璃棒搅拌
B.步骤⑥中可用HCl气体代替CO2气体
C.可用玻璃棒沾取溶液于滤纸上,若滤纸上只有紫红色而无绿色痕迹,则反应Ⅱ完全
D.步骤⑦中蒸发浓缩至溶液表面有晶膜出现再冷却结晶:烘干时温度不能过高
(2)___(填“能”或“不能”)通入过量CO2气体,理由是___(用化学方程式和简要文字说明)。
(3)步骤⑦中应用玻璃纤维代替滤纸进行抽滤操作,理由是___。
草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ.称取1.6000g高锰酸钾产品,配成100mL溶液
Ⅱ.准确称取三份0.5025g已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化;
Ⅲ.锥形瓶中溶液加热到75~80℃,趁热用I中配制的高锰酸钾溶液滴定至终点。
记录实验数据如表
实验次数 | 滴定前读数/mL | 滴定后读数/mL |
1 | 2.65 | 22.67 |
2 | 2.60 | 23.00 |
3 | 2.58 | 22.56 |
已知:MnO4﹣+C2O42﹣+H+→Mn2++CO2↑+H2O(未配平)
则KMnO4的纯度为___(保留四位有效数字);若滴定后俯视读数,结果将___(填“偏高”或“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断A(g)+B(g) ![]() C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
A. 压强不随时间改变
B. 气体的密度不随时间改变
C. c(A)不随时间改变
D. 单位时间里生成C和D的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴是国民经济建设和国防建设不可缺少的重要原料之一,从锂离子二次电池正极![]() 废料--铝钴膜中回收钴的工艺如图所示:
废料--铝钴膜中回收钴的工艺如图所示:

回答下列问题:
(1)写出工业上用![]() 制取铝的化学方程式______
制取铝的化学方程式______
(2)工艺图中加入氢氧化钠净化的目的是______
(3)为使钴浸出。需将![]() 的结构破坏,选择在硫酸和双氧水体系中进行浸出,请写出浸出的化学方程式______
的结构破坏,选择在硫酸和双氧水体系中进行浸出,请写出浸出的化学方程式______
(4)锂可由电解制得,以石墨为阳极,低碳钢为阴极,电解液为熔融的LiCl和KCl的混合液,电解槽压为6.0-6.5V,这样可得到纯度为99%的锂。
①在电解液中加人KCl的原因______
②阴极产物与镁的性质相似,在常温下与氮气反应,请写出其与氮气反应的生成物与水的反应方程式______
③已知阴极产物在500℃与氢气能反应生成氢化物,请写出该氢化物的电子式______
(5)已知钴与铁的性质相似,请写出四氧化三钴与氢碘酸反应的离子方程式______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com