
【题目】甲同学采用如图Ⅰ所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体。

(1)反应过程中的实验现象是__________________________________________________。
(2)乙同学认为虽然收集到的气体为一氧化氮,但并不能说明反应中一定生成一氧化氮。你认为他的理由是______________________________________________________________。
(3)丙同学采用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮。该同学的步骤如下表所示,请回答实验中的有关问题。
实验步骤 | 问题 |
①从U形管左端加入稀硝酸,直至充满U形管右端 | ______ |
②用附有铜丝的胶塞塞住U形管右端,观察现象 | 实验现象是______________ |
③待反应停止后打开胶塞,观察实验现象 | 打开胶塞后的实验现象是_______________________ |
(4)从环境保护的角度看,丙同学的实验存在__________缺陷?你认为应如何改进__________?
【答案】铜片逐渐溶解,溶液由无色变为蓝色,具支试管内液面上空出现少量红棕色气体,水槽试管内液面下降,收集到无色气体 若反应产生NO2,3NO2+H2O=2HNO3+NO,排水收集到的NO为NO2与H2O反应所得 U形管右端收集到无色气体,液面下降 铜丝溶解,溶液变蓝色 U形管左端液面上升 无色气体遇到空气变为红棕色气体 丙同学实验中没有尾气吸收装置;应在胶塞上安装一带活塞的导管并接入盛有O2的集气瓶中(合理均可)。
【解析】
(1)根据铜与稀硝酸的反应判断实验现象;
(2)根据观察到的现象确定并写出反应方程式;
(3)根据生成物的颜色推断现象;根据一氧化氮的性质推断现象;
(4)丙同学实验存在一定的缺陷,生成的NO进入空气中污染大气,同时生成的红棕色NO2被空气稀释颜色较浅,效果不明显,结合原理进行改进。
(1)铜和稀硝酸反应的方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则反应过程中的实验现象是铜片逐渐溶解,溶液由无色变为蓝色,具支试管内液面上空出现少量红棕色气体,水槽试管内液面下降,收集到无色气体;
(2) 若反应产生的是NO2,与水反应也能产生NO,3NO2+H2O=2HNO3+NO,排水收集到的NO为NO2与H2O反应所得;
(3)①从U形管左端加入稀硝酸,直至充满U形管右端,U形管右端收集到无色气体,液面下降;
②用附有铜丝的胶塞塞住U形管右端,观察现象:铜丝溶解,溶液变蓝色;
③待反应停止后打开胶塞,观察实验现象:U形管左端液面上升;
(4)从环境保护的角度看,丙同学的实验存在的缺陷为:无色气体遇到空气变为红棕色气体;改进方案为丙同学实验中没有尾气吸收装置;应在胶塞上安装一带活塞的导管并接入盛有O2的集气瓶中。


科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
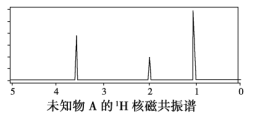
【题目】已知某有机物A的红外光谱和1H核磁共振谱如下图所示,下列说法中错误的是( )
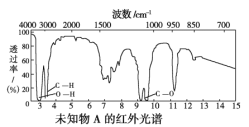
A. 由红外光谱图可知,该有机物中至少含有三种不同的化学键
B. 由1H核磁共振谱可知,该有机物分子中有三种不同的氢原子且个数比为1∶2∶3
C. 若A的化学式为C2H6O,则其结构简式为CH3CH2OH
D. 仅由其1H核磁共振谱就可得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3)经常用来修改错字,其结构如图所示。下列说法不正确的是( )
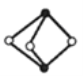
A.As、S原子的杂化方式均为sp3
B.AsH3的沸点比NH3的低
C.与As同周期且基态原子核外未成对电子数目相同的元素只有V
D.已知As2F2分子中各原子均满足8电子结构,分子中σ键和π键的个数比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li2O是离子晶体,从如图的BornHaber循环可得出Li2O晶格能为 ( )
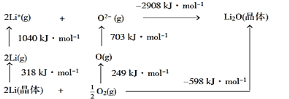
A. 598kJ·mol1B. -598KJ·mol1C. 1168kJ·mol1D. 2908kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①硫酸比次氯酸稳定②硫酸的酸性弱于高氯酸③![]() 比HCl易被氧化④
比HCl易被氧化④![]() 比
比![]() 更容易由单质合成⑤盐酸的酸性比氢硫酸强。上述事实能说明硫的非金属性比氯弱的是
更容易由单质合成⑤盐酸的酸性比氢硫酸强。上述事实能说明硫的非金属性比氯弱的是
A.①②③B.③④⑤C.②③④D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣![]()
![]() 溶液
溶液![]() 绿矾
绿矾![]() 铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42+16H+
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常采用“电催化氧化—化学沉淀法”对化学镀镍废水进行处理,电解过程中电解槽中H2O、Cl-放电产生·OH、HClO,在活性组分作用下,阴阳两极区发生的反应如下(R表示有机物):
①R+·OH→CO2+H2O
②R+HClO→CO2+H2O+Cl-
③H2PO![]() +2·OH-4e-=PO
+2·OH-4e-=PO![]() +4H+
+4H+
④HPO![]() +·OH-2e-=PO
+·OH-2e-=PO![]() +2H+
+2H+
⑤H2PO![]() +2ClO-=PO
+2ClO-=PO![]() +2H++2Cl-
+2H++2Cl-
⑥HPO![]() +ClO-=PO
+ClO-=PO![]() +H++Cl-
+H++Cl-
⑦Ni2++2e-=Ni
⑧2H++2e-=H2↑
下列说法不正确的是( )
A.·OH、HClO在阳极上产生
B.增大电极电压,电化学氧化速率加快
C.电解时,阴极附近pH逐渐升高,Ni2+去除率逐渐减小
D.向电解后的废水中加入CaCl2可以去除磷元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K、25℃,在NaHS溶液中,各离子的浓度随NaHS溶液浓度的变化关系如图所示,下列叙述不正确的是
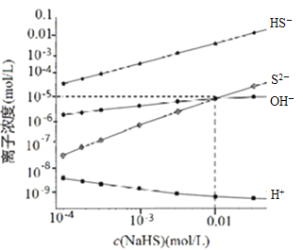
已知:298K(25℃)H2S的Ka1=9.10×10-8,Ka2=1.10×10-12。
A.0.10mol/LNaHS溶液:c(Na+)>c(HS)>c(S2)>c(OH)>c(H+)
B.Na2S溶液中:c(Na+)=2c(S2)+2c(HS)+2c(H2S)
C.随着c(NaHS)浓度的增大c(H+)也将持续增大
D.当c(OH)=c(S2)时,c(H+)=10-9mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com