
【题目】将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应: I2(g) + H2(g) ![]() 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示,则:
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示,则:
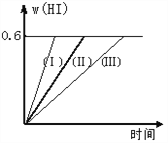
(1)达平衡时,I2(g)的物质的量浓度为___________ 。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是___________,则乙条件可能是___________ 。(填入下列条件的序号)
①恒容条件下,升高温度; ②恒容条件下,降低温度;
③恒温条件下,缩小反应容器体积;
④恒温条件下,扩大反应容器体积;
⑤恒温恒容条件下,加入适当催化剂。
【答案】 0.05mol/L ③⑤ ④
【解析】(1)该反应是一个反应前后气体体积不变的化学反应,所以反应后混合气体的物质的量是3 mol,同一容器中各种气体的体积分数等其物质的量分数,所以平衡时碘化氢的物质的量![]() ,则参加反应的
,则参加反应的![]() ,剩余的
,剩余的![]() ,所以平衡时c(I2)=0.1/2=0.05 mol/L .正确答案是: 0.05 mol/L。
,所以平衡时c(I2)=0.1/2=0.05 mol/L .正确答案是: 0.05 mol/L。
(2)在甲条件下![]() 的变化如曲线(Ⅰ) 所示,反应时间缩短,碘化氢的含量不变,说明该条件只增大了反应速率不影响平衡,增大压强和加入催化剂对该反应平衡无影,但都增大反应速率,缩短反应时间;在乙条件下
的变化如曲线(Ⅰ) 所示,反应时间缩短,碘化氢的含量不变,说明该条件只增大了反应速率不影响平衡,增大压强和加入催化剂对该反应平衡无影,但都增大反应速率,缩短反应时间;在乙条件下![]() 的变化如曲线(Ⅲ) 所示,反应时间变长,碘化氢的含量不变,说明反应速率减小,平衡不移动,所以是减小压强,即扩大容器体积;综上,则甲条件可能是③⑤;乙条件可能是④;正确答案:③⑤;④。
的变化如曲线(Ⅲ) 所示,反应时间变长,碘化氢的含量不变,说明反应速率减小,平衡不移动,所以是减小压强,即扩大容器体积;综上,则甲条件可能是③⑤;乙条件可能是④;正确答案:③⑤;④。


科目:高中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl杂质,现用如图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去;碱石灰是生石灰与氢氧化钠的混合物,可以吸收水和二氧化碳)。
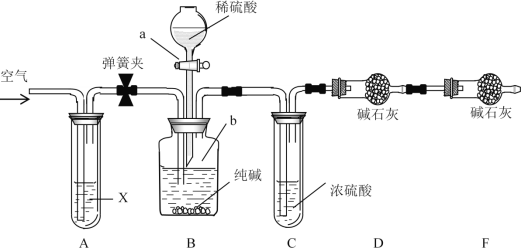
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20g;
③准确称得20.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥然后称得干燥管D的总质量为86.36g ;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,为86.80 g。
试回答:
(1)装置B中发生反应的离子方程式_________________________________;
(2)装置A中试剂X应选用足量的(______)
A.饱和NaCl溶液 B.浓H2SO4
C.NaHCO3溶液 D.NaOH溶液
(3)①请用文字叙述装置C的作用:__________________________________。
②请用文字叙述装置E的作用:__________________________________。
(4)如果将分液漏斗中的硫酸换成浓度相同的盐酸,则会导致测定结果_____(填“偏大”、 “偏小”或“不变”,下同);若没有操作⑤⑦,则会导致测定结果__________。
(5)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯装置,请根据装置回答问题:
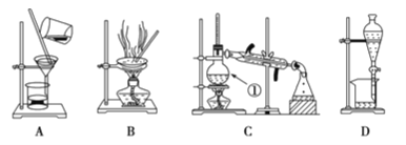
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是_______,装置C中冷凝水从____通入。
(2)装量C中①的名称是________,装置D中的分液漏斗在使用之前应该进行的操作为__________,在分液时为使液体顺利滴下,应进行的操作为________________________。
(3)青蒿素是从复合花序植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯的一种无色针状晶体,是一种高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在乙醇、乙醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。
已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:
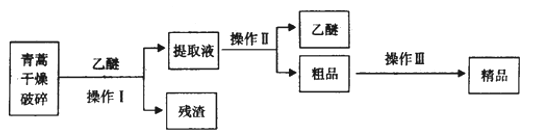
若要在实验室模拟上述工艺,操作Ⅰ选择的装置是_______,操作Ⅱ的名称是________,操作Ⅲ的主要过程可能是_______(填字母)
A. 加95%的乙醇,浓缩、结晶、过滤
B. 加水溶解,蒸发浓缩、冷却结晶、过滤
C. 加入乙醚进行萃取分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择装置,完成实验。

(1)用饱和食盐水除去氯气中的氯化氢,应选用______(填序号,下同)。
(2)除去食盐水中的泥沙,应选用______。
(3)用自来水制取蒸馏水,应选用______。
(4)用四氯化碳提取碘水中的碘,应选用______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法不正确的是

A. 稀释后A酸溶液的酸性比B酸溶液弱
B. a=5时,A是强酸,B是弱酸
C. 若A、B都是弱酸,则5>a>2
D. A、B两种酸济液物质的量浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列状态的物质①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖
其中属于电解质的是___________ ,属于强电解质的是_____________。能导电的是___________。
Ⅱ.胶体是一种常见的分散系,回答下列问题。
①向煮沸的蒸馏水中逐滴加入___________溶液,继续煮沸至____________,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为______________________________________________。
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于_______离子(填离子符号)的作用,使胶体形成了沉淀,这个过程叫做_______________。
③区分胶体和溶液常用的方法叫做__________。
Ⅲ.①FeCl3溶液用作蚀刻铜箔制造电路板的工艺,离子方程式为_________________________。
②有学生利用FeCl3溶液制取FeCl36H2O晶体主要操作包括:滴入过量盐酸,______、冷却结晶、过滤。过滤操作除了漏斗、烧杯还需要什么玻璃仪器________________。
③高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化关系如图所示。下列说法错误的是( )
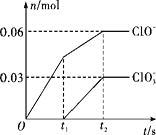
A. Cl2和苛性钾溶液在不同温度下可能发生不同反应
B. 反应中转移电子数为是0.42NA
C. 原苛性钾溶液中KOH的物质的量为0.3 mol
D. 生成物中Cl-的物质的量为0.21 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O中,_____元素的原子失去电子,被________;________________作氧化剂,若参加反应的HCl是73g,则被氧化的HCl是________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com