
【题目】(1)下列物质:①.Cu ②.NaCl晶体 ③.NaHSO4 ④.CO2 ⑤.CaO ⑥HCl ⑦.稀H2SO4 ⑧. 熔融Ba(OH)2 ⑨.C2H5OH ⑩.NaCl溶液。
属于电解质的是(填序号,下同)_____,属于非电解质的是_____,能导电的是______。
(2)写出下列物质在水溶液中的电离方程式:
①NaHSO4 ___________________________;
②Al2(SO4)3 ________________________________;
③NH4NO3 ________________________。
(3)按要求写出下列方程式:
①写出硫酸铜溶液中滴加氢氧化钠溶液的反应的离子方程式:_____________。
②写出能用离子方程式CO32-+2H+=CO2↑+H2O表示的一个化学方程式:__________。
【答案】②③⑤⑥⑧ ④⑨ ①⑦⑧⑩ NaHSO4=Na++H++SO42- Al2(SO4)3=2Al3++3SO42- NH4NO3=NH4++NO3- Cu2++2OH-==Cu(OH)2↓ Na2CO3+2HCl=2NaCl+CO2↑+H2O(或其他)
【解析】
(1)在水溶液里或熔化状态下能够自身电离出离子的化合物是电解质,属于电解质的是NaCl晶体、NaHSO4、CaO、HCl、熔融Ba(OH)2,答案选②③⑤⑥⑧;在水溶液里和熔融状态下都不能自身电离出离子的化合物是非电解质,属于非电解质的是CO2、C2H5OH,答案选④⑨;含有自由移动电子或离子的物质可以导电,能导电的是Cu、稀H2SO4、熔融Ba(OH)2、NaCl溶液,答案选①⑦⑧⑩;(2)①NaHSO4在水溶液中的电离方程式为NaHSO4=Na++H++SO42-;②Al2(SO4)3在水溶液中的电离方程式为Al2(SO4)3=2Al3++3SO42-;③NH4NO3在水溶液中的电离方程式为NH4NO3=NH4++NO3-。(3)①硫酸铜溶液中滴加氢氧化钠溶液生成氢氧化铜沉淀和硫酸钠,反应的离子方程式为Cu2++2OH-==Cu(OH)2↓:②能用离子方程式CO32-+2H+=CO2↑+H2O表示的一个化学方程式可以是Na2CO3+2HCl=2NaCl+CO2↑+H2O。
点睛:化合物在水溶液中或受热熔化时本身能否发生电离是区别电解质与非电解质的理论依据,能否导电则是实验依据。因此能导电的物质不一定是电解质,如石墨;电解质本身不一定能导电,如NaCl晶体。
【题型】填空题
【结束】
27
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A________,B____________。
(2)写出上述过程中有关反应的化学方程式:
Fe2O3→A_______________________;A→B____________________________。
(3)B→C可看到的现象是___________________________________________。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
【答案】血红色 不变(浅绿色) Fe2O3+6HCl=2FeCl3+3H2O Fe+2FeCl3=3FeCl2 白色沉淀转变为灰绿色又转变为红褐色 Fe(OH)3 丁达尔
【解析】
(1)氧化铁与盐酸反应生成氯化铁,氯化铁与铁反应生成氯化亚铁,因此往A、B溶液中分别滴入几滴KSCN溶液,溶液A中显血红色,B中不变色;(2)Fe2O3与盐酸反应的方程式为Fe2O3+6HCl=2FeCl3+3H2O,A→B的方程式为Fe+2FeCl3=3FeCl2。(3)氯化亚铁与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化,所以B→C可看到的现象是白色沉淀转变为灰绿色又转变为红褐色。(4)将氯化铁饱和溶液滴入沸水中并不断加热,可制得氢氧化铁胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为丁达尔效应。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的前四周期元素。A是宇宙中含量最丰富的元素;D与E同主族,且E的原子序数是D的两倍;B与D组成的化合物是一种温室气体;C元素原子最外层P能级比S能级多1个电子;F原子的最外层电子数与A相同,其余各层电子均充满。据此回答下列问题。
(1)F元素形成的高价基态离子的核外电子排布式为____________________________。
(2)E的一种具有强还原性的氧化物分子的VSEPR模型为____________________。
(3)C、D、E元素的第一电离能由大到小排序_________________。(用元素符号表示)
(4)A和D形成的18电子化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___________________________。
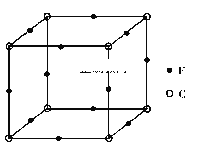
(5)F与C形成化合物的晶胞如图所示,该化合物的化学式为__________,C离子的配位数是_________。此立方晶体的边长为a cm,则该晶体密度为__________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是( )




①除去CO2中HCl ②吸收Cl2 ③检查装置气密性 ④利用排空气法收集CO2
A. ①④ B. ②④ C. ②③ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态铜原子价电子排布式为____________;第一电离能I(Cu)________I (Zn)(填“>”或“<”)
(2)配合物[Cu (CH3CN) 4] BF4[四氟硼酸四(乙腈)合铜(Ⅰ)]是有机合成中常见催化剂。
①该配合物中阴离子的空间构型为__________,与其互为等电子体的分子或离子是________(各举1例)。
②配体分子中与Cu(I) 形成配位键的原子为____________;配体CH3CN 中:碳原子杂化方式是______。
(3)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,Cu2O 属于____晶体,前者熔点较高,其原因是______________________________________________________________________________
(4)Cu3N 的晶胞(立方)结构如下图所示:
①距离最近的两个Cu+间的距离为________nm。(保留两位小数)
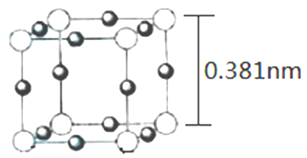
②Cu3N 晶体的密度为____________ g·cm-3。(列出计算式,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时, Ksp (AgCl)= 1.56×10-10, Ksp(Ag2CrO4)= 9.0×10-12,下列说法正确的是
A. AgCl 和 Ag2CrO4 共存的悬浊液中,![]()
B. 向Ag2CrO4悬浊液中加入 NaCl 浓溶液, Ag2CrO4不可能转化为 AgCl
C. 向 AgCl 饱和溶液中加入 NaCl 晶体, 有 AgC1 析出且溶液中 c(Cl-)=c(Ag+)
D. 向同浓度的 Na2CrO4和 NaCl 混合溶液中滴加 AgNO3溶液,AgC1先析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A________,B____________。
(2)写出上述过程中有关反应的化学方程式:
Fe2O3→A_______________________;A→B____________________________。
(3)B→C可看到的现象是___________________________________________。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
【答案】血红色 不变(浅绿色) Fe2O3+6HCl=2FeCl3+3H2O Fe+2FeCl3=3FeCl2 白色沉淀转变为灰绿色又转变为红褐色 Fe(OH)3 丁达尔
【解析】
(1)氧化铁与盐酸反应生成氯化铁,氯化铁与铁反应生成氯化亚铁,因此往A、B溶液中分别滴入几滴KSCN溶液,溶液A中显血红色,B中不变色;(2)Fe2O3与盐酸反应的方程式为Fe2O3+6HCl=2FeCl3+3H2O,A→B的方程式为Fe+2FeCl3=3FeCl2。(3)氯化亚铁与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化,所以B→C可看到的现象是白色沉淀转变为灰绿色又转变为红褐色。(4)将氯化铁饱和溶液滴入沸水中并不断加热,可制得氢氧化铁胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为丁达尔效应。
【题型】实验题
【结束】
28
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。

I、探究浓硫酸的某些性质
(1)按图示连接装置,检查装置___________,称量E的质量。
(2)将aɡ铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为______,未点燃酒精灯前,A、B 均无明显现象,其原因是______________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象,如A中![]() ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
(4)随着反应的进行,浓硫酸浓度逐渐减小变为稀硫酸,A中还可能发生某些离子反应,写出相应的离子方程式:_________________、____________________。
II、测定铁的质量分数
(5)待A中固体完全消失并不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为___________________(写表达式)。
(6)某同学认为上述方法较复杂,使用如图所示的装置和其他常用的实验仪器测定某些数据即可。为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。

①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年诺贝尔化学奖由法国、美国及荷兰的三位化学家分获,以表彰他们在分子机器设计与合成领域方面的成就,其中一种光驱分子马达结构如右图所示。有关该分子的说法不正确的是

A. 光驱分子马达的分子式是C34H46O2,属于烃的含氧衍生物
B. 分子机器设计与合成的研究成果为未来新材料的研发开启了广阔前景
C. 三位科学家通过研究质子和中子重新合成了新的元素
D. 光驱分子马达能与NaHCO3和酸性KMnO4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七种短周期主族元素①~⑦,其原子序数依次增大,②元素是地壳中含量最多的,⑤元素为两性元素,④⑦两元素组成的化合物是我们日常生活必须的调味品,②和⑥元素的原子序数之和是①和④两元素原子序数之和的两倍。请用化学用语回答下列问题:
(1)③、⑤、⑥的简单离子半径由大到小的顺序为_______________________。
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为___________>___________。
(3)写出二氧化硅与含上述某种元素的酸反应的化学方程式_________________。
(4)由⑤和空气、海水构成的原电池中,其正极反应式为_____________________。
(5)由上述元素形成的物质可发生下图中的反应,其中B、C、G 是单质,B为黄绿色气体。
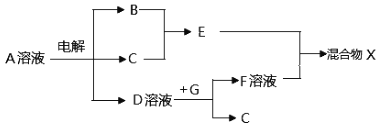
①写出D溶液与G反应的化学方程式________________________________。
②混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,写出能解释它在苛性钠溶液中发生反应的原因的电离方程式_________________________________。
③写出电解A溶液的离子方程式_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com