
【题目】一定温度下,将 2 mol SO2 和 1 mol O2 充入一定容密闭容器中,在催化剂存在下进行下列反应: 2SO2(g)+ O2(g) ![]() 2SO3(g);当达到平衡状态时,下列说法中正确的是
2SO3(g);当达到平衡状态时,下列说法中正确的是
A. 生成 SO3 为2 mol
B. 反应完全停止
C. SO2 和 SO3 物质的量之和为 2mol
D. SO2 的物质的量和SO3 物质的量相等
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如下图所示。

(1)由图中所给数据进行分析,该反应的化学方程式为_______________。
(2)反应从开始至2min末,用Z(为气态)的浓度变化表示的平均反应速率为_______ mol/(L·min)。
(3)当反应进行到第_____min时,该反应达到平衡。反应达到平衡后,下列措施一定能加快化学反应速率的有____
A.增大Z的量 B.升高温度
C.使用正催化剂 D.增大X或Y的量
(4)分别用X和Y的反应速率来表示已达到化学平衡状态的表达式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能源和作为能源的物质叙述错误的是( )
A. 化石能源物质内部蕴涵着大量的能量
B. 绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C. 吸热反应是反应物总能量大于生成物的总能量
D. 物质的化学能可以在不同的条件下转化为热能、电能被人类利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在溶液中可以大量共存的是
A. H+、AlO2-、Cl-、S2- B. Na+、K+、NH4+、CO32-
C. Br-、Al3+、Cl-、HCO3- D. Ba2+、OH-、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、一定温度下,在容积为V L的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应化学方程式中![]() =______。
=______。
(2)t1到t2时刻,以N的浓度变化表示的平均反应速率为:______。
(3)下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中M与N的物质的量之比为1︰1
B.N的质量分数在混合气体中保持不变
C.单位时间内每消耗a mol N,同时生成b mol M
D.混合气体的总物质的量不随时间的变化而变化
E.混合气体的压强不随时间的变化而变化
F.混合气体的总质量不随时间的变化而变化
II、某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:

实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
试回答下列问题:
(1)试分析实验①中t1~t2速率变化的主要原因是____,t2~t3速率变化的主要原因是___。
(2)实验②放出氢气的量减少的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。
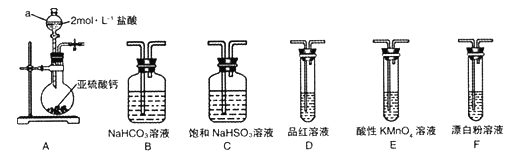
(1)装置A中仪器a的名称为__________。若利用装置A中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理________________。
(2)选用图4中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是_________________。
②丙同学设计的合理实验方案为:按照A→C→_________→F→尾气处理(填字母) 顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是_____________________。
③其中装置C的作用是__________。常温下,测得装置C中饱和NaHSO3溶液的pH≈5,则该溶液中所有离子的浓度由大到小的顺序为__________________。(已知0.1mol/L的H2SO3溶液pH >1)
(3)为了测定装置A残液中SO2的含量,量取10.00 mL残液于圆底烧瓶中,加热使SO2 全部蒸出,用20.00 mL0.0500 mol/L的KMnO4溶液吸收。充分反应后,再用0.2000mol/L的KI标准溶液滴定过量的KMnO4 ,消耗KI溶液15.00 mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为_______g·L-1。
②若滴定过程中不慎将KI标准溶液滴出锥形瓶外少许,使测定结果_______(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 符合同一通式的两种有机物一定互为同分异构体
B. 苯乙烯分子中的所有碳原子可能在同一平面上
C. 同分异构现象的存在是有机物种类繁多的原因之一
D. 乙醇和乙酸生成酯和酯的水解反应都属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.物质的量是衡量物质质量大小的物理量
B.摩尔质量即相对分子质量
C.摩尔是物质的量的单位
D.气体摩尔体积是指单位物质的量的物质所占的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com