
【题目】将一定质量的镁铝合金投入到200 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加 5 mol L-1的NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。求:

(1)原合金中Mg的质量 g;Al的质量 g
(2)盐酸的物质的量浓度 mol/L。
【答案】(1)m(Mg)=4.8g,m(Al)=2.7g;(2)4mol·L-1。
【解析】
试题分析:(1)2Al+6H+=2Al3++3H2↑,Mg+2H+=Mg2++H2↑,Al3++3OH-=Al(OH)3↓,Mg2++2OH-=Mg(OH)2↓,Al(OH)3+OH-=AlO2-+2H2O,因此11.6g沉淀是Mg(OH)2,根据镁元素守恒,即n(Mg)=n[Mg(OH)2]=11.6/58mol=0.2mol,即m(Mg)=0.2×24g=4.8g,19.4g是氢氧化铝和氢氧化镁总质量,即m[Al(OH)3]=(19.4-11.6)g=7.8g,根据铝元素守恒,n(Al)=n[Al(OH)3]=7.8/78mol=0.1mol,因此m(Al)=0.1×27g=2.7g;(2)加入20mLNaOH溶液,恰好中和剩余的盐酸,此时溶液中溶质溶质为AlCl3、MgCl2、NaCl,根据氯元素守恒,n(HCl)=3n(AlCl3)+2n(MgCl2)+n(NaCl)=3×0.1+2×0.2+20×10-3×5=0.8mol,c(HCl)=0.8/200×10-3mol·L-1=4mol·L-1。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式 。
(2)某同学设计的下列滴定方式中,最合理的是___________(夹持部分略去)(填字母序号)
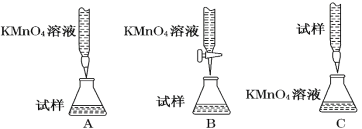
(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管、玻璃棒外,还需 (填仪器名称)。在溶液配制过程中,下列操作会导致配制结果偏低的是___________(填写代号)。
a.定容时,俯视容量瓶刻度线
b.容量瓶在使用前内有少量蒸馏水
c.转移溶液后的烧杯、玻璃棒未洗涤
d.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
A.浓盐酸 B.稀硫酸 C.稀硝酸 D.浓硫酸
方案二 称量法:操作流程如下:

(5)写出步骤②中H2O2氧化Fe2+ 的离子方程式 。步骤②中除用H2O2外还可以使用的物质是 ,步骤②是否可以省略 ,理由是 。
(6)步骤④一系列操作依次是:过滤、洗涤、 、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
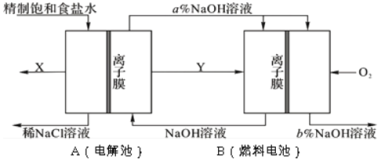
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.石油经过分馏得到多种烃,煤经过分馏可制得焦炭、煤焦油等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是( )
A.前2s,N2O4的平均反应速率为0.005mol·L-1·s-1
B.平衡时,N2O4的转化率为60%
C.平衡时,体系内NO2为0.04mol·L-1
D.在2s时,体系内压强为反应前的1.1倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是( )

A. 该装置为电解池
B. 本实验牺牲了金属Fe来保护金属Zn
C. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将基态P原子的电子排布式写成1s22s22p63s23px23py1,它违背了
A. 泡利原理 B. 能量守恒原理 C. 构造原理 D. 洪特规则
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.向0.1mol![]() CH3COOH溶液中加入少量水,溶液中
CH3COOH溶液中加入少量水,溶液中![]() 减小
减小
B.将CH3COONa溶液从20℃升温至60℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]()
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com